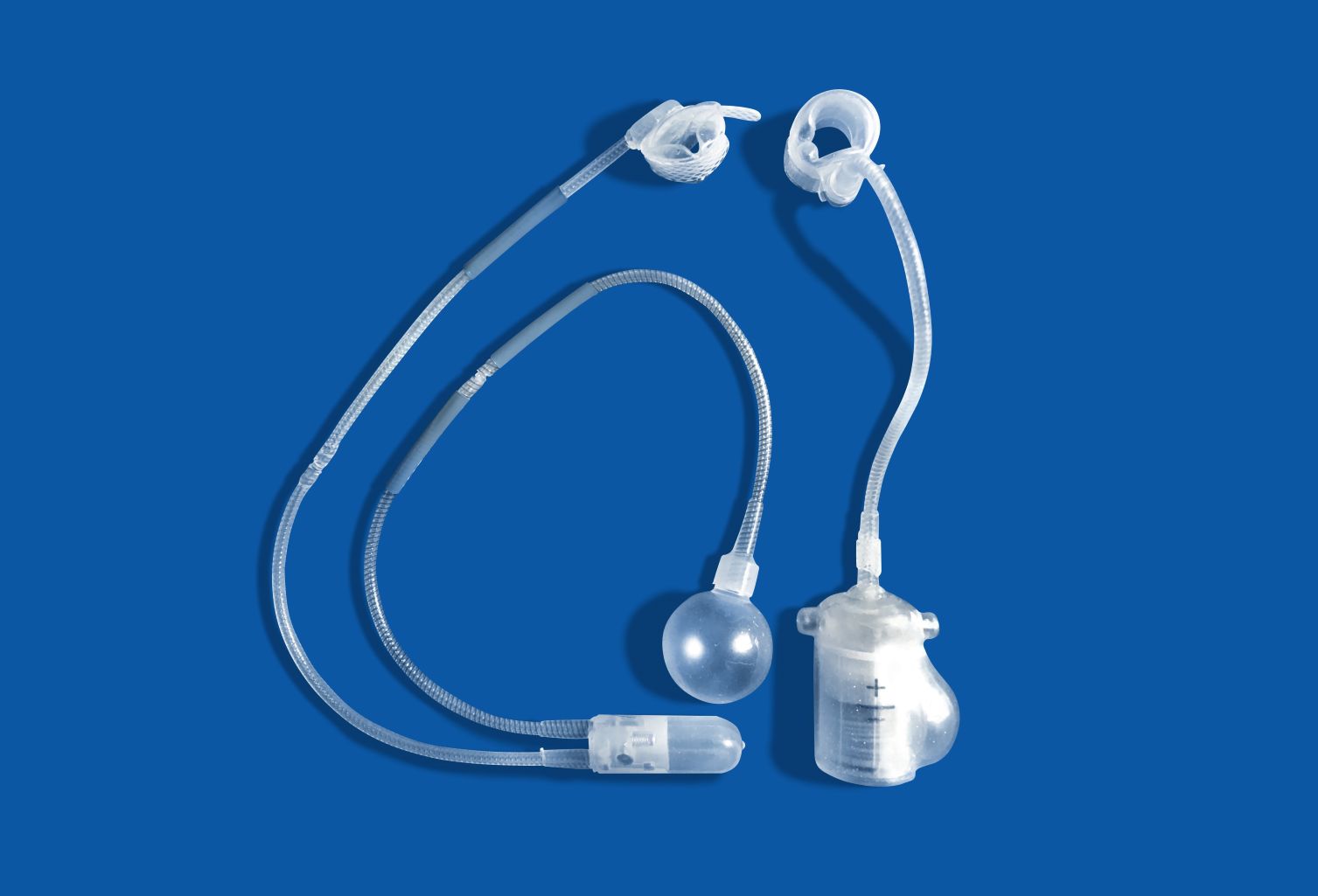
Warum ist die Oberfläche eines Implantats so wichtig?
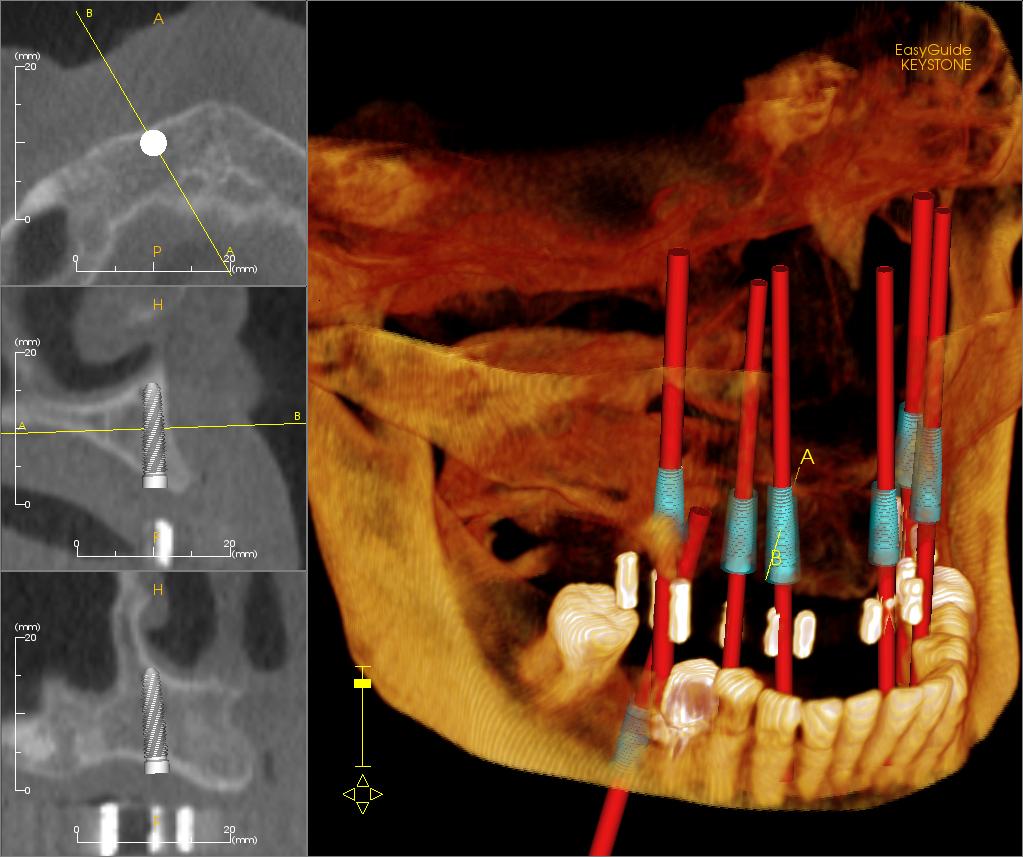
In der Biomaterialtechnik neigt man leicht dazu, sich auf die aus der traditionellen Materialwissenschaft abgeleitete Intuition zu verlassen: Da ein Implantat Belastungen standhalten, nicht korrodieren, sich nicht übermäßig abnutzen und über Jahre hinweg funktionieren muss, sollte sein Erfolg in erster Linie vom Material „im Inneren“ abhängen. Dies ist jedoch nur ein Teil der Wahrheit. Das Grundmaterial sorgt für Festigkeit, Steifigkeit, Elastizität, Haltbarkeit und Durchlässigkeit. Für den Körper beginnt der entscheidende Kontakt jedoch nicht mit dem gesamten Materialblock, sondern mit seiner äußeren Schicht. Dabei kommt diese Schicht mit Blut, Proteinen, Zellen und anderen Körperflüssigkeiten in Kontakt. In der Praxis kann ein Implantat also mechanisch überzeugen, biologisch aber Probleme verursachen, wenn seine Oberfläche „falsche Signale“ an das Gewebe sendet.
Diese Erkenntnis verändert unsere Sicht auf das Implantatdesign. Statt also nur zu fragen: „Aus welchem Material sollte das Implantat bestehen?“, müssen wir uns auch überlegen, wie seine Oberfläche beschaffen sein sollte. Bei Biomaterialien ist die biologische Reaktion kein einfaches Spiegelbild der chemischen Zusammensetzung des gesamten Bauteils. Sie ist vielmehr eine Reaktion auf das, was an der Grenzfläche zwischen Material und Gewebe geschieht: die Oberflächenchemie, Benetzbarkeit, Ladung, Rauheit, Organisation und Reaktivität. Deshalb wird der Erfolg eines Implantats so oft nicht durch das Volumen des Materials bestimmt, sondern genau an der Phasengrenze.
Dieser Artikel basiert auf Biomaterials Science: An Introduction to Materials in Medicine, hrsg. von William R. Wagner et al., 4. Auflage, 2020. Der folgende Inhalt ist nur ein allgemeiner Überblick über das Thema. Interessierten empfehlen wir, sich eingehender mit der Literatur zu befassen.
Wie reagiert der Körper auf die Oberfläche eines Materials?
Kurz gesagt: Der Körper nimmt das Implantat nicht als Ganzes wahr. Stattdessen „liest“ er zunächst die Oberfläche. Laut den Autoren von „Biomaterials Science“ übertragen sich Informationen vom Material auf Proteine, Zellen und den gesamten Organismus über die Oberflächenstruktur, sofern das Material keine unerwünschten Substanzen freisetzt. Entscheidend ist daher weniger das durchschnittliche Verhalten des gesamten Materials als vielmehr die spezifische Chemie und Organisation seiner äußersten Schicht. Diese scheinbar geringfügige Verlagerung des Schwerpunkts hat enorme praktische Bedeutung, da sie die Frage der Biokompatibilität von der Ebene „welche Art von Legierung oder Polymer wir haben“ auf die Ebene „wie ihre Grenzfläche aussieht und sich verhält“ verlagert.
Man sollte stets bedenken: Die Oberfläche ist nicht einfach das Ende des Materials, das sich genau wie das Innere verhält. Das Buch betont, dass die Oberfläche eine Zone besonderer Reaktivität ist, die sich fast zwangsläufig vom Materialinneren unterscheidet. Bei einem echten metallischen Material kann die äußere Schicht nicht nur Metalloxid, sondern auch adsorbiertes Wasser, polare organische Verbindungen und Kohlenwasserstoffverunreinigungen enthalten. Die Oberflächenzone von Polymeren ist einzigartig und liegt zwischen 10 und 100 nm. Das ist wichtig, denn selbst wenn das Material im Inneren homogen ist, kann sein biologisch aktiver Anteil chemisch und strukturell komplex sein.
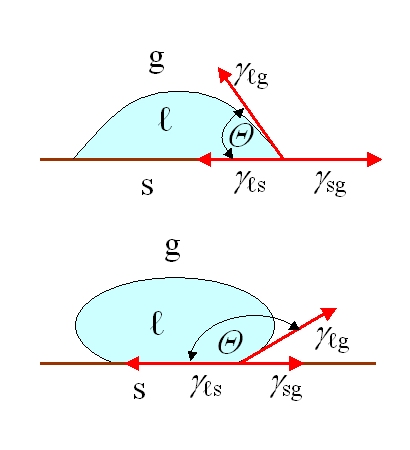
Biologisch betrachtet kommt es an der Oberfläche also nicht allein auf die chemische Zusammensetzung an. Die Autoren führen zahlreiche Merkmale auf, die biologische Reaktionen beeinflussen können: Rauheit, Muster und Topografie, Benetzbarkeit, Oberflächenmobilität, chemische Zusammensetzung, elektrische Ladung, Kristallinität, Elastizitätsmodul und Heterogenität. Gleichzeitig geben sie offen zu, dass es noch nicht möglich ist, ein einzelnes universelles Merkmal zu finden, das für jede biologische Reaktion entscheidend ist. In der Praxis heißt das: Man sollte ein Design nie auf einen einzelnen parametrischen Slogan wie „Lasst uns die Rauheit erhöhen“ oder „Lasst uns die Oberfläche hydrophiler machen“ reduzieren, denn die Reaktion des Körpers entsteht aus dem Zusammenspiel mehrerer Eigenschaften zugleich.
So lässt sich erklären, warum zwei Implantate aus demselben Grundmaterial biologisch unterschiedlich reagieren können. Schon kleine Änderungen in Verarbeitung, Sterilisation, Lagerung oder Verpackung können die Oberfläche verändern. Das Buch zeigt, dass schon Fingerabdrücke, aus der Verpackung migrierende Zusatzstoffe oder Verunreinigungen durch Papier oder Folie den Ausgang beeinflussen können. Im Labor erscheinen solche Effekte oft als Randphänomene, in der Praxis jedoch können sie dazu führen, dass wir eine Oberfläche testen, die nicht mehr der Beschaffenheit des später implantierten Produkts entspricht.

Wie sich die Oberfläche auf die Biokompatibilität auswirkt
Da die Oberfläche als primäre Sprache zwischen Implantat und Körper dient, fragen wir uns, wie dieser Dialog aussieht. Eine zentrale Rolle spielt dabei die Proteinadsorption. Schon Sekunden nach der Implantation eines synthetischen Biomaterials lagern sich an dessen Oberfläche adhäsive Proteine an, betont die Quelle. So wird ein Material, das an sich keine biologischen Erkennungsmuster besitzt, für den Körper lesbar. Kurz gesagt: Zellen reagieren nicht auf das reine Material, sondern auf die kurz nach dem Kontakt entstehende Proteinschicht.
Das beeinflusst unser Verständnis von Biokompatibilität maßgeblich. Biokompatibilität heißt eben nicht nur, dass kein akutes Giftpotenzial besteht. Sie beschreibt vielmehr die Fähigkeit des Materials, in einer bestimmten Anwendung die passende Reaktion des Wirts hervorzurufen. Was „angemessen“ heißt, hängt vom Einsatzgebiet ab – ein Stent, ein orthopädisches Implantat und ein Katheter verlangen jeweils etwas anderes. Dabei bestimmt die Oberfläche, welche Proteine in welcher Anordnung adsorbieren, welche Zellrezeptoren stimuliert werden und ob die Reaktion in Richtung Gewebeintegration, Thrombozytenaktivierung, Biofilmbildung oder Fremdkörperreaktion verläuft.
Ein anschauliches Beispiel dafür liefert der Vergleich von Adhäsions- und Passivierungsproteinen. Das Buch zeigt, dass eine Vorbeschichtung mit Fibronektin die Adhäsion vieler Zellen verstärkt, während Albumin sie bremsen kann. Das ist kein bloßes Kuriosum aus der Zellkultur, sondern ein Modell für das, was bei Implantaten passiert. Die Oberfläche ist kein neutraler Hintergrund. Sie bestimmt damit die Startbedingungen für alles, was danach zellulär folgt. In der Praxis können zwei Oberflächen mit ähnlicher mechanischer Festigkeit deshalb zu deutlich unterschiedlichen Heilungsverläufen führen, allein wegen der variierenden Zusammensetzung der ersten Schicht adsorbierter Proteine.
Ebenso wichtig sind die Wechselwirkungen zwischen der Oberfläche und Mikroorganismen. Im Kapitel über Biofilme weisen die Autoren darauf hin, dass Benetzbarkeit, Ladung, Rauheit und Topografie die bakterielle Adhäsion beeinflussen. Meist begünstigt stärkere Rauheit die Adhäsion, ebenso tun das hydrophobe Oberflächen. Allerdings gibt es Ausnahmen: Sehr superhydrophile oder superhydrophobe Systeme können als Biofilmhemmer wirken, allerdings über einen anderen Mechanismus. In der Praxis ist das ein klarer Warnhinweis: Was der Gewebeintegration nutzt, schadet unter Umständen der Kontrolle der bakteriellen Besiedlung.
Zum Abschluss sehen Sie ein englischsprachiges Video mit dem Titel „BIOE 5820 Biomaterials Protein Adsorption“, eine Vorlesung über die Proteinadsorption an Biomaterialoberflächen.
Warum die Oberfläche modifizieren statt das gesamte Material?
Das ist der Hauptgrund für die Oberflächenmodifikation. Das Grundmaterial sorgt für Tragfähigkeit, Haltbarkeit und mechanische Funktion, während die Oberfläche die Biointeraktion steuert. Darum macht es Sinn, das im Kern bereits Gutfunktionierende zu bewahren und lediglich die Zone zu verändern, die mit dem Gewebe in Kontakt tritt. Genau das empfehlen die Autoren des Kapitels über physikalisch-chemische Oberflächenmodifikationen. Das Ziel besteht darin, die wesentlichen physikalischen Eigenschaften des Biomaterials zu erhalten und gleichzeitig nur die äußere Schicht zu verändern, um die biologische Reaktion an der Schnittstelle zwischen Gewebe und Implantat zu verbessern oder zu modulieren.
Dieser Ansatz bietet mehrere praktische Vorteile. So muss kein Material aufgegeben werden, das mechanisch und technologisch gut verstanden ist. Titan, Stahl, technische Kunststoffe oder Elastomere behalten dadurch ihre bewährte tragende oder funktionelle Rolle. Zweitens lässt sich die biologische Reaktion exakt auf die jeweilige Anwendung zuschneiden. So braucht ein Knochenimplantat eine andere Oberfläche als eine Komponente, die mit Blut in Kontakt kommt, oder ein Katheter, bei dem es vor allem darum geht, die Proteinadsorption sowie die Anhaftung von Zellen oder Bakterien zu begrenzen. Viertens lässt sich durch eine gezielte Oberflächenmodifikation die Leistung eines Produkts steigern, ohne die Grundstruktur neu entwerfen zu müssen. Besonders bei bereits in der klinischen Praxis etablierten Produkten lässt sich so der biologische Effekt anpassen, ohne dass ein kompletter Neuentwurf, eine Umstellung der Produktion oder eine Schulung des Personals nötig wäre.
Dabei gilt eine Bedingung: Wichtig ist nur, dass man echte Schnittstellenmodifikationen von rein kosmetischen Beschreibungsänderungen unterscheidet. Wer behauptet, ein Material sei „bioaktiv“ oder „antifouling“, liefert ohne Kenntnis der endgültigen Oberflächenstruktur nach Verarbeitung und Sterilisation kaum brauchbare Informationen. Die Quelle betont, dass die untersuchte Probe dem Material oder Gerät, so wie es in biologischen Tests oder Implantationen eingesetzt wird, möglichst exakt entsprechen muss. Das ist entscheidend, denn die Oberfläche, die an der Luft liegt, kann sich von der Version unterscheiden, die im wässrigen Milieu des Körpers wirkt.
Drei Hauptmethoden der Oberflächenmodifizierung
Bei der ersten Methode verändern wir die Oberfläche, ohne eine zusätzliche Schicht aufzutragen. Dabei werden Atome, Moleküle und Bindungen der äußersten Schicht entweder chemisch oder physikalisch umgewandelt. Dazu zählen Ätzen, chemische Aktivierung, mechanische Aufrauhung, Ionenimplantation und bestimmte Laserbehandlungen. Entscheidend ist, dass wir die Oberfläche des Implantats nicht durch eine neue Schicht ergänzen, sondern sie direkt umgestalten. Dies ist vorteilhaft, wenn eine starke Integration der Modifikation mit dem Substrat wichtig ist, sowie zur Verringerung des Risikos der Delaminierung und zur Veränderung von Eigenschaften wie Reaktivität, Benetzbarkeit, Korrosionsbeständigkeit, Härte oder Bioaktivität. Die Quelle zeigt beispielsweise, dass sich durch Ionenimplantation die Verschleißfestigkeit oder Korrosionsbeständigkeit verbessern lässt und sich durch Laserbearbeitung die Oberflächenrauheit, Kristallinität und Chemie kontrolliert verändern lassen.
Beim zweiten Ansatz wird eine neue Schicht oder Beschichtung aufgebracht. Dabei wird ein Material mit anderer Zusammensetzung oder anderen Eigenschaften auf die vorhandene Oberfläche aufgetragen. Dies kann ein Dünnfilm, eine aufgepfropfte Schicht, eine Polymerbeschichtung oder ein als nicht-verwachsende Oberfläche konzipiertes System sein. Diese Strategie ist besonders wertvoll, wenn das Substrat ideale mechanische Eigenschaften aufweist, aus biologischer Sicht jedoch zu „roh“ ist. Ein anschauliches Beispiel dafür sind Oberflächen, die sich gegen unspezifische Proteinadsorption wehren. Meist entsteht dieser Effekt durch eine dichte Hydratationsschicht, die Proteine energetisch und physikalisch abblockt. Im Kapitel über nicht-verfoulingende Oberflächen nennen die Autoren zwei Hauptstrategien für deren Einsatz: Beim „Graft-to-Surface“-Verfahren bindet das Material aus der Lösung, während bei „Graft-from-Surface“ Polymerbürsten direkt auf der Oberfläche wachsen. Die erste Variante ist technisch einfacher umzusetzen, während die zweite trotz aufwendigerer Chemie und Substratvorbereitung eine höhere Packungsdichte ermöglicht.
In der Praxis ist dieser Unterschied relevant. Sollen Proteine auf einem einfachen Substrat nur schnell gebremst werden, reicht oft die einfachere Variante. Sollen die Proteine jedoch dauerhaft nicht eindringen, reicht es nicht, die Moleküle lediglich aufzukleben. Die Autoren betonen, dass die gewählte Methode Packungsdichte, Defektzahl und Haltbarkeit der Oberfläche bestimmt. Deshalb zählt nicht nur die angegebene chemische Zusammensetzung einer Beschichtung, sondern vor allem, ob sie unter Betriebsbedingungen eine homogene und stabile Grenzfläche bildet.
Der dritte Weg nutzt Muster, Texturen und Topografien. Hier geht es nicht um eine veränderte Chemie, sondern darum, die Geometrie zu steuern, die Zelle oder Protein wahrnimmt. Die Quelle macht deutlich, dass die Oberflächentopografie Zelladhäsion, Proliferation, Migration, Differenzierung und Genexpression beeinflusst. Sie reagieren sowohl auf Mikro- als auch auf Nanostrukturen und nicht allein auf die bloße Anwesenheit des Materials. In den im Buch zitierten Studien veränderten unterschiedliche Höhen, Größen und Abstände topografischer Strukturen den Grad der Mineralisierung, die Zellorientierung, die Zelladhäsion und die Differenzierung. Textur ist damit kein bloßes Beiwerk der Verarbeitung, sondern ein aktives Werkzeug zur Steuerung biologischer Reaktionen.
Besonders deutlich wird das bei Knochen- und Zahnimplantaten. Eine gut abgestimmte raue oder dreidimensionale Schicht kann die frühe Heilung beschleunigen, die Fibrinablagerung, die Integrinbindung und die mikromechanische Verankerung am Knochen fördern. Dadurch steigt die Scherfestigkeit an der Implantat-Knochen-Grenzfläche, und die Lastübertragung verbessert sich. Dies ist ein gutes Beispiel dafür, dass Texturierung keine „blinde Verbesserung“ ist, sondern der Versuch, einen spezifischen Grenzflächenmechanismus zu steuern. Gleichzeitig gilt es, vorsichtig zu sein, denn dieselbe Rauheit, die die Osseointegration fördert, kann in einem anderen Einsatzgebiet das Risiko einer bakteriellen Besiedlung erhöhen oder die Oberflächenkontrolle erschweren.

Häufige Fehler, Fallstricke und falsche Fährten
Viele verwechseln „besseres Material“ automatisch mit einer „besseren biologischen Reaktion“. Das ist zu vereinfachend. Festigkeit, Ermüdungsbeständigkeit und chemische Stabilität sagen allein noch nichts darüber aus, was an der Gewebegrenzfläche passiert. Ein hervorragendes Strukturmaterial kann trotzdem eine schlechte biologische Grenzfläche besitzen. Genauso kann eine biologisch sehr aktive Oberfläche auf einem Substrat sitzen, das die nötigen mechanischen Eigenschaften nicht erfüllt. Genau darum ist die Vorstellung hilfreich, dass das Material dem Implantat Festigkeit verleiht, während die Oberfläche die Reaktion des Körpers bestimmt. Sie zwingt uns, zwei Fragen zu trennen, die die klassische Technik gern in einen Topf wirft.
Ebenso trügerisch ist die Vorstellung, eine einzelne Oberflächeneigenschaft könne das Problem im Alleingang lösen. In der Praxis gibt es keine universelle „Biokompatibilitäts-Einstellung“. Mehr Hydrophilie mindert zwar die Adsorption bestimmter Proteine, fördert aber nicht automatisch die Gewebeintegration. Mehr Rauheit regt zwar die Osteoblasten an, ist in einer infektionsgefährdeten Umgebung aber nicht unbedingt vorteilhaft. Das Buch selbst stellt fest, dass noch nicht bekannt ist, welcher Parameter für jede spezifische biologische Reaktion am wichtigsten ist, sodass Variablen unabhängig voneinander gemessen und korreliert werden müssen. Dies ist eine sehr wichtige methodische Richtlinie: Anstatt nach einer einzigen magischen Zahl zu suchen, muss eine Karte der Beziehungen zwischen verschiedenen Oberflächeneigenschaften und einem spezifischen klinischen Ziel erstellt werden.
Eine weitere Herausforderung ist die Dicke der Modifikation. Die Autoren des Kapitels über physikalisch-chemische Modifikationen betonen, dass diese so dünn wie möglich sein sollten. Idealerweise genügen schon die äußersten Molekülschichten, also wenige Nanometer. In der Praxis müssen die Schichten jedoch manchmal dicker sein, um Gleichmäßigkeit und Haltbarkeit zu sichern. Eine zu dicke Beschichtung kann die mechanischen und funktionellen Eigenschaften des Produkts verändern und das Risiko von Rissen und Ablösung erhöhen. Das gilt besonders, wenn das Implantat Ermüdung oder Reibung ausgesetzt ist. Eine biologisch vielversprechende Schicht, die sich mit der Zeit mechanisch ablöst, schafft kein Problem, sondern nur ein neues.
Ein weiterer Irrtum liegt darin, die Oberfläche als starren Zustand zu betrachten. Manche Materialien kehren ihre Oberflächenorganisation beim Übergang von Luft zu Wasser sogar um, wie die Quelle zeigt. Was unter trockenen Bedingungen vermessen wird, ist daher nicht unbedingt dieselbe Oberfläche, mit der Proteine und Zellen im Körper tatsächlich in Kontakt kommen. Dies hat direkte Auswirkungen auf die Forschung. Wenn die Oberflächenanalyse die Betriebsumgebung nicht berücksichtigt, könnte man einen Parameter optimieren, der nach der Implantation nicht mehr denselben Wert oder dieselbe Bedeutung hat.
Wenn eine fortgeschrittenere Theorie erforderlich ist
Sind Begriffe wie „glatt“, „hydrophil“ oder „rau“ nicht mehr ausreichend, braucht es einen fortgeschrittenen Ansatz. Ein Beispiel dafür sind anhaftungsfreie Oberflächen. Sie wirken nicht nur glatt, sondern bilden eine stabile Hydratationsschicht. Diese Schicht zu entfernen, ist für adsorbierende Proteine energetisch ungünstig. Wie das Buch zeigt, greifen PEG-basierte hydrophile Materialien auf Wasserstoffbrückenbindungen zurück, zwitterionische Systeme hingegen nutzen elektrostatisch induzierte Hydratation und können dadurch noch stärker Wasser binden. Auf dieser Ebene müssen neben der funktionellen Chemie auch Kettenpackungsdichte, Konformationsfreiheit und die Stabilität der Verankerung berücksichtigt werden.
Noch komplexer wird es, wenn die Oberfläche nicht nur störungsfrei bleiben, sondern auch das Zellverhalten aktiv steuern soll. In solchen Fällen kommt es auf die Geometrie im Mikro- und Nanobereich, die lokale Mechanik, die Größe, Höhe und den Abstand topografischer Merkmale sowie manchmal sogar auf die Ordnungs- oder Unordnungsstruktur des Musters an. Deshalb setzen Forschende inzwischen auf topografische Matrizen und systematische Oberflächenscreenings. Denn Zellen unterscheiden sich in ihren Reaktionen auf unterschiedliche Skalen und Muster, sodass die biologische Antwort längst nicht mehr als lineare Abhängigkeit von nur einem Parameter gilt.
Warum ist die Oberfläche eines Implantats so wichtig? – Zusammenfassung
Bei Biomaterialien entscheidet oft nicht das Material selbst über den Erfolg eines Implantats, sondern seine Oberfläche. Sie ist der erste Kontaktpunkt für Proteine, Zellen und Körperflüssigkeiten und beeinflusst dadurch maßgeblich die Biokompatibilität. Deshalb trennt ein durchdachtes Implantatdesign beide Aufgaben: Das Volumen sorgt für Festigkeit und Haltbarkeit, während die Oberfläche die gewünschte biologische Reaktion auslöst. Darauf beruht die gezielte Modifizierung der Oberfläche, ohne das Grundmaterial zu verändern. Deshalb kann man die vorhandene Oberfläche umgestalten, eine neue Beschichtung auftragen oder eine definierte Topografie entwerfen, die die Proteinadsorption, das Zellverhalten, die Gewebeintegration oder die Widerstandsfähigkeit gegen Bewuchs beeinflusst. Dabei gilt eine Grundbedingung: Dabei muss die Modifikation grenzflächennah, dünn, langlebig und exakt auf das klinische Ziel abgestimmt sein. Deshalb ist die Oberfläche bei Biomaterialien kein bloßes Detail der Endbearbeitung, sondern eines der wichtigsten Werkzeuge im Implantatdesign.