Miksi implantin pinta on niin tärkeä?
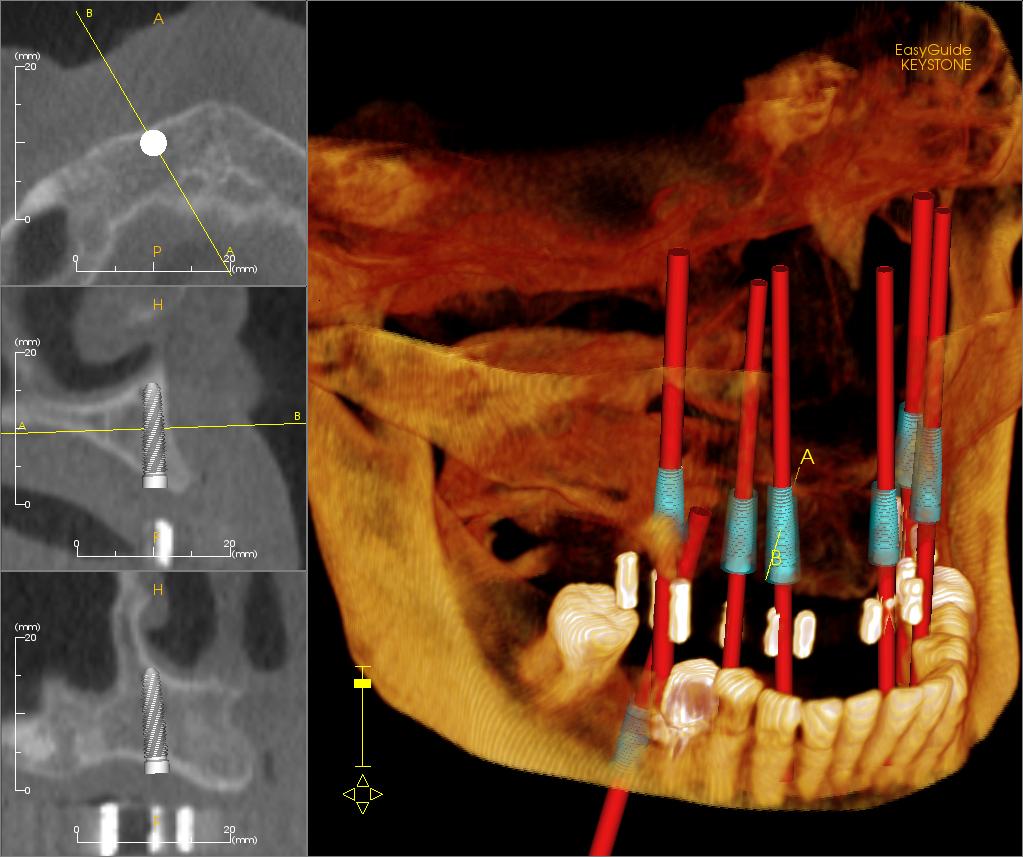
Biomateriaalitekniikassa on helppo turvautua perinteisestä materiaalitieteestä johdettuun intuitioon: koska implantin on kestettävä kuormituksia, sen ei saa ruostua, sen ei saa kulua liikaa ja sen on toimittava vuosien ajan, sen onnistumisen pitäisi riippua ensisijaisesti materiaalin ”sisäosasta”. Tämä on kuitenkin vain osa totuutta. Materiaalin ydin on todellakin vastuussa lujuudesta, jäykkyydestä, joustavuudesta, kestävyydestä ja läpäisevyydestä. Kehon näkökulmasta ensimmäinen ja tärkein kosketus ei kuitenkaan tapahdu koko materiaalilohkon kanssa, vaan sen ulkokerroksen kanssa. Juuri tämä kerros joutuu kosketuksiin veren, proteiinien, solujen ja kehon nesteiden kanssa. Käytännössä tämä tarkoittaa, että implantti voi olla mekaanisesti erittäin hyvä, mutta biologisesti ongelmallinen, jos sen pinta lähettää kudoksille ”väärän signaalin”.
Tämä havainto muuttaa tapaamme ajatella implanttien suunnittelua. Sen sijaan, että kysyisimme vain ”mistä implantti tulisi valmistaa?”, meidän on pohdittava, millainen implantin pinnan tulisi olla. Biomateriaaleissa biologinen vaste ei ole pelkkä koko komponentin kemiallisen koostumuksen heijastuma. Se on pikemminkin vaste sille, mitä tapahtuu materiaalin ja kudoksen rajapinnalla: pinnan kemialliset ominaisuudet, kostuvuus, varaus, karheus, rakenne ja reaktiivisuus. Tämän vuoksi implantin onnistuminen määräytyy niin usein ei materiaalin tilavuuden, vaan juuri faasirajan perusteella.
Tämä artikkeli perustuu teokseen Biomaterials Science: An Introduction to Materials in Medicine, toim. William R. Wagner et al., 4. painos, 2020. Seuraava sisältö on vain yleiskatsaus aiheeseen. Aiheesta kiinnostuneille suosittelemme perehtymistä kirjallisuuteen.
Miten keho reagoi materiaalin pintaan?
Tärkein lähtökohta on yksinkertainen: keho ei ”näe” koko implanttia kerralla. Ensin se ”lukee” sen pintaa. Biomaterials Science -kirjan kirjoittajat toteavat nimenomaisesti, että materiaalien osalta, jotka eivät vapauta haitallisia aineita, tiedon siirto materiaalista proteiineihin, soluihin ja koko kehoon tapahtuu pintarakenteen kautta. Keho reagoi siis ulkokerroksen erityiseen kemialliseen koostumukseen ja rakenteeseen pikemminkin kuin koko materiaalin keskimääräisiin ominaisuuksiin. Tällä näennäisesti vähäisellä painopisteen siirtymällä on valtava käytännön merkitys, sillä se siirtää biokompatibiliteettikysymyksen tasolta ”millainen seos tai polymeeri meillä on” tasolle ”miltä sen rajapinta näyttää ja miten se käyttäytyy”.
On tärkeää muistaa, että pinta ei ole pelkästään materiaalin ohut pää, joka käyttäytyy samalla tavalla kuin sen sisäosa. Kirjassa korostetaan, että pinta on erityisen reaktiivinen alue, joka eroaa lähes väistämättä materiaalin sisäosasta. Todellisessa metallimateriaalissa ulkokerros voi sisältää paitsi metallioksidia myös adsorboitunutta vettä, polaarisia orgaanisia yhdisteitä ja hiilivetypitoisia epäpuhtauksia. Polymeereissä tämä ainutlaatuinen pintavyöhyke voi olla noin 10–100 nm:n paksuinen. Tämä on tärkeää, koska se tarkoittaa, että vaikka materiaalin sisus olisi homogeeninen, sen biologisesti aktiivinen osa voi olla kemiallisesti ja rakenteellisesti monimutkainen.
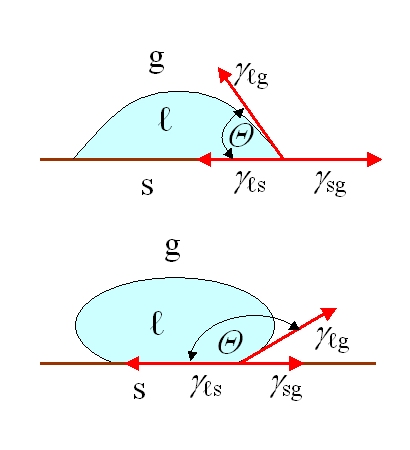
Biologisesta näkökulmasta pinta ei ole pelkästään kemiallisen koostumuksen kysymys. Kirjoittajat luettelevat monia ominaisuuksia, jotka voivat vaikuttaa biologisiin reaktioihin: karheus, kuviot ja topografia, kostuvuus, pinnan liikkuvuus, kemiallinen koostumus, sähkövaraus, kiteisyys, kimmomoduuli ja heterogeenisyys. Samalla he toteavat rehellisesti, että ei ole vielä mahdollista tunnistaa yhtä ainoaa yleispätevää ominaisuutta, joka olisi tärkein jokaiselle biologiselle reaktiolle. Käytännössä tämä on hyvin tekniikkakeskeinen oppitunti; suunnittelua ei pidä perustaa yhteen ainoaan parametriseen iskulauseeseen, kuten ”lisätään karheutta” tai ”tehdään pinnasta hydrofiilisempi”, koska kehon reaktio on useiden ominaisuuksien samanaikaisen vuorovaikutuksen tulos.
Tämä lähestymistapa selittää, miksi kaksi samasta perusmateriaalista valmistettua implanttia voi käyttäytyä biologisesti eri tavalla. Muutos käsittelyssä, sterilisoinnissa, varastoinnissa tai pakkaamisessa riittää muuttamaan pinnan tilaa. Kirja korostaa jopa niin arkisia asioita kuin sormenjäljet, pakkauksesta siirtyvät lisäaineet tai paperista tai kalvosta peräisin olevat epäpuhtaudet. Laboratoriossa tämä on yksityiskohta, mutta todellisuudessa juuri tällaiset yksityiskohdat voivat johtaa siihen, että testaamme pintaa, joka ei ole sama kuin kliinisesti käytetyssä implantissa.

Miten pinta vaikuttaa biologiseen yhteensopivuuteen
Jos pinta on implantin ja kehon välisen viestinnän ensisijainen kieli, meidän on kysyttävä, miltä tämä vuoropuhelu näyttää. Yksi keskeisistä mekanismeista on proteiinien adsorptio. Lähde korostaa, että synteettisen biomateriaalin implantoinnin jälkeen adheesiiviset proteiinit adsorboituvat sen pinnalle hyvin nopeasti, sekunneissa. Tällä tavalla materiaali, josta itsessään puuttuvat biologiset tunnistusmotiivit, muuttuu kehon kannalta ”luettavaksi”. Toisin sanoen solut eivät useinkaan reagoi suoraan puhtaaseen materiaaliin, vaan proteiinikerrokseen, joka muodostuu sen pinnalle pian kehon kanssa kosketukseen jouduttuaan.
Tällä on perustavanlaatuinen merkitys biokompatibiliteetin ymmärtämiselle. Biokompatibiliteetti ei tarkoita pelkästään akuutin toksisuuden puuttumista. Se merkitsee materiaalin kykyä saada aikaan sopiva isäntävaste tietyssä sovelluksessa. Tämä ”sopiva vaste” voi tarkoittaa yhtä asiaa stentille, toista ortopediselle implantille ja vielä toista katetrille. Kussakin näistä tapauksista pinta ohjaa alkuperäisiä biologisia tapahtumia: mitkä proteiinit adsorboituvat, missä konfiguraatiossa, mitkä solureseptorit stimuloituvat ja eteneekö signaali kohti kudoksen integroitumista, verihiutaleiden aktivaatiota, biofilmin muodostumista vai vierasesinereaktiota.
Hyvä esimerkki on adheesioproteiinien ja passivointiproteiinien vertailu. Kirjassa kuvataan, kuinka pinnan esipinnoittaminen fibronektiinillä lisää monien solujen adheesiota, kun taas albumiini voi rajoittaa sitä. Tämä ei ole vain soluviljelyn kuriositeetti, vaan malli siitä, mitä implantteissa tapahtuu. Pinta ei ole neutraali tausta. Se asettaa lähtöolosuhteet myöhemmälle soluvasteelle. Käytännössä tämä tarkoittaa, että kaksi mekaanisesti yhtä lujaa pintaa voi johtaa täysin erilaisiin paranemiskulkuun yksinkertaisesti siksi, että ne muodostavat adsorboituneiden proteiinien ensimmäisen kerroksen eri tavalla.
Yhtä tärkeitä ovat pinnan ja mikro-organismien väliset vuorovaikutukset. Biofilmejä käsittelevässä luvussa kirjoittajat huomauttavat, että kostuvuus, varaus, karheus ja topografia vaikuttavat bakteerien adheesioon. Yleinen suuntaus on, että suurempi karheus edistää usein bakteerien tarttumista ja hydrofobiset pinnat helpottavat useammin bakteerien kiinnittymistä. Samalla tämä ei ole sääntö ilman poikkeuksia, sillä erittäin superhydrofiiliset tai superhydrofobiset järjestelmät voivat toimia biofilmin estäjinä eri mekanismin kautta. Käytännössä tämä toimii varoituksena: kudosintegraatiolle hyödyllinen ratkaisu ei aina ole yhtä hyödyllinen bakteerien kolonisaation hallitsemiseksi.
Alla on englanninkielinen video nimeltä BIOE 5820 Biomaterials Protein Adsorption, joka on luento proteiinin adsorptiosta biomateriaalipinnoille.
Miksi muokata pintaa eikä koko materiaalia
Tämä on pintamuokkauksen pääasiallinen perustelu. Jos materiaalin ydin on vastuussa kantokyvystä, kestävyydestä ja mekaanisesta toiminnasta, kun taas pinta on vastuussa biologisesta vuorovaikutuksesta, on järkevintä säilyttää se, mikä toimii hyvin ytimessä, ja muokata vain sitä, mikä tulee kosketuksiin kudoksen kanssa. Juuri näin fysikaalis-kemiallisia pintamuokkauksia käsittelevän luvun kirjoittajat asian muotoilevat: tavoitteena on säilyttää biomateriaalin keskeiset fysikaaliset ominaisuudet ja muuttaa vain ulkokerrosta kudos-laite-rajapinnan biologisen vasteen parantamiseksi tai säätelemiseksi.
Tällä lähestymistavalla on useita hyvin käytännöllisiä etuja. Ensinnäkin ei tarvitse luopua materiaalista, jonka mekaaniset ja teknologiset ominaisuudet tunnetaan hyvin. Titaani, teräs, teknilliset polymeerit tai elastomeerit voivat edelleen täyttää rakenteellisen tai toiminnallisen roolinsa. Toiseksi biologinen vaste voidaan räätälöidä tarkemmin tiettyä sovellusta varten. Haluamme erilaisen pinnan luuimplantille, toisen veriin kosketuksissa olevalle komponentille ja vielä toisen katetrille, jossa prioriteettina voi olla proteiinien adsorptio sekä solujen tai bakteerien tarttumisen rajoittaminen. Kolmanneksi pinnan muokkaus mahdollistaa laitteen parantamisen ilman, että koko rakennetta tarvitsee suunnitella kokonaan uudelleen. Kirjassa jopa korostetaan, että jo kliinisessä käytössä vakiintuneiden laitteiden kohdalla tämä on tapa muuttaa biologisia vuorovaikutuksia ilman, että tuotetta tarvitsee suunnitella uudelleen, tuotantoa uudistaa tai lääkintähenkilökuntaa kouluttaa uuden ratkaisun käyttöön.
On kuitenkin yksi ehto: on erotettava toisistaan rajapinnan todellinen muokkaus ja kuvauksen kosmeettinen muutos. Pelkkä väite, että materiaali on ”bioaktiivinen” tai ”antifouling”, ei merkitse paljoakaan, jos ei tiedetä, miltä pinta todellisuudessa näyttää lopullisessa muodossaan käsittelyn ja sterilisoinnin jälkeen. Lähde huomauttaa, että analysoitavan näytteen tulisi vastata mahdollisimman tarkasti materiaalia tai laitetta siinä muodossa, jossa sitä käytetään biologisissa testeissä tai implantaatioissa. Tämä on tärkeää, koska ilmalle altistuva pinta ei välttämättä ole sama pinta, jonka materiaali esittää kehon vesiympäristössä.
Kolme päämenetelmää pinnan muokkaamiseen
Ensimmäisessä menetelmässä muutetaan olemassa olevaa pintaa lisäämättä erillistä, uutta kerrosta. Materiaalin ulkokerroksessa jo olevia atomeja, molekyylejä ja sidoksia voidaan muuttaa kemiallisesti tai fysikaalisesti. Tähän ryhmään kuuluvat muun muassa etsaus, kemiallinen aktivointi, mekaaninen karhennus, ioni-istutus ja tietyt laserhoidot. Tärkeää on, että emme ”kiinnitä” uutta kerrosta implanttiin, vaan muokkaamme sen omaa pintaa. Tämä on edullista silloin, kun modifikaation vahva integroituminen substraattiin on tärkeää, sekä delaminaation riskin vähentämiseksi ja ominaisuuksien, kuten reaktiivisuuden, kostuvuuden, korroosionkestävyyden, kovuuden tai bioaktiivisuuden, muuttamiseksi. Lähde osoittaa esimerkiksi, että ioni-istutus voi parantaa kulutuskestävyyttä tai korroosionkestävyyttä, ja laserprosessointi voi hallitusti muuttaa pinnan karheutta, kiteisyyttä ja kemiaa.
Toinen lähestymistapa käsittää uuden kerroksen tai pinnoitteen levittämisen. Tässä tapauksessa olemassa olevalle pinnalle sijoitetaan materiaali, jolla on erilainen koostumus tai ominaisuudet. Tämä voi olla ohut kalvo, siirrostettu kerros, polymeeripinnoite tai järjestelmä, joka on suunniteltu likaantumattomaksi pinnaksi. Tämä strategia on erityisen arvokas, kun substraatilla on ihanteelliset mekaaniset ominaisuudet, mutta se on biologisesta näkökulmasta liian ”raaka”. Hyvä esimerkki ovat pinnat, jotka vastustavat epäspesifistä proteiinin adsorptiota. Niiden mekanismi perustuu yleensä vahvaan hydraatiokerrokseen, joka toimii proteiineille energisenä ja fyysisenä esteenä. Luvussa likoittumattomista pinnoista kirjoittajat kuvaavat kahta päästrategiaa tällaisten järjestelmien soveltamiseksi: ”graft-to-surface”, jossa materiaali adsorboituu tai sitoutuu liuoksesta, ja ”graft-from-surface”, jossa polymeeriharjat kasvavat pinnalta. Ensimmäinen lähestymistapa on teknisesti yksinkertaisempi; jälkimmäisellä saavutetaan helpommin suuri pakkaustiheys, mutta se vaatii yleensä monimutkaisempaa kemiaa ja substraatin valmistelua.
Käytännössä tällä erolla on teknistä merkitystä. Jos halutaan vain nopeasti rajoittaa proteiinien kertymistä suhteellisen yksinkertaiselle substraatille, yksinkertaisempi ratkaisu voi riittää. Jos kuitenkin tarvitaan kestävä, läpäisemätön ja tiheästi pakattu adsorptiota estävä kerros, pelkkä molekyylien ”kiinnittäminen” pintaan ei välttämättä riitä. Kirjassa korostetaan selvästi, että menetelmän valinta määrää pakkaustiheyden, vikojen määrän ja lopullisen pinnan kestävyyden. Tämä tarkoittaa, että pinnoitteita ei arvioida pelkästään niiden ilmoitetun kemian perusteella, vaan sen perusteella, muodostavatko ne todellisuudessa homogeenisen, vakaan rajapinnan käyttöolosuhteissa.
Kolmas lähestymistapa liittyy kuvioiden, tekstuurien ja topografioiden luomiseen. Tässä pääpaino ei ole kemiallisen koostumuksen muuttamisessa, vaan sen geometrian muuttamisessa, mitä solu tai proteiini ”näkee”. Lähde korostaa, että pinnan topografia vaikuttaa solujen adheesioon, proliferaatioon, migraatioon, erilaistumiseen ja geenien ilmentymiseen. Solut reagoivat sekä mikro- että nanomittakaavan piirteisiin, eivät pelkästään materiaalin läsnäoloon. Kirjassa mainituissa tutkimuksissa topografisten rakenteiden vaihtelevat korkeudet, koot ja välit muuttivat mineralisaation astetta, solujen suuntautumista, solujen adheesiota ja erilaistumista. Tämä tarkoittaa, että tekstuuri ei ole pelkkä koriste tai prosessoinnin sivuvaikutus, vaan aktiivinen työkalu biologisten reaktioiden hallitsemiseksi.
Tämä on erityisen ilmeistä luu- ja hammasimplanttien kohdalla. Kirjassa kuvataan, kuinka sopivan karhea tai kolmiulotteinen pintakerros voi nopeuttaa paranemisen alkuvaiheita, edistää fibriinin kertymistä, integriinien sitoutumista ja mikromekaanista lukittumista luuhun. Tämän seurauksena implantin ja luun rajapinnan leikkauslujuus kasvaa ja kuormituksen siirto paranee. Tämä on hyvä esimerkki siitä, kuinka teksturointi ei ole ”sokeaa parannusta”, vaan yritys hallita tiettyä rajapintamekanismia. Varovaisuutta on kuitenkin noudatettava, sillä sama karheus, joka auttaa luuintegraatiota, voi toisessa sovelluksessa lisätä bakteerien kolonisaation riskiä tai haitata pinnan hallintaa.

Yleisiä virheitä, sudenkuoppia ja vääriä johtolankoja
Yleisin virhe on rinnastaa ”parempi materiaali” ”parempaan biologiseen reaktioon”. Se on liian yksinkertaistettua. Lujuus, väsymiskestävyys ja kemiallinen stabiilius eivät vielä selitä, mitä kudosrajapinnalla tapahtuu. Biomateriaaleissa voi olla erinomainen rakennemateriaali ja huono biologinen rajapinta. Voi myös kohdata päinvastaisen ongelman: biologisesti erittäin aktiivinen pinta, joka on kiinnitetty substraattiin, joka ei täytä mekaanisia vaatimuksia. Juuri tästä syystä lähtökohta, että materiaali antaa implantille lujuuden, kun taas pinta määrää kehon reaktion, on hyödyllinen suunnittelussa. Se pakottaa meidät erottamaan kaksi kysymystä, jotka klassisessa insinööritieteessä usein niputetaan yhteen.
Toinen sudenkuoppa on uskomus, että yksi ainoa pinnan ominaisuus ratkaisee koko ongelman. Käytännössä ei ole olemassa yleistä ”biokompatibiliteettiasetusta”. Hydrofiilisyyden lisääminen voi rajoittaa tiettyjen proteiinien adsorptiota, mutta se ei välttämättä paranna kudoksen integroitumista. Karheuden lisääminen voi edistää osteoblastien reaktiota, mutta se ei välttämättä ole hyödyllistä ympäristössä, jossa on infektioriski. Kirjassa itsessään todetaan, että ei vielä tiedetä, mikä parametri on tärkein kunkin biologisen reaktion kannalta, joten muuttujat on mitattava ja korreloitava itsenäisesti. Tämä on erittäin tärkeä metodologinen ohje: yhden maagisen luvun etsimisen sijaan on luotava kartta useiden rajapintaominaisuuksien ja tietyn kliinisen tavoitteen välisistä suhteista.
Kolmas sudenkuoppa koskee modifikaation paksuutta. Fysikaalis-kemiallisia modifikaatioita käsittelevän luvun kirjoittajat korostavat, että modifikaatioiden tulisi olla mahdollisimman ohuita. Ihannetapauksessa riittää, että muutetaan vain muutama uloimpia molekyylikerroksia – suuruusluokkaa muutama nanometri –, vaikka käytännössä kerrosten on joskus oltava paksumpia yhtenäisyyden ja kestävyyden varmistamiseksi. Liian paksu pinnoite voi muuttaa laitteen mekaanisia ja toiminnallisia ominaisuuksia sekä lisätä halkeilun ja delaminaation riskiä. Tämä on erityisen tärkeää, jos implantti altistuu väsymiselle tai kitkalle. Kerros, joka näyttää lupaavalta biologisesta näkökulmasta mutta irtoaa mekaanisesti jonkin ajan kuluttua, ei ratkaise ongelmaa, vaan luo vain uuden.
Neljäs väärinkäsitys on pinnan käsittely staattisena tilana. Lähde osoittaa, että jotkut materiaalit voivat muuttaa pintarakenteensa siirtyessään ilmasta vesiympäristöön. ”Kuivissa olosuhteissa” mitattu pinta ei välttämättä ole sama pinta, jonka proteiinit ja solut kohtaavat kehossa. Tällä on suoria vaikutuksia tutkimukseen. Jos pinnan analyysissä ei oteta huomioon käyttöympäristöä, saatetaan optimoida parametri, jolla ei ole enää samaa arvoa tai merkitystä implantoinnin jälkeen.
Kun tarvitaan edistyneempää teoriaa
Edistyneempi lähestymistapa tulee tarpeelliseksi, kun intuitiiviset termit kuten ”sileämpi”, ”hydrofiilisempi” tai ”karheampi” eivät enää riitä. Esimerkkinä ovat likaantumattomat pinnat. Niiden toiminta ei johdu pelkästään siitä, että ne ovat liukkaita, vaan siitä, että ne muodostavat stabiilin hydraatiokerroksen, jonka poistaminen on energian kannalta epäedullista proteiineille. Kirja osoittaa, että PEG-pohjaiset hydrofiiliset materiaalit sitovat vettä vetysidosten kautta, kun taas zwitterioniset materiaalit voivat tehdä niin vielä voimakkaammin sähköstaattisesti indusoidun hydraation kautta. Tällä tasolla on otettava huomioon paitsi funktionaalinen kemia myös ketjujen pakkautumistiheys, konformaatiovapaus ja kerroksen kiinnittymisen stabiilius.
Kehittynyttä teoriaa tarvitaan myös silloin, kun pinnan ei ole tarkoitus olla vain häiritsemätön, vaan aktiivisesti ohjata solujen käyttäytymistä. Tällaisissa tapauksissa merkitystä on mikro- ja nanomittakaavan geometrialla, paikallisella mekaniikalla, topografisten piirteiden koolla, korkeudella ja välillä, ja joskus jopa kuvion järjestyneisyydellä tai epäjärjestyneisyydellä. Juuri tämän vuoksi nykypäivän tutkimuksessa käytetään topografisia matriiseja ja systemaattisempia pintaseulontoja. Kyse ei ole aiheen akateemisesta monimutkaisuudesta, vaan siitä, että solut todella erottavat ominaisuuksien mittakaavat ja kuviot toisistaan, eikä biologinen vaste ole enää yhden parametrin lineaarinen funktio.
Miksi implantin pinta on niin tärkeä? – yhteenveto
Biomateriaaleissa implantin onnistuminen ei useinkaan riipu itse materiaalista, vaan pinnasta, jonka se esittää keholle. Pinta on ensimmäinen kosketuspiste proteiineihin, soluihin ja kehon nesteisiin, ja siten se määrää suurelta osin biologisen yhteensopivuuden. Tästä syystä järkevä implanttisuunnittelu edellyttää toimintojen erottamista: materiaalin tilavuuden tarkoituksena on varmistaa mekaaniset ominaisuudet ja kestävyys, kun taas pinnan tarkoituksena on saada aikaan sopiva biologinen vaste. Tämä on perustana koko logiikalle, jossa pintaa muokataan muuttamatta koko materiaalia. Voidaan muokata olemassa olevaa ulkokerrosta, levittää uusi pinnoite tai suunnitella kuvio ja topografia, jotka vaikuttavat proteiinien adsorptioon, solujen käyttäytymiseen, kudosten integroitumiseen tai likaantumisen kestävyyteen. On yksi ehto: muokkauksen on oltava aidosti rajapinnallinen, ohut, kestävä ja räätälöity tiettyä kliinistä tavoitetta varten. Juuri tästä syystä biomateriaaleissa pinta ei ole viimeistelyyksityiskohta, vaan yksi implanttisuunnittelun päätyökaluista.




