Biomedizinische Technik im Kontext der Materialwissenschaft
Inhaltsverzeichnis
Heute präsentiert sich die Biomedizinische Technik als ein umfassendes Wissensgebiet, in dem Materialwissenschaft, Strömungsmechanik, Transportphänomene, Messtechnik und Systemtechnik mit Physiologie sowie klinischer Praxis interdisziplinär interagieren. Die zweite Ausgabe des The Biomedical Engineering Handbook, herausgegeben von J.D. Bronzino, fasst diese Themen zusammen und zeigt, wie die Wahl des Materials und seiner Oberflächenbeschaffenheit durch die Konstruktion von Sensoren und Massenflusseigenschaften die Konstruktion künstlicher Organe und deren präzise Fertigung beeinflusst. Anhand von Beispielen aus den Bereichen Biomaterialien, biomedizinische Sensorik, Gewebetechnik sowie künstliche Organe ermöglicht dieser Artikel ein vertieftes Verständnis der dargestellten Perspektive. Darüber hinaus werden die Implikationen für Fertigungstechnologie und Qualitätskontrolle deutlich hervorgehoben.
In der Biomedizintechnik gibt es keine isolierten Entscheidungen – die Wahl der Materialklasse, der Oberflächentopographie und -chemie, der Strömungs- und Stoffübergangsbedingungen, der Gerätearchitektur und des Herstellungsprozesses bilden ein systemisches Ganzes, das für eine bestimmte klinische Indikation und ein bestimmtes biologisches Belastungsregime ausgelegt sein muss.
Der Stellenwert der Materialwissenschaft in der Biomedizintechnik
Enzyklopädisch gesehen ist ein Biomaterial ein Material, das für den direkten Kontakt mit Gewebe in einem medizinischen Gerät bestimmt ist und dazu dient, die Struktur oder Funktion des Körpers sicher und effektiv zu ersetzen. Im Abschnitt „Biomaterialien” wird ein umfassender Überblick über die Klassen und konstruktionsrelevanten Fragestellungen gegeben, wobei Metalle, Keramiken, Polymere, Verbundwerkstoffe, biologisch abbaubare Polymere sowie Materialien biologischen Ursprungs berücksichtigt werden; zudem werden Aspekte der Wartung und Fixierung von Endoprothesen erörtert. Allein schon der Aufbau der Kapitel führt von der Auswahl grundlegender Materialklassen zu Fragen der Integration mit Hart- und Weichgewebe, was die systemische Natur des Fachgebiets gut widerspiegelt.
Bei Metallen (Cr–Ni–Mo-Stähle, Co–Cr-Legierungen, Titanlegierungen) sind Korrosions- und Ermüdungsbeständigkeit sowie die Möglichkeit, die Mikrostruktur präzise zu formen, von entscheidender Bedeutung. Aus praktischer Sicht betont das Buch, dass die Geschichte der Verarbeitung – Schmelzen, plastische Verformung, Wärmebehandlung, Reinigung und sogar die abschließende Mikrobearbeitung – mit der Beständigkeit gegen Spalt- und Spannungskorrosion sowie Ermüdungsrisse zusammenhängt. Wichtig für die Präzisionsfertigung ist, dass das Kapitel über Metalle auch die „Herstellung von Implantaten” behandelt und damit die Untrennbarkeit von Materialdesign und Fertigungstechnologie in der Medizin bestätigt.
Keramiken (Aluminiumoxid, Zirkonoxid, Kohlenstoffe, Glaskeramiken, Calciumphosphatsysteme) bieten Härte, chemische Beständigkeit und – im Falle von bioaktiven Glaskeramiken – die Fähigkeit, chemisch vermittelte Bindungen mit Gewebe einzugehen. Die Monografie erinnert zugleich an die Zerbrechlichkeit sowie an die Verschleißmechanismen keramischer Werkstoffe und stellt biokeramische Fertigungstechniken für den Ersatz von Hartgewebe sowie für die Gewebeintegration vor. Geometrie, Porosität sowie Oberflächenqualität werden gezielt gestaltet, wobei eine strenge Kontrolle der für die Bruchfestigkeit kritischen Defekte sichergestellt wird.
Polymere sind das Schweizer Taschenmesser der Biomedizin. Das Spektrum umfasst PVC und PE, erstreckt sich über PMMA und PU und reicht bis zu biologisch abbaubaren Polyestersystemen. Allen gemein ist ein umfangreiches Arsenal an Oberflächenmodifikationen, durch die sich die Biokompatibilität gezielt steigern lässt. Von besonderer Bedeutung ist die Tatsache, dass diese Klasse die Kontrolle der Eigenschaften durch Molekulargewicht und -verteilung, chemische Struktur und Vernetzung sowie die Kombination der mechanischen Barrierefunktion mit bioaktiven chemischen Motiven ermöglicht. Die vorliegende Untersuchung beleuchtet zudem die Sterilisation sowie deren Konsequenzen für die Eigenschaften und Verfahren der chemischen Gradientenformung an Protein-Oberflächen-Grenzflächen, welche sich unmittelbar auf Hämokompatibilität und Zelladhäsion auswirken.
In Verbundwerkstoffen ist es dank ihrer Struktur (Partikel, Fasern, Porosität) möglich, widersprüchliche Anforderungen zu kombinieren: Anisotropie modulieren, den Modul an den Knochen anpassen, die Schwingungsdämpfung verbessern und allmähliche Übergänge in den Eigenschaften erreichen. Die Monografie ordnet diese Themen und diskutiert Eigenschaftsgrenzen, Porosität und Biokompatibilität. Aus produktionstechnischer Sicht wird die Kontrolle der Phasenverteilung und der Defekte an der Grenzfläche zwischen Matrix und Verstärkung ebenso wichtig wie das Material selbst.
Die Auswahl sowie die Qualifizierung eines Biomaterial lassen sich nicht von der eingesetzten Verarbeitungstechnologie sowie der vorgesehenen Belastungsmethode trennen. Dasselbe Material mit unterschiedlicher Mikrostruktur, Topografie und Oberflächenreinheit weist ein unterschiedliches Profil hinsichtlich Korrosion, Verschleiß, Proteinadsorption und Gewebeintegration auf. Daher ist es im Konstruktionsprozess notwendig, die Volumenmikrostruktur und die biophysikalisch-chemische Grenzfläche gleichzeitig zu kontrollieren.
Biomedizinische Sensoren und Material-Biologie-Grenzflächen
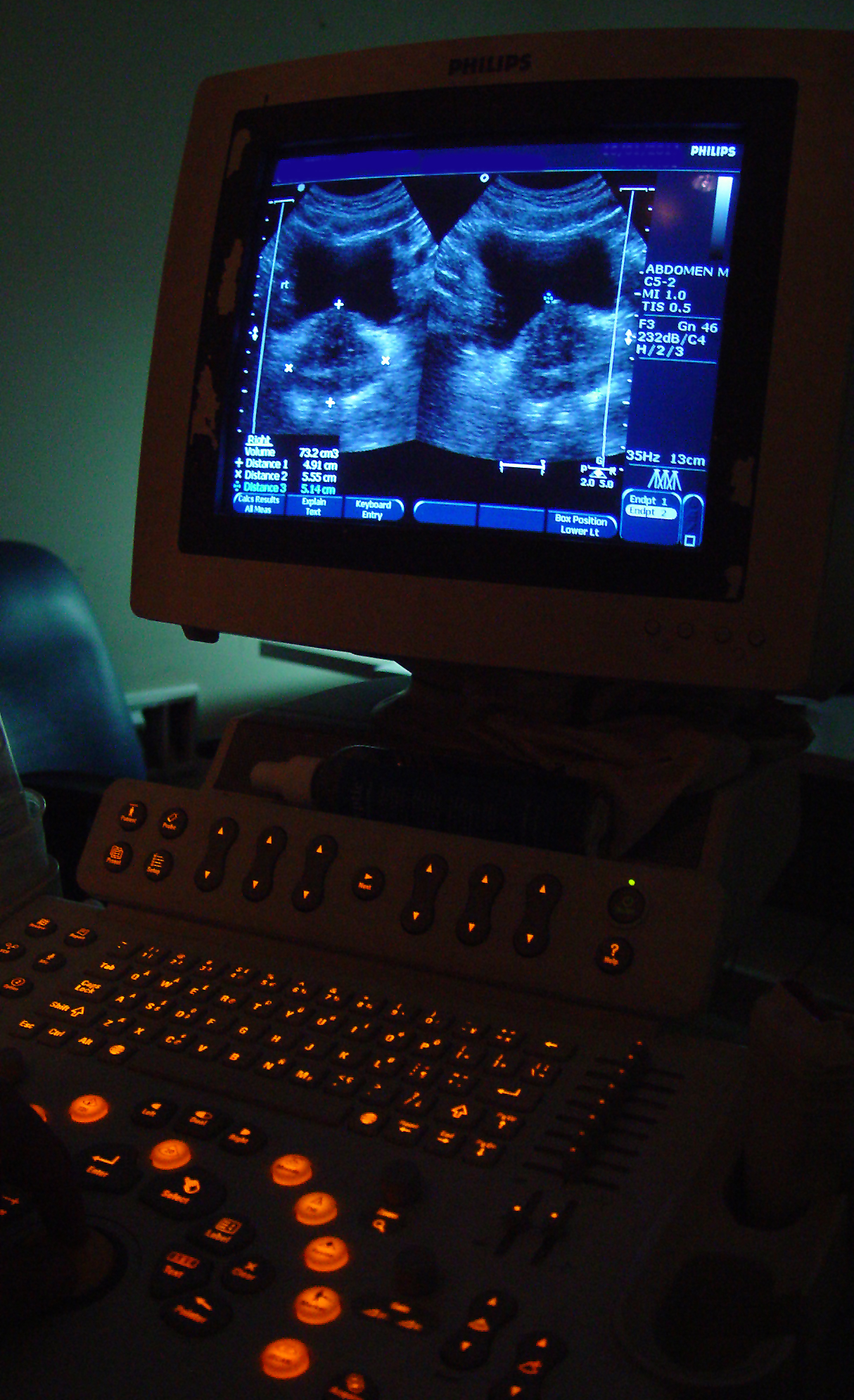
Biomedizinische Sensoren dienen als Schnittstelle zwischen dem biologischen System und dem elektronischen System und wandeln geometrische, mechanische, thermische, hydraulische oder chemische Größen in elektrische Signale um. Das Kompendium stellt zwei Klassifizierungen in den Vordergrund: physikalische Sensoren, welche beispielsweise Muskelverschiebungen, Blutdruck und Flüssigkeitsströmungen erfassen, und chemische Sensoren, die Verbindungen, Konzentrationen und Aktivitäten identifizieren, von elektrochemischen und photometrischen Verfahren bis hin zu komplexen Analysesystemen. Besonders hervorzuheben ist die Glasfasertechnik, die optische Sensoren sowohl für die Detektion als auch für die Übertragung zu einem äußerst vielseitigen Werkzeug macht.
In der Diagnostik und Therapie unverzichtbar, nehmen Biopotentialelektroden eine besondere Stellung ein. Nicht allein das elektronische System und die Geometrie bestimmen ihre Funktionsweise, sondern in erster Linie die Interaktion mit der biologischen Umgebung. Die Vielfalt der Anwendungen, die von Oberflächen-Ag/AgCl über EMG-Nadeln bis hin zu Dünnschicht-Mikroelektroden für die intrakardiale und zentrale Nervensystem-Aufzeichnung reicht, erfordert unterschiedliche Konfigurationen von Materialien, Beschichtungen und mechanischem Design sowie spezifische Qualifizierungsverfahren. Das Problem der Abstoßung und Fremdkörperreaktionen verringert die Signalstabilität und die Haltbarkeit der Schnittstelle, sodass es nicht nur um Elektronik, sondern auch um Chemie, Oberflächentopografie und Prozessreinheit geht.
Das Buch organisiert auch die Methoden zur Anwendung des Sensors am Patienten, die von berührungslosen Methoden über Hautkontakt bis hin zu minimalinvasiven Intrakörpersensoren und implantierbaren Sensoren reichen. Die spezifischen Anforderungen jeder Methode an Biokompatibilität, Signalstabilität sowie Desinfektions- und Sterilisationsstrategien bedingen direkte Konsequenzen für die Material- und Fertigungstechnologiewahl.
Das Design eines biomedizinischen Sensors kann mit dem einer Schnittstelle verglichen werden, wobei elektrische und mechanische Parameter, die Wahl des Kontaktmaterials, dessen Beschichtungen, die Oberflächenvorbereitung sowie die Befestigungsmethode gleichermaßen von Bedeutung sind, da sie die Bioreaktion und die Signalabweichung im Zeitverlauf beeinflussen.
Transportphänomene und mechanische Einschränkungen
Die Steuerung der Funktion von Geweben und Geräten durch den Transport von Masse, Energie und Impuls im Bereich von Mikrometern bis Zentimetern bildet die fundamentale Grundlage für das Gewebeengineering sowie das künstliche Organdesign. Die Herausgeber des Abschnitts „Gewebeengineering” heben zwei technische Themen hervor: die Eigenschaften und Entwicklung von Materialien auf zwei Längenskalen (molekular und zellulär) und die Analyse von Geschwindigkeitsprozessen. Auf der Oberflächenebene umfasst dies die Biomolekulartechnik (Immobilisierung von adhäsiven Liganden, Kontrolle der Motifdichte) sowie Proteinadsorptionsphänomene, die die weitere zelluläre Reaktion beeinflussen. Auf der Mesoskala sind Gerüste und Regenerationsvorlagen mit genau definierten Porengrößen, Permeabilitäten und Abbaugraden von entscheidender Bedeutung.
Tangentiale Spannungen infolge von Strömungen sowie die Diffusions- und Konvektionsraten von Nährstoffen, Sauerstoff und Metaboliten spielen darüber hinaus eine wesentliche Rolle. Die in separaten Kapiteln dargelegten Auswirkungen von Scherspannungen auf Zellen und der Beitrag des Massentransports zur Gewebefunktion verdeutlichen, dass sich die mechanische Umgebung sowie Konzentrationsgradienten auf Morphologie, Zytoskelett-Umstrukturierung, Signaltransduktion, Metabolitsekretion und Genregulation von Endothelzellen auswirken, und somit die Entwicklung, Stabilität sowie Funktion von Neugewebe prägen. Die Schlussfolgerung ist einfach: Ohne Kontrolle der Strömung und des Stoffaustauschs wird selbst das am besten ausgewählte Material nicht die erwartete Leistung erbringen.
In der Gewebe- und Organersatztechnik erweisen sich Strömungs- und Diffusionsparameter als ebenso fundamentale Gestaltungselemente wie Polymere oder Keramiken. Bioreaktoren, Porenstruktur sowie die Strömungseigenschaften des Produkts sind dabei als wesentliche Konstruktionsvariablen aufeinander abzustimmen.
Gewebeengineering
Die Definition des Gewebeengineering umfasst die Anwendung wissenschaftlicher Prinzipien auf Konstruktion, Aufbau, Modifikation, Wachstum sowie Erhaltung lebender Gewebe. Unter anderem sind, gemäß Bronzino et al., eine Zelllinie sowie eine Zellquelle zu selegieren, eine Matrix-Zell-Schnittstelle und eine Gewebeorganisationskontrolle zu konzipieren, und die Stoffversorgung sicherzustellen. Hier treffen Materialien auf Biologie: immobilisierte adhäsive Liganden, die Kontrolle der Proteinadsorption und die Mikroarchitektur des Gerüsts bestimmen die Adhäsion, Proliferation und Differenzierung.
In der Praxis besteht der Kern aus Gerüsten mit Strukturgrößen von 10 bis 100 µm, die den Transport, die Zellbesiedlung und die Richtung des Gewebewachstums bestimmen. Vor dem Hintergrund dieser Überlegungen erweist sich die Klasse der biologisch abbaubaren Polymere als von entscheidender Bedeutung. Das entsprechende Kapitel widmet sich aliphatischen Polyestern auf Glykolid- und Lactidbasis, stellt darüber hinaus alternative Familien vor und erläutert die Modellierung ihres Abbaus. Der Autor hebt zwei Vorteile hervor: das Verschwinden der chronischen Fremdkörperreaktion im Verlauf der Resorption und die Fähigkeit, als temporäre Gerüste für die Geweberegeneration zu dienen.
Kollagenmaterialien bieten als Systeme geweblichen Ursprungs eine biologisch vertraute extrazelluläre Matrixarchitektur. Die chemische Struktur sowie die physikalisch-chemischen Eigenschaften von Kollagen werden in diesem Abschnitt detailliert dargestellt, wobei zudem moderne Technologien zur Herstellung von Membranen, porösen Schäumen, Gelen und Verbundwerkstoffen erläutert werden. Abschließend werden die Konstruktionskriterien für resorbierbare Kollagenimplantate präzise konturiert, wobei Porosität, scheinbare Dichte, Hydrophilie, Permeabilität sowie In-vivo-Stabilität in den Vordergrund rücken. Diese Parameter, die auch Parameter des Herstellungsprozesses sind, darunter Trocknungsgeschwindigkeit, Gefriertrocknungsbedingungen, Vernetzungsmittel und Reagenzienreinheit, wirken sich direkt auf die biologischen Ergebnisse aus.
Geräte und Bioreaktoren werden an der Schnittstelle zwischen Material- und Strömungsmechanik entwickelt. Kapillarfaser- und Mikroträgersysteme gewährleisten, sofern Scherspannungen sowie Konzentrationsgradienten präzise kontrolliert werden, die Aufrechterhaltung des Stoffwechsels unter den für die Geweberekonstruktion erforderlichen Zelldichten. Im klinischen Maßstab gilt diese Logik ebenfalls, sobald das Gerüst in situ besiedelt wird. Das Schicksal des Implantats wird durch Perfusion, Diffusion sowie mechanische Limitierungen des Wirtsorganismus determiniert.
Künstliche Organe und Ersatzmedizin
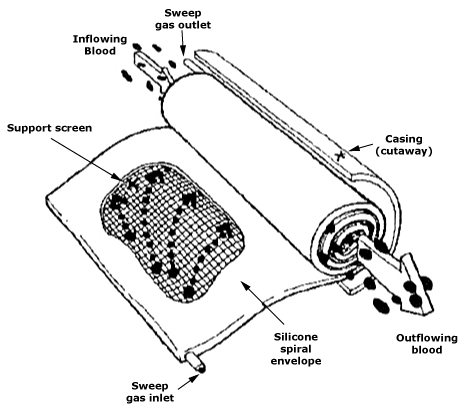
Der Abschnitt „Prothesen und künstliche Organe” zeigt, dass die Ersatzfunktion eines Organs überbrückend (z. B. extrakorporale Zirkulation), intermittierend und wiederholbar (Hämodialyse, CAPD) oder langfristig mit Implantation sein kann. Eingangs weisen die Autoren offen die Grenzen aus. In Anbetracht der Tatsache, dass Reibung, Verschleiß und Materialalterung in der warmen, feuchten sowie korrosiven Umgebung des Körpers zwangsläufig zu einer begrenzten Lebensdauer führen, vergleichbar mit jeder Maschine, ergibt sich für ein künstliches Organ eine entsprechende Restriktion. Das Nutzen-Kosten-Verhältnis hängt daher von der Kombination aus der erwarteten Lebensdauer des Geräts, der Art seiner Wartung/Ersetzung und der Prognose für den Zustand des Patienten ab. Dieser technische Realismus geht einher mit einer demografischen Tatsache: Millionen von Patienten leben dank Herzschrittmachern, Herzklappen, Dialyse oder Drainagesystemen.
Besonders aufschlussreich präsentiert sich das Beispiel einer künstlichen Niere, welche als Gerät den Massentransport verkörpert. Während einer Dialyse bestimmen die Membranen, die Permeabilitätskoeffizienten, die Clearances, die Strömungsbedingungen sowie die Pharmakokinetik und die Angemessenheit des Verfahrens in ihrer Gesamtheit die klinische Wirkung. Diese Variablen stehen in engem Zusammenhang mit der Materialwissenschaft, also Chemie und Membranarchitektur, der Strömungsmechanik, das heißt laminare beziehungsweise turbulente Strömung sowie Wandphänomene, und der Betriebssicherheit. Daher wurden die Hämodiafiltration, die Oberflächenmodifizierung und neue Membranpolymere intensiv weiterentwickelt.
Im Herz-Kreislauf-System besteht ein Konflikt zwischen den Anforderungen an die Hämokompatibilität und die mechanische Haltbarkeit. Das Ventildesign umfasst sowohl die hämodynamische Bewertung (Druckabfälle, Energieverluste, Rückflüsse und Stauzonen) als auch Fragen der Thrombusablagerung und zyklischen Haltbarkeit. Bei Gefäßtransplantaten werden Thrombosen und Neointimahyperplasie durch Modifikationen der Materialien und der Geometrie bekämpft, die sich auf die Scherspannungsverteilung und die Strömungseigenschaften auswirken. Jede Modifikation des Materials beziehungsweise der Oberflächentopographie geht über einen rein kosmetischen Effekt hinaus, da sie zwangsläufig in die Biologie der Thrombogenese sowie der Wundheilung eingreift.
Biohybride Organe repräsentieren eine Klasse von Geräten, welche lebende Elemente integrieren und Transplantationstechnologien mit synthetischen Strukturen verknüpfen, wodurch naturnahe Funktionen ermöglicht werden, während zugleich anspruchsvolle Anforderungen an Materialien und Verfahren formuliert werden. In diesem Bereich entwickeln sich Tissue Engineering und Massenersatzgeräte konsequent weiter, wobei sie sich einer immer funktionaleren und widerstandsfähigeren Schnittstellengeneration annähern.
Präzisionsfertigung und Qualitätskontrolle
Wie und woraus ein Produkt hergestellt wird, bestimmt seinen Endzustand. Bei Metallen bestimmen Verarbeitungsmethoden wie Walzen, Schmieden, Wärmebehandlung, Schneiden sowie Reinigen und Passivieren die Textur, Korngröße, Restspannungen und Oberflächenschichtzusammensetzung, die Ermüdung, Korrosion und Zelladhäsion steuern. Für Stahl, Co-Cr- und Ti-Legierungen behandelt die Monografie nicht nur die Eigenschaften, sondern auch die Besonderheiten der Implantatherstellung und schließt damit die Lücke zwischen Werkstofftechnik und Technologie. Dieser Übergang vom Datenblatt zum Prozessblatt ist in der Medizin von entscheidender Bedeutung.
Bei Keramiken wirken sich die Wahl der Synthese- und Sinterverfahren, die Kontrolle der Phasenanteile und Defekte sowie die Oberflächenbehandlung auf die Bruchfestigkeit und die bioaktiven Eigenschaften aus. Insbesondere bei glaskeramischen Biokeramiken und Hydroxylapatiten steht die präzise Kontrolle der Zusammensetzung, Kristallinität und Porosität in direktem Zusammenhang mit der Gewebeintegration und Druckfestigkeit. Dies sind Bereiche, in denen die Messung von Porosität, Topografie und Defekten Teil der klinischen Sicherheit wird.
Die Eigenschaften eines Polymers werden durch den Herstellungsprozess, die thermomechanische Geschichte, die Glühumgebung, die Sterilisationsmethode sowie die stabilisierenden Additive definiert, wobei sämtliche dieser Faktoren den Abbau und die Alterung maßgeblich beeinflussen. Die Monografie lenkt die Aufmerksamkeit auf zwei Bereiche: Oberflächenmodifikationen (physikalisch und chemisch) als Mittel zur Verbesserung der Biokompatibilität und der Protein-/Zelladhäsion sowie die Erzeugung chemisch gradientierter Oberflächen, die die Untersuchung und Manipulation des biologischen Verhaltens ermöglichen. Aus fertigungstechnischer Perspektive ist es unerlässlich, dass die Oberflächenvorbereitung, sei es durch Plasma, Silanisierung oder gepfropfte Schichten, als validierter, reproduzierbarer Prozess etabliert wird und nicht als Kunstfertigkeit betrachtet wird.
In der Gewebetechnik und der Herstellung von biohybriden Organen umfasst die Technologie den Aufbau von Gerüst-Mikroarchitekturen, Methoden zu deren Sterilisation ohne Beeinträchtigung der biologischen Funktion sowie die Steuerung von Bioreaktorparametern und Zellbesiedlungsverfahren. Diffusion, Permeabilität und Wandmechanik müssen bei der Konstruktion immunprotektiver Kapseln oder offener Architekturen simultan gesteuert werden.
Materialklassen
Zur Anwendung der oben genannten Prinzipien auf klinische Indikationen in der Orthopädie ist bei der Auswahl des Gleitpaarungsmaterials und der Fixierungsstrategie für Endoprothesen ein Kompromiss erforderlich, der einerseits Verschleiß, mechanische Stabilität und Ermüdungsfestigkeit und andererseits die biologische Integration mit dem Knochen berücksichtigt. Aus diesem Grund gab es in der Literatur intensive Entwicklungen im Bereich poröser, bioaktiver Beschichtungen und Oberflächenmodifikationen von Polymeren mit ultrahohem Molekulargewicht. In der Zahnmedizin findet sich eine analoge Vorgehensweise bei Implantaten und Restaurationen, wobei bioinerte sowie bioaktive Keramiken, Titan und Zirkoniumoxid in Kombination mit Mikro- und Nanostrukturen zum Einsatz kommen, die die Osseointegration und die biologische Dichtheit des Schleimhautübergangs fördern. Im Herz-Kreislauf-System ist die Konstruktion von Klappen und Transplantaten eine direkte Ableitung der Hämodynamik und der prokoagulierenden Auswirkungen der lokalen Geometrie und Rauheit.
Membranvorrichtungen im Nierenbereich demonstrieren, inwiefern sich die Theorien von Clearance, Permeabilität und Gesamttransport in ein praktisches Behandlungsschema überführen lassen, und sie verdeutlichen, wie sich hieraus die Pharmakokinetik von Arzneimitteln sowie die Beurteilung der Dialyseadäquanz ableiten lassen. Darüber hinaus wird ersichtlich, dass geringfügige Unterschiede in Membranen, Strömungen und Hydraulik zu klinisch signifikanten Differenzen führen. Die Übertragung auf die Klinik erfordert die Zuordnung physiologischer Anforderungen zu Material-, Geometrie-, Transport- und Herstellungsparametern; es gibt kein bestes Material außerhalb des Kontexts einer bestimmten Anwendung und Belastung.
Die Herausgeber der Monografie weisen auf die Richtung der Entwicklung hin: Geräte, die lebende Komponenten mit synthetischen Strukturen integrieren, wie z. B. biohybride Organe und Informationsprothesen, die dem Körper Ersatz- oder modulierte Signale liefern, um eine Erkrankung zu korrigieren. Im Fokus stehen nicht nur Steuerungsalgorithmen, sondern in gleichem Maße Materialien sowie Oberflächenschnittstellen, die über viele Jahre hinweg eine hohe Funktionssicherheit gewährleisten müssen. Um Soft-Robotik-Geräte sowie Sensoren mit hoher biologischer Spezifität (Enzym-Substrat, Antigen-Antikörper, Ligand-Rezeptor) zu entwickeln, beherrschen Konstrukteure Mikro- und Nanofertigungstechnologien und stabilisieren aktive Schichten.
Biomedizinische Technik im Kontext der Materialwissenschaften – Zusammenfassung
Die zweite Ausgabe des The Biomedical Engineering Handbook bietet einen umfassenden Überblick über die biomedizinische Technik, der Klassen von Biomaterialien, Sensoren und Messungen sowie Gewebetechnik und künstliche Organe umfasst. Drei zentrale Themen durchziehen den vorliegenden Überblick. Erstens steht die Systemizität im Zentrum, denn Material, Oberfläche, Transport, Strömungsmechanik, Elektronik sowie der Herstellungsprozess bilden eine untrennbare Einheit, die sich gegenseitig in Bezug auf Sicherheit und Wirksamkeit beeinflusst. Das zweite ist die Skalierbarkeit: Von Molekülen und adhäsiven Liganden über 10–100 µm-Architekturen bis hin zu ganzen Geräten müssen die Parameter auf einer Skala mit den Anforderungen auf anderen Skalen übereinstimmen. Als drittes Kriterium ist die Herstellbarkeit zu nennen, wobei Sterilisation, Sauberkeit, die Kontrolle von Porosität und Rauheit, Passivierung sowie Oberflächenmodifikation nicht als nachträgliche Zusatzfunktionen, sondern als integral definierte Designelemente zu betrachten sind.
Infolgedessen fungiert der biomedizinische Konstrukteur als Dirigent, der Materialien, Strömungen, Signale und Prozesse koordiniert, um die gewünschte biologische Reaktion auszulösen und gemeinsam eine Betriebsstabilität zu erreichen. Diese Perspektive, die in der Monografie konsequent entwickelt wird, bleibt eine aktuelle Grundlage für Praktiker in der Biomedizin, Zahnmedizin und Präzisionsfertigung.
Literaturverzeichnis
Bronzino, J.D. (Hrsg.). The Biomedical Engineering Handbook. Zweite Auflage. CRC Press, Boca Raton, 2000.




