Varför är ytan på ett implantat så viktig?
Inom biomaterialteknik är det lätt att förlita sig på den intuition som härrör från traditionell materialvetenskap: eftersom ett implantat måste tåla belastningar, inte korrodera, inte slitas ned i överdriven utsträckning och fungera i åratal, borde dess framgång i första hand bero på materialet ”inuti”. Detta är dock bara en del av sanningen. Materialet i sig står visserligen för styrka, styvhet, elasticitet, hållbarhet och permeabilitet. Men ur kroppens perspektiv sker den första och viktigaste kontakten inte med hela materialblocket, utan med dess yttre skikt. Det är detta skikt som kommer i kontakt med blod, proteiner, celler och kroppsvätskor. I praktiken innebär detta att ett implantat kan vara mekaniskt mycket bra men ändå biologiskt problematiskt om dess yta sänder ”fel signal” till vävnaderna.
Denna iakttagelse förändrar vårt sätt att tänka kring implantatdesign. Istället för att endast fråga ”vad ska implantatet vara tillverkat av?” måste vi överväga hur implantatets yta bör se ut. När det gäller biomaterial är den biologiska responsen inte en enkel återspegling av hela komponentens kemiska sammansättning. Det är snarare en respons på vad som sker vid gränssnittet mellan material och vävnad: ytkemi, vätbarhet, laddning, grovhet, struktur och reaktivitet. Det är därför ett implantats framgång så ofta avgörs, inte av materialets volym, utan just vid fasgränsen.
Denna artikel baseras på Biomaterials Science: An Introduction to Materials in Medicine, red. William R. Wagner et al., 4:e uppl., 2020. Följande innehåll är endast en allmän översikt över ämnet. För den som är intresserad av ämnet rekommenderar vi att fördjupa sig i litteraturen.
Hur reagerar kroppen på ett materials yta?
Den viktigaste utgångspunkten är enkel: kroppen ”ser” inte hela implantatet på en gång. Först ”läser” den dess yta. Författarna till Biomaterials Science anger särskilt att för material som inte avger oönskade ämnen sker informationsöverföringen från materialet till proteiner, celler och hela kroppen genom ytstrukturen. Kroppen reagerar därför på den specifika kemin och organisationen i det yttre skiktet, snarare än på de genomsnittliga egenskaperna hos hela materialet. Denna till synes lilla förskjutning i tyngdpunkten har enorm praktisk betydelse, eftersom den flyttar frågan om biokompatibilitet från nivån ”vilken typ av legering eller polymer vi har” till nivån ”hur dess gränssnitt ser ut och beter sig”.
Det är viktigt att komma ihåg att ytan inte bara är en tunn del av materialet som beter sig på samma sätt som dess inre. Boken betonar att ytan är en zon med särskild reaktivitet och nästan oundvikligen skiljer sig från resten av materialet. För ett verkligt metalliskt material kan det yttre skiktet innehålla inte bara metalloxid, utan även adsorberat vatten, polära organiska föreningar och kolväteföroreningar. För polymerer kan den unika ytzonen sträcka sig från cirka 10 till 100 nm. Detta är viktigt eftersom det innebär att även om materialet i sin helhet är homogent kan dess biologiskt aktiva del vara kemiskt och strukturellt komplex.
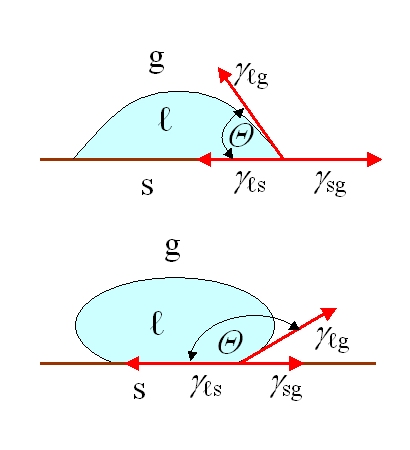
Ur ett biologiskt perspektiv handlar ytan inte enbart om kemisk sammansättning. Författarna listar många egenskaper som kan påverka biologiska reaktioner: ojämnhet, mönster och topografi, vätbarhet, ytmobilitet, kemisk sammansättning, elektrisk laddning, kristallinitet, elasticitetsmodul och heterogenitet. Samtidigt konstaterar de ärligt att det ännu inte är möjligt att identifiera en enda universell egenskap som är viktigast för varje biologisk reaktion. I praktiken är detta en mycket ingenjörsinriktad lärdom; man får inte basera en design på en enda parametrisk slogan som ”låt oss öka grovheten” eller ”låt oss göra ytan mer hydrofil”, eftersom kroppens reaktion är resultatet av samspelet mellan flera egenskaper samtidigt.
Detta synsätt förklarar varför två implantat tillverkade av samma grundmaterial kan uppföra sig biologiskt olika. En förändring i bearbetning, sterilisering, lagring eller förpackning räcker för att förändra ytförhållandena. Boken belyser till och med så vardagliga frågor som fingeravtryck, tillsatser som migrerar från förpackningen eller föroreningar från papper eller film. I laboratoriet är detta en detalj, men i verkligheten är det just sådana detaljer som kan leda till att vi testar en yta som inte är den som faktiskt finns på det implantat som används kliniskt.

Hur ytan påverkar biokompatibiliteten
Om ytan är det primära kommunikationsspråket mellan implantatet och kroppen, måste vi fråga oss hur denna dialog ser ut. En av de viktigaste mekanismerna är proteinadsorption. Källan betonar att efter implantation av ett syntetiskt biomaterial adsorberas adhesiva proteiner på dess yta mycket snabbt, inom några sekunder. På detta sätt blir ett material som i sig saknar biologiska igenkänningsmotiv ”läsbart” för kroppen. Med andra ord reagerar celler ofta inte direkt på det rena materialet, utan på det proteinskikt som bildas på dess yta kort efter kontakt med kroppen.
Detta har en grundläggande betydelse för förståelsen av biokompatibilitet. Biokompatibilitet innebär inte bara frånvaron av akut toxicitet. Det innebär materialets förmåga att framkalla en lämplig värdrespons i en specifik tillämpning. Denna ”lämpliga respons” kan betyda en sak för en stent, en annan för ett ortopediskt implantat och ännu en annan för en kateter. I vart och ett av dessa fall styr ytan de initiala biologiska händelserna: vilka proteiner som kommer att adsorberas, i vilken konfiguration, vilka cellreceptorer som kommer att stimuleras och om signalen kommer att leda till vävnadsintegration, trombocytaktivering, biofilmbildning eller en främmande kroppsreaktion.
Ett bra exempel är jämförelsen mellan adhesionsproteiner och passiveringsproteiner. Boken beskriver hur förbeläggning av en yta med fibronektin ökar adhesionen hos många celler, medan albumin kan begränsa den. Detta är inte bara en kuriositet från cellodling, utan en modell för vad som händer på implantat. Ytan är inte en neutral bakgrund. Den sätter de initiala villkoren för den efterföljande cellulära responsen. I praktiken innebär detta att två ytor med liknande mekanisk hållfasthet kan leda till helt olika läkningsförlopp, helt enkelt därför att de etablerar det första skiktet av adsorberade proteiner på olika sätt.
Lika viktiga är interaktionerna mellan ytan och mikroorganismerna. I kapitlet om biofilmer noterar författarna att vätbarhet, laddning, grovhet och topografi påverkar bakteriell adhesion. Den allmänna trenden är att större ojämnhet ofta främjar bakteriell adhesion, och hydrofoba ytor underlättar oftare bakteriell vidhäftning. Samtidigt är detta inte en regel utan undantag, eftersom extremt superhydrofiliska eller superhydrofoba system kan fungera som biofilmhämmare genom en annan mekanism. I praktiken fungerar detta som en varning: en lösning som är fördelaktig för vävnadsintegration kommer inte alltid att vara lika fördelaktig för att kontrollera bakteriell kolonisering.
Nedan finns en engelskspråkig video med titeln BIOE 5820 Biomaterials Protein Adsorption, som är en föreläsning om proteinadsorption på biomaterialytor.
Varför modifiera ytan istället för hela materialet
Följande är den huvudsakliga motiveringen bakom ytmodifiering. Om materialet i sin helhet ansvarar för bärförmåga, hållbarhet och mekanisk funktion, medan ytan ansvarar för biointeraktion, är det mest logiskt att bevara det som fungerar bra i materialet och endast modifiera det som kommer i kontakt med vävnaden. Det är precis så författarna till kapitlet om fysikalisk-kemiska ytmodifieringar uttrycker det: målet är att bevara biomaterialets viktigaste fysikaliska egenskaper samtidigt som endast det yttre skiktet ändras för att förbättra eller modulera den biologiska responsen vid gränssnittet mellan vävnad och implantat.
Denna strategi har flera mycket praktiska fördelar. För det första behöver man inte överge ett material som är välkänt ur mekanisk och teknisk synvinkel. Titan, stål, tekniska polymerer eller elastomerer kan fortsätta att fylla sin strukturella eller funktionella roll. För det andra kan den biologiska responsen skräddarsys mer exakt för en given tillämpning. Vi vill ha en annan yta för ett benimplantat, en annan för en komponent som kommer i kontakt med blod och ytterligare en annan för en kateter, där prioriteringen kan vara att begränsa proteinadsorption och vidhäftning av celler eller bakterier. För det tredje möjliggör ytmodifiering en förbättring av en anordning utan att man behöver omkonstruera hela strukturen. Boken betonar till och med att för anordningar som redan är väl etablerade i klinisk praxis är detta ett sätt att ändra biointeraktioner utan att omkonstruera produkten, omstrukturera produktionen eller omskola medicinsk personal för att använda den nya lösningen.
Det finns dock ett villkor: man måste skilja mellan en verklig modifiering av gränssnittet och en kosmetisk förändring i beskrivningen. Enbart påståendet att ett material är ”bioaktivt” eller ”antifouling”/”påväxthindrande” betyder föga om man inte vet hur ytan faktiskt ser ut i sin slutliga form efter bearbetning och sterilisering. Källan påpekar att det analyserade provet bör motsvara så nära som möjligt det material eller den anordning som används för biologisk testning eller implantation. Detta är viktigt eftersom den yta som utsätts för luft kanske inte är samma yta som materialet uppvisar i kroppens vattenmiljö.
Tre huvudsakliga metoder för ytmodifiering
Den första metoden innebär att man förändrar den befintliga ytan utan att lägga till ett separat, nytt skikt. Atomer, molekyler och bindningar som redan finns i materialets yttre skikt kan omvandlas kemiskt eller fysiskt. Denna grupp omfattar bland annat etsning, kemisk aktivering, mekanisk uppruggning, jonimplantering och vissa laserbehandlingar. Poängen är att man inte ”fäster” ett nytt skikt på implantatet, utan snarare omformar dess egen yta. Detta är fördelaktigt där en stark integration av modifieringen med substratet är viktig, liksom att minska risken för delaminering och förändra egenskaper såsom reaktivitet, vätbarhet, korrosionsbeständighet, hårdhet eller bioaktivitet. Källan visar till exempel att jonimplantering kan förbättra slitstyrkan eller korrosionsbeständigheten, och att laserbearbetning på ett kontrollerat sätt kan förändra ytjämnhet, kristallinitet och kemi.
Den andra metoden innebär att man applicerar ett nytt skikt eller en ny beläggning. I detta fall placeras ett material med annan sammansättning eller andra egenskaper på den befintliga ytan. Detta kan vara en tunn film, ett ympat skikt, en polymerbeläggning eller ett system utformat som en påväxthindrande yta. Denna strategi är särskilt värdefull när substratet har idealiska mekaniska egenskaper men är för ”rått” ur biologisk synvinkel. Ett bra exempel är ytor som är resistenta mot ospecifik proteinadsorption. Deras mekanism bygger vanligtvis på ett starkt hydratiseringsskikt, som fungerar som en energetisk och fysisk barriär mot proteiner. I kapitlet om nonfouling surfaces (påväxthindrande ytor) beskriver författarna två huvudstrategier för att applicera sådana system: ”graft-to-surface”, där materialet adsorberas eller binds från lösningen, och ”graft-from-surface”, där polymerborstar växer från ytan. Den första metoden är tekniskt enklare; den andra uppnår lättare hög packningsdensitet men kräver vanligtvis mer komplex kemi och substratförberedelse.
I praktiken har denna skillnad ingenjörsmässig betydelse. Om vi bara vill snabbt begränsa proteinavlagring på ett relativt enkelt substrat kan den enklare lösningen räcka. Men om vi behöver ett hållbart, ogenomträngligt och tätt packat antiadsorptionsskikt, kanske det inte räcker att bara ”klistra fast” molekyler på ytan. Boken betonar tydligt att valet av metod avgör packningsdensiteten, antalet defekter och hållbarheten hos den slutliga ytan. Detta innebär att beläggningar inte utvärderas enbart utifrån deras deklarerade kemi, utan utifrån om de faktiskt bildar ett homogent, stabilt gränssnitt under driftsförhållanden.
Den tredje metoden handlar om att skapa mönster, texturer och topografier. Här ligger huvudfokus inte på att ändra den kemiska sammansättningen, utan på att förändra geometrin hos det som cellen eller proteinet ”ser”. Källan betonar att yttopografin påverkar celladhesion, proliferation, migration, differentiering och genuttryck. Celler reagerar på både mikro- och nanoskalegenskaper, inte bara på materialets blotta närvaro. I de studier som citeras i boken förändrade varierande höjder, storlekar och avstånd mellan topografiska strukturer graden av mineralisering, cellorientering, celladhesion och differentiering. Detta innebär att texturen inte är en ren prydnad eller en bieffekt av bearbetningen, utan ett aktivt verktyg för att styra biologiska reaktioner.
Detta är särskilt tydligt när det gäller ben- och tandimplantat. Boken beskriver hur ett ytskikt med lämplig grovhet eller tredimensionell struktur kan påskynda de tidiga stadierna av läkning, främja fibrinavsättning, integrinbindning och mikromekanisk sammankoppling med benet. Som ett resultat ökar skjuvhållfastheten vid gränssnittet mellan implantat och ben, och belastningsöverföringen förbättras. Detta är ett bra exempel på hur texturering inte är en ”blind förbättring”, utan ett försök att styra en specifik gränssnittsmekanism. Man måste dock vara försiktig, eftersom samma grovhet som underlättar osseointegration i en annan tillämpning kan öka risken för bakteriell kolonisering eller hindra ytkontroll.

Vanliga misstag, fallgropar och felaktiga slutsatser
Det vanligaste misstaget är att likställa ”bättre material” med ”bättre biologisk respons”. Det är alltför förenklat. Hållfasthet, utmattningsmotstånd och kemisk stabilitet förklarar ännu inte vad som kommer att hända vid vävnadsgränssnittet. När det gäller biomaterial kan man ha ett utmärkt strukturellt material och en dålig biologisk gränsyta. Man kan också ställas inför det motsatta problemet: en yta med hög biologisk aktivitet monterad på ett substrat som inte uppfyller de mekaniska kraven. Det är just därför som premissen att materialet ger implantatet hållfasthet, medan ytan avgör kroppens respons, är användbar vid design. Den tvingar oss att skilja på två frågor som ofta klumpas ihop inom klassisk teknik.
Den andra fallgropen är tron att en enda ytegenskap kommer att lösa hela problemet. I praktiken finns det ingen universell ”inställning för biokompatibilitet”. Att öka hydrofiliciteten kan begränsa adsorptionen av vissa proteiner, men det förbättrar inte nödvändigtvis vävnadsintegrationen. Att öka ytans grovhet kan främja osteoblasternas respons, men det är kanske inte fördelaktigt i en miljö där det finns risk för infektion. I boken påpekas att det ännu inte är känt vilken parameter som är viktigast för varje specifik biologisk respons, så variablerna måste mätas och korreleras oberoende av varandra. Detta är en mycket viktig metodologisk riktlinje: istället för att söka efter ett enda magiskt tal måste man skapa en karta över relationerna mellan flera gränssnittsegenskaper och ett specifikt kliniskt mål.
Den tredje fallgropen gäller modifieringens tjocklek. Författarna till kapitlet om fysikalisk-kemiska modifieringar betonar att modifieringarna bör vara så tunna som möjligt. Idealt sett skulle det räcka att ändra endast de yttersta molekylskikten – i storleksordningen några nanometer – men i praktiken måste skikten ibland vara tjockare för att säkerställa enhetlighet och hållbarhet. En beläggning som är för tjock kan förändra enhetens mekaniska och funktionella egenskaper, samt öka risken för sprickbildning och delaminering. Detta är särskilt viktigt där implantatet utsätts för utmattning eller friktion. Ett skikt som ser lovande ut ur biologisk synvinkel men som mekaniskt flagnar av efter en tid löser inte problemet; det skapar bara ett nytt.
Den fjärde missuppfattningen är att behandla ytan som ett statiskt tillstånd. Källan visar att vissa material kan vända sin ytorganisation vid övergången från luft till en vattenhaltig miljö. En yta som mäts ”under torra förhållanden” är kanske inte samma yta som proteiner och celler möter i kroppen. Detta har direkta konsekvenser för forskningen. Om ytanalysen inte tar hänsyn till driftsmiljön kan man optimera en parameter som upphör att ha samma värde eller betydelse efter implantation.
När en mer avancerad teori behövs
Ett avancerat tillvägagångssätt blir nödvändigt när intuitiva termer som ”slätare”, ”mer hydrofil” eller ”grövre” inte längre räcker till. Påväxthindrande ytor är ett exempel på detta. Deras funktion beror inte bara på att de är hala, utan på att de bildar ett stabilt hydratiseringsskikt, vars borttagning är energimässigt ogynnsamt för adsorberande proteiner. Boken visar att PEG-baserade hydrofila material binder vatten genom vätebindningar, medan zwitterjoniska material kan göra det ännu starkare genom elektrostatiskt inducerad hydratisering. På denna nivå måste man beakta inte bara funktionell kemi utan även kedjepaketdensitet, konformationsfrihet och stabiliteten hos skiktets förankring.
Avancerad teori behövs också när ytan inte bara är avsedd att vara icke-störande utan att aktivt styra cellernas beteende. I sådana fall är det geometrin på mikro- och nanoskalan, den lokala mekaniken, storleken, höjden och avståndet mellan topografiska särdrag, och ibland till och med mönstrets ordning eller oordning, som spelar roll. Det är just därför som dagens forskning använder topografiska matriser och mer systematiska ytundersökningar. Det handlar inte om ämnets akademiska komplexitet, utan om det faktum att celler verkligen skiljer mellan skalor och mönster hos egenskaper, och att den biologiska responsen upphör att vara en linjär funktion av en enda parameter.
Varför är ytan på ett implantat så viktig? – sammanfattning
När det gäller biomaterial avgörs ofta ett implantats framgång inte av själva materialet, utan av den yta det visar upp mot kroppen. Det är ytan som är den första kontaktpunkten med proteiner, celler och kroppsvätskor, och som därmed i stor utsträckning styr biokompatibiliteten. Av denna anledning innebär en förnuftig implantatdesign att funktionerna separeras: volymen är avsedd att säkerställa mekaniska egenskaper och hållbarhet, medan ytan är avsedd att framkalla rätt biologisk respons. Detta är grunden för hela logiken bakom att modifiera ytan utan att ändra hela materialet. Man kan omforma det befintliga yttre skiktet, applicera en ny beläggning eller utforma ett mönster och en topografi som påverkar proteinadsorption, cellbeteende, vävnadsintegration eller motståndskraft mot påväxt. Det finns ett villkor: modifieringen måste vara verkligt gränsskiktsbaserad, tunn, hållbar och anpassad till ett specifikt kliniskt mål. Det är just därför som ytan inom biomaterial inte är en ytlig detalj, utan ett av de viktigaste verktygen i implantatdesign.




