A cerâmica como material biomédico

Índice
A cerâmica costuma estar associada à porcelana, ao vidro ou a elementos arquitetónicos. Na engenharia biomédica, no entanto, o termo tem um significado muito mais amplo. A cerâmica é um material inorgânico e não metálico, cujos principais componentes são geralmente óxidos metálicos, silicatos, carbonetos ou nitretos. Caracterizam-se por uma elevada dureza, elevada resistência à compressão, elevado ponto de fusão, e condutividade elétrica e térmica muito baixas. Ao nível atómico, as suas propriedades resultam principalmente da predominância de ligações iónicas ou covalentes e do número limitado de planos de deslizamento possíveis na rede cristalina. É por isso que a cerâmica, ao contrário dos metais, não sofre facilmente deformação plástica.
A principal consequência desta estrutura é a fragilidade. A cerâmica tende a rachar na presença de microfissuras, inclusões ou entalhes acentuados. Em vez de se deformar gradualmente, como os metais, ela quebra repentinamente e de forma relativamente violenta quando a tensão perto de um defeito existente excede um valor crítico. É por este motivo que a sua resistência à tração é muito menor do que a sua resistência à compressão. Curiosamente, em condições ideais, quando o material está praticamente isento de defeitos, a cerâmica pode ser extremamente resistente. Um exemplo são as microfibras de vidro, que têm uma resistência à tração de vários gigapascais, excedendo a resistência de muitos aços de alta resistência.
A cerâmica também é um material que praticamente não sofre deformação à temperatura ambiente. Enquanto os metais podem deformar-se gradualmente sob tensão prolongada, a cerâmica, devido à sua estrutura rígida, mantém a sua dimensionalidade até que uma fissura se inicie. Esta característica é uma vantagem quando pensamos na transferência estável de carga, e uma desvantagem, porque a incapacidade de «libertar» tensões através da deformação plástica promove fraturas repentinas.
O campo da biocerâmica surgiu quando a cerâmica começou a ser conscientemente utilizada para contacto com tecidos corporais. Descobriu-se que é possível utilizar composições cerâmicas adequadamente selecionadas não apenas em indústrias eletrónicas ou de alta temperatura, mas também para substituir fragmentos ósseos, reconstruir dentes, construir implantes articulares e até mesmo elementos que entram em contacto com o sangue, como válvulas cardíacas artificiais. No entanto, vários critérios biológicos básicos devem ser atendidos.
Para que um material cerâmico seja considerado biocerâmico, deve ser atóxico, não cancerígeno, não alergénico, não deve causar reações inflamatórias crónicas e deve ser biocompatível e manter a sua biofuncionalidade durante todo o período de implantação previsto. Por outras palavras, não deve causar danos, deve cumprir a sua função mecânica ou biológica e não deve degradar-se de forma imprevisível.
Com base nisso, as biocerâmicas são divididas em três classes principais. A primeira classe consiste em cerâmicas não absorvíveis, ou seja, cerâmicas relativamente biocompatíveis que, após a implantação, praticamente não se dissolvem nem sofrem alterações estruturais significativas e são projetadas para durar muitos anos. O segundo grupo consiste em cerâmicas biodegradáveis (reabsorvíveis), que são projetadas para serem gradualmente substituídas pelo tecido em crescimento do hospedeiro. A terceira categoria consiste em biocerâmicas bioativas e reativas à superfície, cuja função é formar uma forte ligação química com o osso ou outro tecido, principalmente através de reações que ocorrem apenas na zona superficial.

Biocerâmicas relativamente biocompatíveis
As biocerâmicas relativamente compatíveis mantêm as suas propriedades físicas e mecânicas durante o uso prolongado no corpo. Não se dissolvem de forma significativa, são resistentes à corrosão e ao desgaste, e o contacto com os tecidos geralmente resume-se a uma adaptação ou integração mecânica, sem reações químicas significativas. O óxido de alumínio, o óxido de zircónio e vários tipos de carbono, incluindo o carbono pirolítico, são particularmente importantes neste grupo.
O óxido de alumínio, também conhecido como alumina (Al₂O₃), é um dos materiais cerâmicos mais utilizados na implantologia. Em aplicações biomédicas, utiliza-se uma variedade alfa de alta pureza, na qual o teor de Al₂O₃ excede 99,5% e a quantidade de impurezas, como sílica e óxidos alcalinos, é limitada a décimos de um por cento. A alumina tem uma estrutura cristalina romboédrica e ocorre naturalmente como safira ou rubi, dependendo das impurezas presentes que lhe conferem cor. Formas monocristalinas deste material podem ser obtidas através da fusão gradual do pó sobre uma semente de cristal, a partir da qual o cristal em crescimento é «puxado».
As propriedades mecânicas da alumina são impressionantes. O seu módulo de Young atinge várias centenas de gigapascais, a sua resistência à flexão excede 400 MPa e a sua dureza varia entre 20 GPa e 30 GPa. Este último valor significa que o óxido de alumínio ocupa uma posição muito elevada na escala de Mohs (9/10), ficando apenas atrás do diamante. No entanto, a resistência e a fiabilidade da alumina policristalina dependem significativamente do tamanho dos grãos e da porosidade. Reduzir a porosidade e usar uma estrutura de grãos finos aumenta a resistência e reduz a dispersão dos resultados.
Esta combinação de dureza, resistência ao desgaste e inércia química no ambiente corporal torna a alumina o material de eleição para a construção de elementos deslizantes em endopróteses articulares, especialmente cabeças de próteses de anca que interagem com copos de polietileno de peso molecular ultraelevado. Estudos com implantes de óxido de alumínio inseridos no crânio não revelaram toxicidade nem sinais de rejeição e demonstraram uma tolerância muito boa durante longos períodos de observação. A alumina também pode ser aplicada em implantes dentários, placas e parafusos ósseos, reconstruções do ouvido médio e componentes que exigem alta dureza e inércia química.
O segundo material importante neste grupo é o óxido de zircónio (ZrO₂). Na sua forma pura, tem um diagrama de fases complexo – a diferentes temperaturas, assume diferentes estruturas cristalinas, acompanhadas por alterações significativas no volume. Esta variabilidade é desfavorável do ponto de vista da estabilidade dimensional, razão pela qual a zircónia parcialmente estabilizada com óxidos como o Y₂O₃ é utilizada na prática. Graças a estes aditivos, é possível estabilizar fases de alta temperatura (tetragonal ou cúbica) também em temperaturas mais baixas, o que melhora a estabilidade da estrutura após a sinterização.
A zircónia parcialmente estabilizada tem um módulo de elasticidade inferior ao da alumina, o que a torna ligeiramente mais semelhante ao osso, ao mesmo tempo que apresenta uma resistência particularmente boa à fratura. Isto deve-se ao mecanismo de reforço transformacional – ocorre uma transição de fase local perto da fratura em propagação, acompanhada por um ligeiro aumento de volume, que «fecha» a fratura e impede o seu crescimento. A biocompatibilidade da zircónia é muito boa, e os seus parâmetros de atrito e desgaste quando utilizada com UHMWPE são tão favoráveis que este material passou a ser aplicado em cabeças de endopróteses articulares e outros elementos de suporte de carga.
Várias formas de carbono desempenham um papel especial entre as cerâmicas bioinertes. A estrutura cristalina da grafite, uma forma clássica de carbono, consiste em redes planas hexagonais de átomos ligados por fortes ligações covalentes, dispostas em camadas. Interações mais fracas ocorrem entre as camadas, o que facilita o seu movimento relativo entre si e explica a lubrificação da grafite. Em materiais como o carbono pirolítico ou o carbono vítreo, estas camadas hexagonais são parcialmente perturbadas, deformadas e misturadas com áreas amorfas. Em escala macro, isto traduz-se em propriedades mecânicas mais isotrópicas.
O carbono pirolítico é particularmente valioso na implantologia, pois é caracterizado por alta resistência, módulo de elasticidade decente e excelente compatibilidade com o sangue. Este material costuma ser mais utilizado como revestimento aplicado a partir da fase gasosa às formas finais dos implantes, por exemplo, componentes de válvulas cardíacas ou próteses vasculares. Os parâmetros do processo, tais como temperatura, pressão, composição do gás, geometria do reator e tempo de deposição, permitem um ajuste muito preciso da densidade, anisotropia, tamanho dos cristalitos e presença de defeitos no carbono. Uma densidade mais elevada significa geralmente maior resistência e módulo de elasticidade, o que é fundamental para a segurança a longo prazo dos implantes.
Existem também compósitos carbono-carbono, nos quais as fibras de carbono reforçam a matriz de carbono. Estes compósitos alcançam uma resistência muito alta ao longo da direção das fibras, mas são distintamente anisotrópicos e porosos. Do ponto de vista mecânico, podem ser interessantes, mas o seu uso requer um planeamento extremamente cuidadoso da distribuição de carga no corpo.
Biocerâmicas biodegradáveis
Em muitas aplicações, o objetivo não é substituir permanentemente o tecido, mas preencher temporariamente um defeito, fornecer suporte mecânico ou administrar um medicamento, após o qual o implante deve ser gradualmente substituído pelo tecido hospedeiro em regeneração. Nestas situações, as cerâmicas reabsorvíveis, que se degradam de maneira controlada, são a escolha ideal.
Historicamente, um dos primeiros materiais deste tipo foi o gesso, ou sulfato de cálcio di-hidratado, que já era utilizado no final do século XIX como substituto ósseo. No entanto, a verdadeira inovação ocorreu na segunda metade do século XX, com o advento dos fosfatos de cálcio totalmente sintéticos e de sistemas mais complexos, como cerâmicas de fosfato de alumínio-cálcio (ALCAP), fosfato de zinco-cálcio (ZCAP), fosfato de zinco-sulfato-cálcio (ZSCAP) e fosfato de ferro-cálcio (FECAP).
O representante mais importante deste grupo é a hidroxiapatita (HA), quimicamente semelhante à fase mineral dos ossos e dentes. Tem uma fórmula semelhante a Ca₁₀(PO₄)₆(OH)₂ e pertence à família da apatita. Estruturalmente, forma prismas hexagonais nos quais os iões hidroxilo estão dispostos em colunas ao longo do eixo c, e alguns dos iões cálcio estão fortemente ligados a eles. Os iões Ca²⁺ restantes completam a rede cristalina, garantindo a estabilidade da estrutura. A razão molar do cálcio para o fósforo é de 10:6, e a densidade teórica é próxima de 3,2 g/cm³. A substituição dos iões OH⁻ por iões F⁻ resulta num aumento da estabilidade química, motivo pelo qual a fluoretação fortalece o esmalte dos dentes.
A hidroxiapatita é um material com biocompatibilidade excecional, uma vez que a sua estrutura e composição química se assemelham muito às do tecido ósseo natural. Após a implantação na forma de grânulos ou blocos porosos, forma-se rapidamente osso esponjoso novo, e a fronteira entre o implante e o osso assume frequentemente a forma de uma ligação química direta, sem uma zona fibrosa distinta.
As propriedades mecânicas da hidroxiapatita podem variar significativamente dependendo do método de fabrico, do tamanho do grão e da porosidade. O módulo de elasticidade pode atingir um valor comparável ao dos tecidos duros naturais, como esmalte, dentina ou osso compacto. Isto permite a criação de implantes cuja rigidez é compatível com o tecido circundante, reduzindo o risco do fenómeno adverso conhecido como blindagem de tensão, ou seja, descarga e perda óssea gradual.
Além da hidroxiapatita, o beta fosfato tricálcico (β-TCP) desempenha um papel importante. É mais solúvel do que a HA, o que resulta numa reabsorção mais rápida in vivo, mantendo uma boa osteocondutividade. Desta forma, o material torna-se adequado como preenchimento temporário de defeitos ósseos, que desaparece gradualmente à medida que o osso do paciente cresce. Tal como a hidroxiapatita, o TCP é frequentemente produzido por síntese húmida a partir de sais de cálcio e fosfato apropriados, seguido de calcinação e sinterização. Pode formar compostos com aminoácidos como a cisteína, que, quando misturados com água, ligam-se e endurecem no local da implantação, permitindo que o material se forme diretamente no defeito.
Sistemas cerâmicos mais complexos, como ALCAP, ZCAP, ZSCAP e FECAP, são geralmente polifásicos. Isto significa que a sua estrutura contém várias fases cristalinas diferentes, com taxas de solubilidade e reabsorção variáveis. Esta estrutura permite a criação de materiais que se degradam em várias etapas: algumas fases desaparecem mais rapidamente, outras mais lentamente e, durante esse processo, são libertados iões importantes do ponto de vista biológico, como zinco ou ferro. Estes também podem ser usados como transportadores de medicamentos. A substância ativa é encerrada numa matriz cerâmica e libertada gradualmente à medida que o implante é reabsorvido.
Um exemplo interessante de material reabsorvível natural é a corallina, ou seja, o esqueleto dos corais, composto principalmente por carbonato de cálcio na forma de aragonita. Cada espécie de coral forma estruturas porosas tridimensionais únicas que se assemelham ao osso trabecular em termos de tamanho e distribuição dos poros. Isto faz com que os materiais como o Biocoral sejam ideais para preencher defeitos ósseos. O carbonato de cálcio sofre reabsorção gradual e é substituído pelo osso. Além disso, os esqueletos de coral podem ser convertidos hidrotermicamente em hidroxiapatita, mantendo sua arquitetura natural de poros, combinando as vantagens de uma estreita semelhança química com o osso com uma microestrutura espacial muito favorável.
Biocerâmicas bioativas reativas à superfície
Entre cerâmicas extremamente inertes e materiais mais rapidamente reabsorvíveis, existe um terceiro grupo extremamente importante: as biocerâmicas bioativas, ou seja, vidros reativos à superfície, vitrocerâmicas e certas formas de hidroxiapatita. A sua característica especial é que, embora o volume total do material permaneça relativamente estável, a superfície reage ativamente com os fluidos corporais, formando uma camada que pode criar uma forte ligação química com o osso.
Um exemplo clássico são os vidros de silicato bioativos, como os materiais da família Bioglass, e os seus equivalentes cristalizados, os vidros-cerâmicos. Estes sistemas são baseados em sílica (SiO₂) com aditivos de óxido de cálcio, óxido de sódio e óxido de fósforo (V). Após a implantação no corpo, ocorre uma série de reações na superfície destes materiais: primeiro, os iões Na⁺ e Ca²⁺ são trocados com o ambiente, provocando uma alteração local no pH e na atividade iónica. Em seguida, forma-se uma camada de gel rica em sílica, na qual precipitam fosfatos de cálcio que, com o tempo, se transformam numa estrutura semelhante à apatita. Esta camada superficial de apatita permite que o osso se fixe diretamente no vidro, sem a mediação do tecido fibroso.
A bioatividade do vidro depende fortemente da sua composição química, principalmente do teor de SiO₂ e das proporções de CaO, Na₂O e P₂O₅. Existe uma faixa específica de composição na qual tanto a camada de sílica quanto a de fosfato são formadas simultaneamente. Fora dessa faixa, o material é muito pouco reativo para formar uma ligação duradoura com o tecido ou muito suscetível à dissolução.
As vitrocerâmicas, tais como o Bioglass cristalizado ou as formas Ceravital, são produzidas como resultado da cristalização controlada do vidro. Durante a produção, o material é submetido a uma sequência de tratamentos térmicos, que levam à formação de um grande número de minúsculos cristalitos (com diâmetros de uma fração de micrómetro) distribuídos uniformemente por todo o volume. Como resultado, as vitrocerâmicas combinam alta densidade, alta resistência, boa resistência a riscos e propriedades térmicas adequadas. Uma composição cuidadosamente selecionada permite que a bioatividade seja mantida, melhorando os parâmetros mecânicos em comparação com o vidro puramente amorfo.
Apesar destas vantagens, o vidro bioativo e a cerâmica de vidro continuam a ser materiais relativamente frágeis. A sua resistência à tração, embora tenha melhorado, ainda é muito baixa para serem usados como componentes independentes em implantes grandes que suportam carga, como hastes de próteses articulares. No entanto, são amplamente usados como revestimentos em implantes metálicos, onde formam uma ligação direta com o osso, e como enchimentos em compósitos dentários, materiais para reconstrução do ouvido médio e pequenos implantes cranianos.
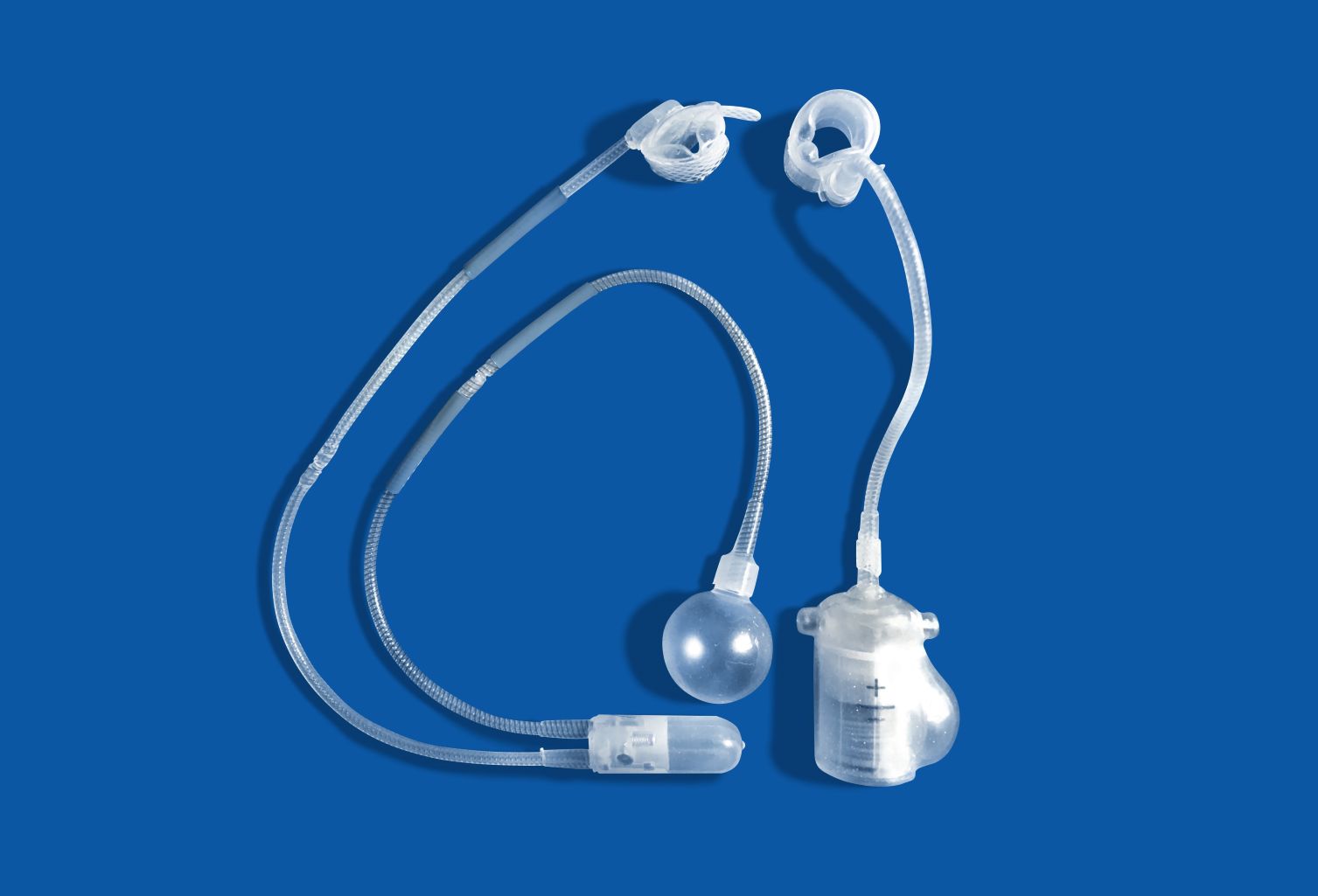
Deterioração e desgaste da cerâmica no corpo
No processo de criação de implantes cerâmicos, é importante considerar não só as propriedades do material imediatamente após a fabricação, mas também as alterações verificadas nas suas propriedades ao longo do tempo sob a influência do ambiente biológico e das cargas mecânicas.
Em cerâmicas não absorventes, a fadiga estática e dinâmica desempenha um papel significativo. Em ambiente aquático, que corresponde às condições fisiológicas, a água pode acelerar o crescimento de microfissuras existentes. Se o material contiver aditivos que facilitam a penetração da água, pode verificar-se uma redução gradual da resistência sob carga prolongada, mesmo que as tensões sejam inferiores ao limite de resistência determinado num ensaio de curta duração. Este fenómeno foi estudado em detalhe no óxido de alumínio, entre outros materiais, observando-se a relação entre a presença de vestígios da ação da água na superfície de fratura e a diminuição da resistência.
Modelos estatísticos de resistência, como a distribuição de Weibull, são frequentemente utilizados para descrever o comportamento da cerâmica, em que a probabilidade de falha depende de um parâmetro constante de escala e forma m. Quanto maior for o valor do parâmetro m, menor a dispersão da resistência e maior a previsibilidade do comportamento do material, o que é fundamental na criação de componentes de implantes. Os testes de prova, nos quais os componentes acabados são submetidos a tensões superiores às cargas operacionais esperadas, também são uma ferramenta prática de engenharia de fiabilidade. As amostras mais fracas são destruídas durante os testes e, para as restantes, é possível determinar a vida útil mínima esperada num determinado nível de carga.
No caso de revestimentos de carbono em metais, os testes de fadiga demonstraram que a integridade do revestimento depende fortemente do comportamento do substrato. Se o substrato metálico não sofrer deformação plástica significativa, o carbono pirolítico pode permanecer intacto mesmo com um número muito elevado de ciclos de carga, o que é particularmente importante para válvulas cardíacas revestidas ou próteses vasculares.
Técnicas de fabrico de biocerâmica
A escolha da técnica de fabrico de biocerâmica depende em grande parte da utilização pretendida do implante. Se o objetivo for substituir tecido duro e transferir cargas mecânicas, a prioridade é existir alta densidade, alta resistência e um módulo de elasticidade adequado. Em aplicações onde a integração do tecido e a vascularização intensiva são mais importantes, a alta porosidade aberta e a distribuição correta do tamanho dos poros desempenham um papel fundamental.
Os implantes de suporte utilizam técnicas como moldagem por injeção, moldagem em gel e métodos de microemulsão, que permitem atingir alta densidade (acima de 97% a 99% da densidade teórica) com porosidade relativamente baixa. Aditivos adequadamente selecionados, incluindo fosfatos de sódio, lítio ou zircónia parcialmente estabilizada, podem melhorar a sinterabilidade, aumentar a microdureza e a resistência à fratura e influenciar o desenvolvimento da microestrutura durante a sinterização. Deve ter-se sempre em mente que o excesso de aditivos ou sua seleção inadequada pode dar origem à formação de fases não biocompatíveis ou excessivamente solúveis.
Se o objetivo é uma rápida integração com os ossos e outros tecidos, as cerâmicas são criadas para ter alta porosidade aberta, com poros que possuam um diâmetro que permita a penetração de vasos sanguíneos e células (geralmente pelo menos várias dezenas de micrómetros). Aqui, entre outros aspetos, é utilizado o método de consolidação do amido, no qual os grânulos de amido são misturados com uma suspensão cerâmica e, em seguida, incham durante a secagem. Durante a sinterização, o amido queima, deixando poros no seu lugar. Ao ajustar a proporção de amido na mistura, é possível controlar com precisão a porosidade final e a distribuição do tamanho dos poros, obtendo estruturas com poros que variam de alguns micrómetros a dezenas de micrómetros.
Outra técnica é a moldagem por gotejamento, na qual se verifica a formação de gotas ou grânulos a partir de uma suspensão de hidroxiapatita, por exemplo, gotejando-os em moldes especiais ou em nitrogénio líquido. Após secagem, calcinação e sinterização, obtêm-se grânulos porosos de HA, que podem ser usados como preenchimentos para defeitos ósseos. Independentemente dos detalhes do processo, o objetivo é criar uma estrutura que seja suficientemente forte para resistir à implantação e à fase inicial de cicatrização, ao mesmo tempo que proporciona um alto grau de penetração nos tecidos.
Resumo – A cerâmica como material biomédico
Atualmente, as biocerâmicas são um dos principais grupos de biomateriais utilizados na medicina. Estes materiais incluem cerâmicas de óxido relativamente bioinertes, como alumina e zircónia, assim como fosfatos de cálcio reabsorvíveis, estruturas à base de coral, sistemas multicomponentes contendo zinco ou ferro e vidros e vitrocerâmicas bioativas. Cada um destes materiais tem o seu próprio «papel» a desempenhar no corpo: alguns destinam-se a ser substitutos ósseos estáveis e duradouros, outros a substituir gradualmente novos tecidos e outros ainda a fornecer uma forte âncora química para implantes ósseos.
A essência da criação de biocerâmicas é compreender a relação entre composição química, estrutura cristalina, microestrutura, método de fabricação e comportamento em um ambiente biológico. Os implantes modernos combinam frequentemente diferentes materiais: metal para suportar cargas, cerâmicas bioativas para uma ligação duradoura com o osso, estruturas reabsorvíveis para promover a regeneração e revestimentos de carbono em componentes que entram em contacto com o sangue. As biocerâmicas já não são apenas um «material duro». Atualmente, são uma ferramenta concebida com precisão para a engenharia de tecidos e a implantologia, permitindo uma imitação cada vez melhor das funções biológicas e da estrutura dos tecidos do corpo.