Biomateriales metálicos

Índice
Los metales desempeñan un papel completamente diferente en la ingeniería biomédica que la cerámica o los polímeros. Se distinguen, principalmente, por sus excelentes propiedades mecánicas y su alta conductividad eléctrica y térmica. Esto se debe a la naturaleza del enlace metálico: algunos de los electrones se deslocalizan y forman una nube de «electrones libres» que son los responsables de la conductividad y del fuerte enlace, aunque no direccional, entre los iones metálicos. Esta estructura permite que los átomos de la red cristalina se muevan entre sí sin alterar el orden, lo que da como resultado la plasticidad característica de los metales y la capacidad de sufrir grandes deformaciones sin padecer una destrucción repentina.
Esta característica se utiliza de forma muy consciente en los biomateriales. Los metales sirven tanto como sustitutos pasivos de tejidos duros (en prótesis de cadera y rodilla, placas óseas, tornillos, clavos intramedulares e implantes dentales) como materiales para dispositivos más «activos», como stents vasculares, guías de catéteres, alambres de ortodoncia e implantes cocleares. En estas aplicaciones, no solo cuenta la resistencia, sino también la conformabilidad, la elasticidad, la conductividad y la susceptibilidad a la fabricación de precisión.
La historia de los biomateriales metálicos comenzó con las aleaciones de acero. La primera aleación desarrollada específicamente para aplicaciones ortopédicas fue el acero al vanadio, utilizado para fabricar placas y tornillos para la fijación de fracturas (conocidas como placas Sherman). Con el tiempo, los aceros inoxidables y, más tarde, las aleaciones de cobalto y cromo y las aleaciones de titanio los sustituyeron. Estas aleaciones utilizan varios metales: hierro (Fe), cromo (Cr), cobalto (Co), níquel (Ni), titanio (Ti), tantalio (Ta), niobio (Nb), molibdeno (Mo) y tungsteno (W) que, en grandes dosis, son tóxicos para el organismo, pero que, en forma de aleaciones estables y resistentes a la corrosión, se toleran bien.
El principal reto en el uso de metales es la corrosión en el entorno in vivo. Los productos de la corrosión pueden provocar tanto el debilitamiento del propio implante como reacciones biológicas adversas. Por ejemplo, inflamación local, decoloración de los tejidos, daños en los órganos o respuestas inmunitarias. Por lo tanto, la ingeniería moderna de biomateriales metálicos se centra en aleaciones capaces de formar capas protectoras duraderas y pasivas en la superficie y en la modificación consciente de la superficie para combinar una buena solidez, una alta resistencia a la corrosión y una respuesta biológica adecuada.
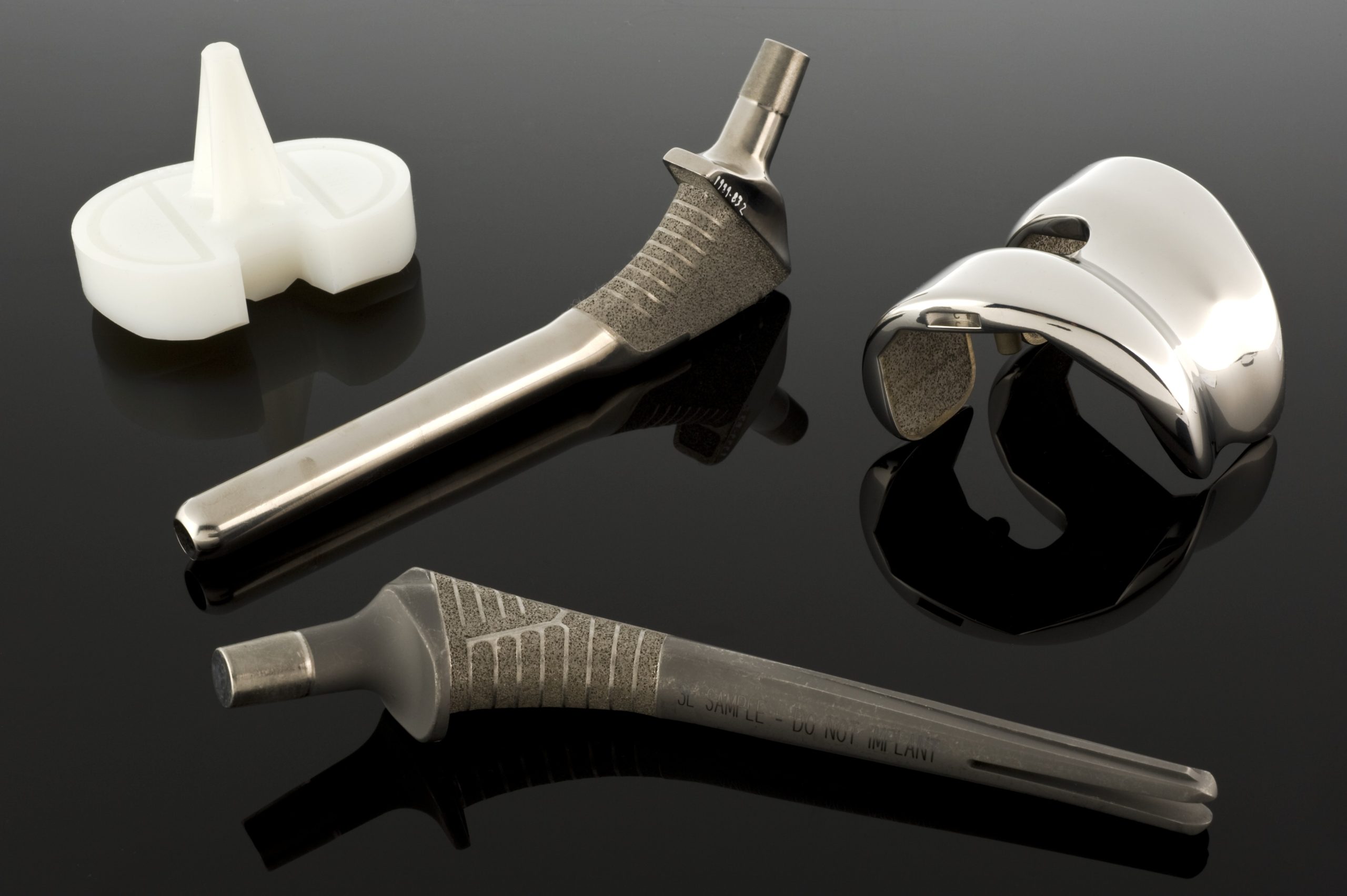
Aceros inoxidables como materiales para implantes
El acero inoxidable fue uno de los primeros materiales que sustituyó con éxito al acero al vanadio en los implantes. Inicialmente, se utilizó acero 18‑8 (tipo 302), que contiene aproximadamente un 18 % de cromo y un 8 % de níquel y posee una resistencia a la corrosión significativamente mejor que los aceros al carbono clásicos. Con el tiempo, apareció una variante del 18‑8 con la adición de molibdeno (18‑8sMo), conocida hoy en día como acero 316, seguida de una modificación con un contenido reducido de carbono: el acero 316L. La reducción del contenido de carbono de, aproximadamente, un 0,08 % a un máximo del 0,03 % disminuye la tendencia a la formación de carburos de cromo en los límites de grano, lo que mejora la resistencia a la corrosión en entornos ricos en cloruros, como los fluidos corporales.
El cromo es el principal responsable de la resistencia a la corrosión de los aceros inoxidables. Incluso con un contenido de Cr del 11 %, se forma una fina capa protectora de óxido en la superficie, lo que confiere al acero el denominado estado pasivo. La adición de molibdeno aumenta la resistencia a la corrosión por picaduras en entornos clorados, lo que hace que los aceros 316/316L sean más adecuados para condiciones fisiológicas. El níquel, a su vez, estabiliza la fase austenítica (estructura γ, fcc) a temperatura ambiente, lo que hace que el material sea no magnético y mejora su resistencia a la corrosión.
Los aceros austeníticos no pueden endurecerse mediante tratamientos térmicos convencionales, pero responden muy bien al endurecimiento por deformación. Esto permite ajustar una amplia gama de propiedades mecánicas, desde estructuras más dúctiles y blandas hasta otras significativamente endurecidas con una alta resistencia a la tracción. Los datos mecánicos del acero 316L muestran que, dependiendo del grado de deformación en frío, se pueden conseguir diferentes combinaciones de resistencia y ductilidad, lo cual es importante para adaptar el material a la función específica del implante.
A pesar de sus numerosas ventajas, los aceros 316 y 316L no son los materiales ideales. En condiciones de alta tensión, especialmente, en zonas con acceso limitado al oxígeno, como alrededor de las roscas de los tornillos o las conexiones de las placas óseas, puede producirse corrosión por hendiduras y por picaduras y, a largo plazo, también puede producirse corrosión por fatiga. Por este motivo, los aceros inoxidables se utilizan más comúnmente en implantes temporales, como placas, tornillos, clavos y alambres de fijación, que pueden retirarse una vez que el hueso se ha curado. Para mejorar sus propiedades, se utilizan ampliamente modificaciones superficiales, desde el pulido y la pasivación en ácido nítrico hasta el anodizado o la implantación de nitrógeno por descarga luminiscente, lo que aumenta la resistencia a la corrosión, el desgaste y la fatiga.
Aleaciones de cobalto y cromo
Cuando los requisitos mecánicos superan las capacidades de los aceros inoxidables, entran en juego las aleaciones de cobalto y cromo. Existen dos grupos principales de aleaciones de este tipo en los biomateriales: la aleación CoCrMo fundida, utilizada, entre otras cosas, en copas y cabezas de endoprótesis, y la aleación CoNiCrMo forjada, utilizada en componentes de alta carga, como los vástagos de prótesis de cadera o rodilla. Las normas ASTM describen varias versiones de estos materiales (F75, F90, F562, F563), pero en la práctica clínica, predominan el CoCrMo y el CoNiCrMo.
El cobalto y el cromo forman una solución sólida de hasta aproximadamente un 65 % de Co. La adición de molibdeno provoca un refinamiento del grano y, como resultado, un aumento de la resistencia tras la fundición o forja. El cromo desempeña una doble función: aumenta la resistencia a la corrosión al formar una capa de óxido pasiva y participa en el endurecimiento de la solución. En la práctica clínica, las aleaciones de Co‑Cr se caracterizan por tener un módulo de elasticidad muy alto, en el rango de 220‑234 GPa, superior al de los aceros inoxidables, y una muy buena resistencia al desgaste.
Sin embargo, esta alta rigidez tiene sus consecuencias. Un implante demasiado rígido puede soportar demasiada carga, lo que provoca un efecto de blindaje a la tensión, es decir, una reducción de la carga sobre el hueso del paciente y su reabsorción gradual. Aunque la importancia clínica de este efecto no está del todo clara, es un factor importante en el diseño y la forma de los vástagos protésicos. Por otro lado, la dureza y la resistencia a la abrasión hacen que las aleaciones de cobalto y cromo sean una excelente opción para los pares de fricción «metal‑metal», en los que es fundamental minimizar el desgaste a largo plazo. Los estudios sobre endoprótesis a largo plazo con estos pares indican una tasa de desgaste lineal muy baja, del orden de unos pocos micrómetros al año.
Otra cuestión importante es la liberación de iones de las aleaciones de Co‑Cr y su posible toxicidad. Los experimentos realizados con solución de Ringer han demostrado que la tasa de liberación de níquel de la aleación CoNiCrMo y del acero 316L es muy similar tras un determinado periodo de tiempo, a pesar de que la aleación de cobalto contiene aproximadamente tres veces más níquel. Estudios in vitro han demostrado que las partículas de cobalto pueden ser tóxicas para las células que forman los huesos, mientras que las partículas de cromo y aleación de Co‑Cr se toleran mucho mejor. Las altas concentraciones de extractos de iones de Co y Ni alteran claramente el metabolismo celular en los cultivos, mientras que los iones de cromo muestran una toxicidad menor.
El titanio y sus aleaciones
Entre los metales utilizados como biomateriales, el titanio ocupa una posición especial. En la serie electroquímica, es un elemento «activo», pero en un entorno fisiológico, está recubierto por una capa de óxido pasiva muy estable gracias a la cual su corriente de corrosión en soluciones fisiológicas es extremadamente baja, del orden de 10⁻⁸ A/cm². En la práctica, los implantes de titanio permanecen visualmente inalterados tras un largo periodo de tiempo en el cuerpo.
El titanio puro (cp-Ti) y la aleación más popular Ti–6Al–4V combinan una muy buena resistencia a la corrosión con una relación resistencia‑peso favorable. Su módulo de elasticidad es inferior al del acero o las aleaciones de Co‑Cr, lo que los acerca más al hueso y reduce, potencialmente, el riesgo de blindaje a la tensión. Por otro lado, el titanio no es tan rígido ni tan resistente a la tensión como los mejores aceros o aleaciones de cobalto, por lo que el diseño de los elementos que soportan carga requiere un análisis preciso de las tensiones y, a menudo, una sección transversal más grande.
En las últimas décadas, también se han desarrollado aleaciones de titanio con un módulo de elasticidad reducido y una mayor resistencia a la corrosión, que contienen, entre otros, Nb y Zr. Por ejemplo, Ti-13Nb-13Zr, diseñadas específicamente para prótesis articulares. Además, se ha desarrollado el endurecimiento superficial de las aleaciones de Ti (por ejemplo, tratamiento termoquímico, nitruración, etc.), lo que permite combinar la buena biocompatibilidad del sustrato con una alta resistencia al desgaste en las zonas de fricción.
Las aleaciones de níquel‑titanio (NiTi), que presentan memoria de forma y superelasticidad, constituyen un grupo especial. Gracias a la transformación martensítica, pueden reproducir una forma previamente registrada cuando se calientan por encima de la temperatura de transformación o presentar una deformabilidad elástica muy alta en un rango de tensión estrecho. Esta característica se utiliza, entre otras cosas, en stents vasculares, arcos ortodónticos y guías de catéteres, lo que permite la inserción atraumática de los dispositivos y su expansión estable tras la dilatación.
En el caso del titanio, las propiedades de la superficie son especialmente importantes. Los estudios demuestran que tanto la rugosidad como la química de la superficie regulan el comportamiento de los osteoblastos y las células formadoras de hueso, ya que afectan a la adhesión, la proliferación y la producción de factores de crecimiento y citocinas. El tratamiento químico adecuado de la superficie del titanio y sus aleaciones puede hacerlas bioactivas. Es decir, las hace capaces de formar una capa de apatita en contacto con los fluidos corporales, lo que favorece la unión directa con el hueso.

Metales en odontología y otras aplicaciones especiales
Tanto los metales preciosos como los metales básicos se utilizan en odontología. El oro es prácticamente resistente a la corrosión (resistencia de tipo inmune) y proporciona una excelente durabilidad y estabilidad química en las reconstrucciones protésicas. Sin embargo, sus limitaciones son su alta densidad, su resistencia insuficiente para cargas pesadas y su coste, lo que significa que, prácticamente, no se utiliza en ortopedia.
La amalgama dental, una aleación de plata, estaño y mercurio, se utiliza habitualmente. Aunque las fases individuales de este material son pasivas a pH neutro, en la práctica, la amalgama a menudo se corroe, especialmente, en presencia de diferencias de aireación bajo la placa bacteriana y las microcélulas galvánicas locales. De hecho, es el material más propenso a la corrosión que se utiliza en odontología, lo que se manifiesta en la decoloración y la formación de productos de corrosión en la superficie de los empastes.
El grupo de metales especiales también incluye los metales del platino y sus aleaciones, utilizados cuando la resistencia química y el control de la conductividad son cruciales, así como las aleaciones de Ni‑Cu y otros sistemas utilizados en hipertermia, el calentamiento deliberado de tejidos cancerosos mediante un campo magnético inducido. Este tipo de aleaciones están diseñadas para que su respuesta térmica en un campo electromagnético esté bien controlada, lo que permite suministrar energía térmica al tumor con precisión.
La corrosión de implantes metálicos en un entorno biológico
La corrosión es un fenómeno fundamental en los biomateriales metálicos. En el cuerpo, nos encontramos con un fluido electrolítico que contiene iones (Na⁺, Cl⁻, HCO₃⁻ y fosfatos), un pH variable y diferencias de potencial entre distintas zonas. Es decir, factores que favorecen la aparición de reacciones electroquímicas.
Los diagramas de Pourbaix, que muestran la relación entre el potencial electroquímico y el pH, se utilizan para describir la estabilidad de los metales. Distinguen entre áreas de corrosión (actividad), pasividad e inmunidad. En el cuerpo humano, los diferentes fluidos tienen diferentes niveles de pH y oxigenación: el fluido tisular suele tener un pH de alrededor de 7,4, pero en las proximidades de una herida puede descender hasta 3,5, y en una herida infectada puede ascender hasta 9,0. Esto significa que un metal que funciona bien en una zona del cuerpo puede corroerse en otra.
Sin embargo, los diagramas de Pourbaix tienen limitaciones, ya que se basan en estados de equilibrio en un sistema simple de metal‑agua‑productos de reacción. La presencia de iones cloruro o moléculas orgánicas complejas puede alterar significativamente el comportamiento del metal, y la pasividad prevista puede resultar, en la práctica, demasiado optimista. Por lo tanto, además de estos diagramas, se utilizan curvas de polarización que permiten determinar la corriente de corrosión y, sobre esta base, calcular el número de iones liberados en los tejidos y la tasa de pérdida de material. Alternativamente, se mide la pérdida de masa de la muestra durante la exposición en una solución similar al fluido corporal.
La corrosión de los materiales de los implantes puede adoptar diversas formas. La corrosión uniforme provoca una pérdida de material relativamente homogénea, pero las formas localizadas son mucho más peligrosas. La corrosión por picaduras provoca pérdidas profundas y localizadas; los aceros inoxidables son especialmente susceptibles a este tipo de corrosión en presencia de cloruros. La corrosión por hendiduras se produce en zonas con acceso limitado al oxígeno, como los espacios entre el tornillo y la placa, donde las condiciones químicas locales (pH, concentración de iones, etc.) difieren significativamente del entorno circundante. La corrosión por fricción es una corrosión asociada a los micromovimientos de dos superficies en contacto: la abrasión mecánica destruye la capa pasiva, deja al descubierto el metal fresco y acelera la corrosión.
La corrosión por tensión y la corrosión por fatiga son formas especiales de corrosión. En presencia de tensiones mecánicas, especialmente las repetitivas, la velocidad de corrosión puede aumentar y las microfisuras pueden propagarse más rápidamente. En los implantes de acero inoxidable, por ejemplo, se han observado fracturas de clavos y pernos de cadera en los que se daban simultáneamente cargas de flexión y un entorno fisiológico agresivo. En tales casos, es difícil hablar de corrosión «pura», ya que siempre se trata de una interacción dinámica entre la química, la mecánica y la microestructura.
Los diferentes metales se comportan de manera diferente en este sentido. Los metales preciosos, como el oro, son prácticamente resistentes a la corrosión: su potencial electroquímico estándar es positivo y, en los diagramas de Pourbaix, ocupan el área de inmunidad. El titanio y las aleaciones de Co‑Cr se basan en la pasividad: forman una capa de óxido bien adherida y hermética gracias a la cual sus corrientes de corrosión son muy bajas y la superficie permanece estable. Los aceros inoxidables también se benefician de la pasividad del cromo, pero su capa pasiva es menos estable, lo que los hace más susceptibles a la corrosión por picaduras y hendiduras. La amalgama dental, por otro lado, aunque es termodinámicamente parcialmente pasiva, es en la práctica un material muy susceptible a la corrosión, especialmente en presencia de biofilm.
Fabricación y procesamiento de implantes metálicos
La fabricación de implantes metálicos no solo consiste en darles forma, sino también en controlar la microestructura y el estado de la superficie que determinan la resistencia a la fatiga, la resistencia a la corrosión y la respuesta biológica.
En el caso de los aceros inoxidables, es fundamental que los aceros austeníticos se endurezcan muy rápidamente bajo compresión. Esto significa que durante el trabajo en frío (laminado, estirado o doblado), su resistencia aumenta pero, al mismo tiempo, disminuye su plasticidad. Para restaurar el nivel de deformabilidad requerido, se utiliza un recocido intermedio en el que deben evitarse las temperaturas y los tiempos que favorecen la precipitación de carburos de cromo en los límites de grano, lo que debilita la resistencia a la corrosión. Después del conformado, los componentes se limpian, desoxidan (químicamente o por abrasión) y pasivan, normalmente, en una solución de ácido nítrico de acuerdo con la norma ASTM F86.
Las aleaciones de Co‑Cr se comportan de manera diferente: son muy susceptibles al endurecimiento durante la deformación, lo que en muchos casos dificulta el forjado convencional. Por lo tanto, los componentes con geometrías complejas, como las cabezas y copas protésicas, se fabrican a menudo mediante la fundición de precisión (el llamado método de la cera perdida). El proceso consiste en preparar un modelo de cera preciso, cubrirlo con material refractario, quemar la cera y verter aleación líquida de Co‑CrMo en el molde a alta temperatura. La temperatura del molde y el tiempo de enfriamiento afectan al tamaño del grano y al tamaño y la distribución de los carburos: una microestructura fina aumenta la solidez, pero puede reducir la resistencia a la fractura frágil, mientras que los granos y carburos más grandes mejoran la ductilidad a expensas de la solidez. Por lo tanto, el diseñador debe encontrar un equilibrio entre la resistencia y la resistencia a la fractura.
En el caso de las aleaciones de titanio, los procesos de fundición, forja y tratamiento térmico, así como el tratamiento superficial, son fundamentales. El titanio requiere una atmósfera protectora durante el procesamiento a alta temperatura, ya que reacciona fácilmente con el oxígeno y el nitrógeno para formar capas superficiales frágiles. Tras el procesamiento mecánico inicial, las superficies de los implantes de titanio se someten a un chorro de arena, se graban con ácido, se anodizan o se combina varios de estos procesos, lo que da como resultado una rugosidad micrométrica favorable y una capa de óxido modificada. Los estudios indican que las superficies preparadas de esta manera favorecen un crecimiento óseo más rápido y la formación de una unión mecánica fuerte y, potencialmente, química.
Los procesos de fabricación de aleaciones con memoria de forma constituyen una categoría aparte. En su caso, es fundamental controlar con precisión la composición química y el tratamiento térmico, que determinan las temperaturas de transformación martensítica y el rango de superelasticidad. Los stents de NiTi o los arcos ortodónticos deben alcanzar la deformación deseada y recuperar su forma dentro de un rango de temperatura estrictamente definido, incluidas las condiciones fisiológicas.
Resumen: biomateriales metálicos
Los biomateriales metálicos forman una amplia familia en la que cada material ocupa su propio nicho funcional, definido con bastante precisión. Los aceros inoxidables, especialmente el tipo 316L, son materiales relativamente económicos y fáciles de procesar, con buenas propiedades mecánicas y suficiente resistencia a la corrosión, por lo que se utilizan principalmente en implantes temporales y componentes menos críticos. Las aleaciones de cobalto‑cromo ofrecen una solidez, dureza y resistencia al desgaste muy elevadas, lo que las convierte en el material ideal para copas y cabezales protésicos, así como para vástagos, donde es importante la durabilidad bajo cargas pesadas. El titanio y sus aleaciones, que combinan una muy buena resistencia a la corrosión, un módulo de elasticidad favorable y una alta biocompatibilidad, se han convertido en el «estándar de oro» para los implantes a largo plazo, especialmente en ortopedia e implantología dental.
Las aleaciones especiales, como el NiTi con memoria de forma, también desempeñan un papel importante, ya que permiten aplicar estrategias terapéuticas completamente nuevas, desde stents autoexpandibles hasta arcos ortodónticos superelásticos. El oro y las amalgamas siguen siendo importantes en odontología, aunque sus aplicaciones se están revisando a la luz de los requisitos estéticos y de seguridad.
El denominador común de todos los biomateriales metálicos es la necesidad de controlar la corrosión y la interacción con los tejidos. Los diagramas de Pourbaix, las curvas de polarización, los ensayos de fatiga y los estudios de toxicidad iónica constituyen la base para el diseño técnico de estos materiales. La ingeniería de superficies es igualmente importante, ya que determina la calidad de la capa pasiva, la resistencia al desgaste, la adhesión celular y la naturaleza de la unión con el hueso.
Como resultado, la ingeniería moderna de biomateriales no considera los metales de forma aislada, sino que los trata como parte de sistemas complejos: un núcleo metálico puede recubrirse con cerámica bioactiva, rodearse de un compuesto polimérico o combinarse con estructuras cerámicas porosas que favorezcan la regeneración. Los metales proporcionan capacidad de carga y plasticidad, las cerámicas aportan bioactividad y resistencia a la abrasión, y los polímeros proporcionan flexibilidad y la capacidad de formar estructuras blandas. Juntos, constituyen la base de la implantología moderna, cuyo objetivo ya no es solo «sustituir piezas», sino lograr una reconstrucción funcional y biológicamente integrada de los órganos.




