Pourquoi la surface d’un implant est-elle si importante ?
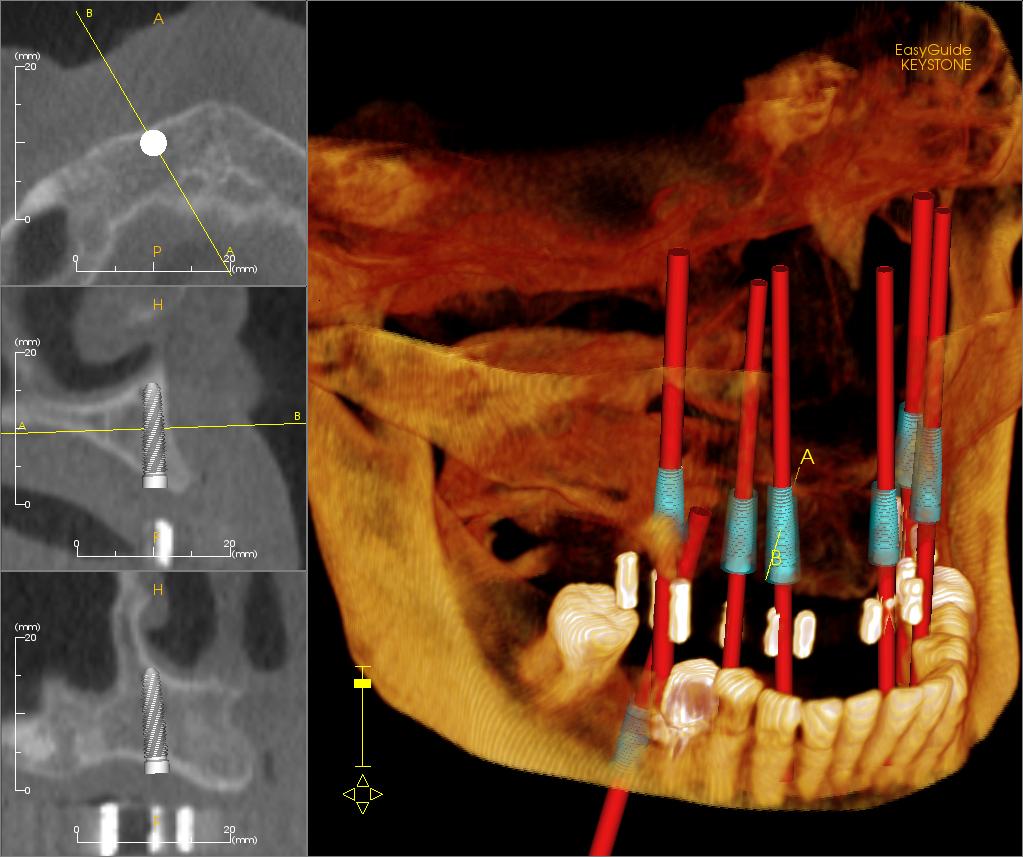
En ingénierie des biomatériaux, la tendance à ne se fier qu’à l’intuition issue de la science des matériaux traditionnelle est assez répandue, puisqu’un implant doit résister aux contraintes, ne pas se corroder, ne pas s’user excessivement et être fonctionnel durant des années… Ce succès devrait donc dépendre principalement du matériau « de l’intérieur ». Toutefois, ce n’est qu’une partie de la vérité. Le matériau de base est, en effet, responsable de la résistance, de la rigidité, de l’élasticité, de la durabilité et de la perméabilité. Cependant, du point de vue de l’organisme, le premier contact, qui est le plus important, ne se fait pas avec l’ensemble du matériau, mais avec sa couche externe. C’est cette couche qui entre en contact avec le sang, les protéines, les cellules et autres fluides corporels. En pratique, cela signifie qu’un implant peut être effectivement très performant sur le plan mécanique, mais il peut poser de graves problèmes sur le plan biologique si sa surface envoie un « mauvais signal » aux tissus.
Cette observation modifie notre façon d’envisager la conception des implants. Au lieu de nous demander uniquement « de quoi l’implant doit-il être fait ? », nous devons nous interroger sur ce à quoi la surface de l’implant doit ressembler. En matière de biomatériaux, la réponse biologique ne peut donc être qu’une question de composition chimique de l’ensemble du composant. La réponse se situe à l’interface matériau-tissu, à l’observation de ce qui s’y passe, à la chimie de surface, à la mouillabilité, à la charge, à la rugosité, à l’organisation et à la réactivité. C’est pourquoi le succès d’un implant est si souvent déterminé non par le « volume » du matériau, mais très précisément au niveau de la frontière de phase.
Cet article s’appuie sur Biomaterials Science: An Introduction to Materials in Medicine, éd. William R. Wagner et al., 4ᵉ éd., 2020. Le contenu suivant est un aperçu général du sujet. Nous recommandons aux personnes intéressées par celui-ci de se plonger dans la littérature spécialisée.
Comment le corps réagit-il à la surface d’un matériau ?
Le point de départ le plus important est simple. Le corps ne « voit » pas l’implant dans son ensemble et d’un seul coup. Il « lit » d’abord sa surface. Les auteurs de Biomaterials Science affirment explicitement que pour les matériaux qui ne libèrent pas de substances indésirables, le transfert d’informations du matériau vers les protéines, les cellules et l’ensemble du corps se fait par le biais de la structure de surface. Le corps réagit donc à la chimie et à l’organisation, toutes deux spécifiques de la couche externe, plutôt qu’aux propriétés moyennes/générales de l’ensemble du matériau. Ce changement d’accent, apparemment mineur, revêt toutefois une importance pratique considérable, car il fait passer la question de la biocompatibilité du niveau de « quel type d’alliage ou de polymère avons-nous ? » à celui de « comment son interface se présente et se comporte ? ».
Il est donc très important de garder à l’esprit que la surface n’est pas simplement qu’une fine couche du matériau qui se comporte de la même manière que son intérieur. Cet ouvrage souligne que la surface est une zone de réactivité particulière et elle diffère presque inévitablement du reste du matériau. Pour un véritable matériau métallique, la couche externe peut comprendre, outre de l’oxyde métallique, également de l’eau adsorbée, des composés organiques polaires ou bien des contaminants hydrocarbonés. Pour les polymères, cette zone superficielle si unique peut s’observer sur environ 10 à 100 nm. Cette notion est très importante, car cela signifie que même si le matériau « en masse » est homogène, sa partie biologiquement active peut se trouver être chimiquement et structurellement complexe.
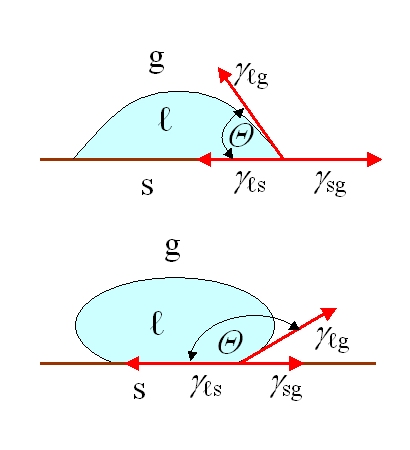
D’un point de vue biologique, la surface est loin de n’être qu’une question de composition chimique. Nous pouvons énumérer de nombreuses caractéristiques qui peuvent influencer les réponses biologiques, tels que rugosité, motifs et topographie, mouillabilité, mobilité de surface, composition chimique, charge électrique, cristallinité, module d’élasticité et hétérogénéité.
Dans le même temps, les auteurs notent, en toute honnêteté, qu’il n’est pas encore possible d’identifier une seule caractéristique universelle qui se dégagerait comme étant la plus importante pour toutes les réponses biologiques. Dans la pratique, il s’agit d’une action très axée sur l’ingénierie, dans la mesure où il ne faut pas fonder une conception particulière qui ne soit basée que sur un slogan paramétrique unique, tel que « augmentons la rugosité » ou bien « rendons la surface plus hydrophile », car la réponse de l’organisme résulte, quant à elle, de l’interaction simultanée de plusieurs caractéristiques.
Cette approche explique pourquoi deux implants fabriqués à partir du même matériau de base peuvent se comporter différemment sur un plan biologique. Un simple changement dans le traitement, la stérilisation, le stockage ou l’emballage suffit aussi à modifier l’état de la surface ! Il est même possible de mettre en évidence des problèmes aussi banals que des empreintes digitales, des additifs qui ont migré depuis l’emballage ou bien de contaminants provenant du papier ou du film ayant servi à l’envelopper.
En laboratoire, il s’agit d’un détail, mais dans la réalité, ce sont précisément ces détails qui peuvent amener à tester une surface qui, finalement, n’est pas celle réellement présente sur l’implant qui sera utilisé en clinique.

Comment la surface se traduit-elle, en biocompatibilité ?
Si la surface est le principal moyen de communication entre l’implant et le corps, nous devons nous demander à quoi ressemble ce dialogue ! L’un des mécanismes clés est l’adsorption des protéines. Nous pouvons souligner ici qu’après l’implantation d’un biomatériau synthétique, des protéines adhésives s’adsorbent très rapidement sur sa surface, en quelques secondes. C’est de cette manière qu’un matériau qui, en soi, ne possède pas de motifs de reconnaissance biologique, devient « lisible » pour le corps. En d’autres termes, les cellules ne réagissent pas souvent directement au matériau pur, mais à la couche de protéines qui se forme à sa surface, peu après le contact avec le corps.
Ceci a une implication fondamentale pour la compréhension de la biocompatibilité. Celle-ci ne se limite absolument pas à de l’absence de toxicité aiguë. En revanche, elle désigne la capacité du matériau à susciter une réponse appropriée de l’hôte, dans une application spécifique. Cette « réponse appropriée » peut signifier un aspect pour un stent, un autre aspect pour un implant orthopédique, ou encore un autre pour un cathéter. Dans chacun de ces cas, la surface contrôle les événements biologiques initiaux, quelles protéines vont s’adsorber, dans quelle configuration, quels récepteurs cellulaires seront stimulés, et si le signal va mener à l’intégration tissulaire, à l’activation plaquettaire, à la formation d’un biofilm ou bien à une réaction de rejet.
Un bon exemple est la comparaison entre les protéines d’adhésion et les protéines de passivation. Nous pouvons décrire comment le pré-revêtement d’une surface par de la fibronectine augmente l’adhésion de nombreuses cellules, tandis que l’albumine peut la limiter. Nous ne pouvons pas considérer ceci comme étant une curiosité issue de la culture cellulaire, mais bien d’un modèle de ce qui se passe sur les implants. La surface n’est jamais une toile de fond neutre, finalement, car c’est elle qui définit les conditions initiales de la réponse cellulaire qui s’ensuit.
En pratique, les deux surfaces présentant une résistance mécanique similaire peuvent conduire à des trajectoires de cicatrisation complètement différentes, simplement parce qu’elles établissent différemment la première couche de protéines adsorbées.
Bien évidemment, les interactions entre la surface et les micro-organismes sont tout aussi importantes. Spécifiquement aux biofilms, nous pouvons mentionner que la mouillabilité, la charge, la rugosité et la topographie influencent l’adhérence bactérienne. La tendance générale veut qu’une plus grande rugosité favorise fréquemment l’adhérence bactérienne, tandis que les surfaces hydrophobes facilitent plus fréquemment la fixation bactérienne.
Toutefois, il n’existe aucune règle sans exceptions, ce qui fait que des systèmes extrêmement superhydrophiles ou superhydrophobes peuvent agir comme des inhibiteurs de biofilm… par un mécanisme différent ! Dans la pratique, cela sert d’avertissement, car c’est une solution bénéfique pour l’intégration tissulaire, mais qui ne sera pas toujours aussi bénéfique dans le cadre du contrôle de la colonisation bactérienne.
Vous trouverez ci-dessous une vidéo, en anglais, intitulée BIOE 5820 Biomaterials Protein Adsorption, qui est un cours sur l’adsorption des protéines sur les surfaces des biomatériaux.
Pourquoi modifier la surface plutôt que l’ensemble du matériau ?
C’est là la principale justification de la modification de surface. Si le matériau en vrac est responsable de la capacité de charge, de la durabilité et de la fonction mécanique, tandis que la surface est responsable de l’interaction biologique, il est plus logique de préserver ce qui fonctionne bien dans le matériau en vrac et de ne modifier que ce qui entre en contact avec les tissus.
C’est précisément ainsi que les modifications physicochimiques de surface nous permettent de formuler les actions à entreprendre, l’objectif étant de préserver les propriétés physiques clés du biomatériau, tout en modifiant uniquement la couche externe afin d’améliorer ou de moduler la réponse biologique à l’interface tissu-dispositif.
Cette approche présente plusieurs avantages, très pratiques. Premièrement, il n’est pas nécessaire d’abandonner un matériau dont nous connaissons bien les propriétés mécaniques et technologiques.
Premièrement, le titane, l’acier, les polymères techniques ou les élastomères peuvent continuer à remplir leur rôle structurel ou fonctionnel.
Deuxièmement, la réponse biologique peut être adaptée plus précisément à une application donnée. Lorsque nous souhaitons une surface différente pour un implant osseux, une autre pour un composant en contact avec le sang, ou encore une autre pour un cathéter, sur laquelle la priorité peut alors être de limiter l’adsorption des protéines ainsi que l’adhérence des cellules ou des bactéries.
Troisièmement, la modification de surface permet d’améliorer un dispositif, sans avoir à repenser complètement l’ensemble de la structure. C’est ainsi que… pour les dispositifs déjà bien établis dans la pratique clinique, c’est un moyen de modifier les bio-interactions sans repenser le produit, sans réorganiser la production, sans devoir former à nouveau le personnel médical à l’utilisation de la solution nouvelle.
Il y a toutefois une condition à tout ceci, qui est qu’il faut distinguer entre une véritable modification de l’interface et un changement purement cosmétique dans la description. La simple déclaration selon laquelle un matériau est « bioactif » ou « anti-salissure » n’a guère de sens si nous ignorons à quoi ressemble réellement la surface, dans sa forme finale, après traitement et stérilisation. Notons aussi que l’échantillon analysé doit correspondre autant que possible au matériau ou au dispositif sous la forme utilisée pour les essais biologiques ou l’implantation. Ceci est très important, car la surface exposée à l’air peut ne pas être la même que celle que le matériau présente dans l’environnement aqueux du corps.
Trois principales méthodes de modification de surface
La première méthode consiste à modifier la surface existante sans ajouter une nouvelle couche distincte. Les atomes, molécules et liaisons déjà présents dans la couche externe du matériau peuvent être transformés chimiquement ou physiquement.
Ce groupe comprend, entre autres, la gravure, l’activation chimique, la rugosité apportée mécaniquement, l’implantation ionique et certains traitements au laser. Loin de « fixer » une nouvelle couche à l’implant, sa propre surface est modelée ou remodelée. Cette approche est avantageuse lorsqu’une forte intégration de la modification avec le substrat est importante, ainsi que pour réduire le risque de délamination et pour modifier des propriétés telles que la réactivité, la mouillabilité, la résistance à la corrosion, la dureté ou la bioactivité. Il est intéressant de mentionner que l’implantation ionique peut améliorer la résistance à l’usure ou à la corrosion, et que le traitement au laser peut modifier de manière contrôlée la rugosité de surface, la cristallinité et la composition chimique.
La seconde approche consiste à appliquer une nouvelle couche ou un nouveau revêtement. Dans ce cas, un matériau de composition ou de propriétés différentes est déposé sur la surface. Il peut s’agir d’un film mince, d’une couche greffée, d’un revêtement polymère ou d’un système présentant une surface anti-encrassement.
Cette stratégie est particulièrement utile lorsque le substrat présente des propriétés mécaniques idéales, mais qu’il est trop « brut », d’un point de vue biologique. Les surfaces résistantes à l’adsorption non spécifique des protéines en sont un bon exemple. Leur mécanisme repose généralement sur une couche d’hydratation forte, qui agit comme une barrière énergétique et physique face aux protéines. Dans un chapitre consacré aux surfaces antisalissantes, les auteurs décrivent deux stratégies principales pour mettre en œuvre de tels systèmes, le « graft-to-surface », le greffage sur surface, où le matériau s’adsorbe ou se lie à partir d’une solution, et le « graft-from-surface », greffage avec lequel des brosses polymères se développent à partir de la surface. La première approche est technologiquement plus simple, et la seconde permet d’atteindre plus facilement une densité de packing/greffage élevée, mais nécessite généralement une chimie et une préparation du substrat qui soient plus complexes.
En pratique, cette différence revêt une importance technique. Si le souhait est de simplement limiter rapidement le dépôt de protéines sur un substrat relativement simple, la solution « de base » peut suffire. Cependant, s’il y a besoin d’une couche anti-adsorption durable, imperméable et dont la densité packée/greffée est optimale, le simple fait de « coller » des molécules à la surface peut ne pas être suffisant.
Il est clairement visible que le choix de la méthode détermine la densité de packing, le nombre de défauts et la durabilité de la surface finale. Cela signifie que les revêtements ne sont pas évalués uniquement sur la base de leur composition chimique déclarée, mais sur leur capacité à former effectivement une interface homogène et stable dans les conditions d’exploitation.
Une troisième approche consiste à créer des motifs, des textures et des topographies. Ici, l’objectif principal n’est pas de modifier la composition chimique, mais d’altérer la géométrie de ce que la cellule ou la protéine « voit ». La topographie de surface influence naturellement l’adhésion, la prolifération, la migration, la différenciation et l’expression génétique des cellules. Ces dernières réagissent à la fois aux caractéristiques à l’échelle micro et nanométrique, et pas uniquement à la simple présence du matériau. Dans les études citées dans l’ouvrage source, la variation des hauteurs, des tailles et des espacements des structures topographiques peut modifier le degré de minéralisation, l’orientation cellulaire, l’adhérence cellulaire et la différenciation. Cela signifie que la texture n’a finalement rien d’un ornement ni d’un effet secondaire du traitement, mais c’est un outil actif qui permet de contrôler les réponses biologiques.
Cela est particulièrement évident dans le cas des implants osseux et dentaires. Nous savons désormais comment une couche superficielle suffisamment rugueuse ou tridimensionnelle peut accélérer les premières étapes de la cicatrisation, favoriser le dépôt de fibrine, la liaison des intégrines et l’interverrouillage micromécanique avec l’os. En conséquence, la résistance au cisaillement à l’interface implant-os augmente et le transfert de charge s’améliore. C’est un excellent exemple qui nous montre que la texturation n’est en aucun cas une « amélioration aveugle », mais bien une tentative de contrôler un mécanisme interfacial spécifique. Il convient toutefois de faire preuve de grande prudence, car la même rugosité qui favorise l’ostéointégration peut, dans une application différente, augmenter le risque de colonisation bactérienne ou entraver le contrôle de la surface.

Erreurs courantes, pièges et fausses pistes
En premier lieu, l’erreur la plus fréquente consiste à assimiler « meilleur matériau » à « meilleure réponse biologique ». Cependant, cette assimilation est bien trop schématique. La résistance mécanique, la résistance à la fatigue et la stabilité chimique n’expliquent pas encore ce qui va se passer au niveau de l’interface tissulaire. En biomatériaux, nous pouvons donc être en présence d’un excellent matériau structurel et d’une interface biologique médiocre. Nous pouvons également être confrontés au problème inverse, qui serait une surface hautement active sur le plan biologique montée sur un substrat qui ne répond pas aux exigences mécaniques. C’est précisément pour cette raison que le postulat selon lequel le matériau confère à l’implant sa résistance, tandis que la surface détermine la réponse de l’organisme, est utile en conception. Il nous oblige à séparer deux questions qui sont malheureusement confondues dans l’ingénierie classique.
Le second écueil est la croyance qu’une seule propriété de surface peut résoudre l’ensemble du problème. En pratique, il n’existe pas de « paramètre universel de biocompatibilité ».
Augmenter l’hydrophilie peut limiter l’adsorption de certaines protéines, mais cela n’améliore pas nécessairement l’intégration tissulaire.
Augmenter la rugosité peut favoriser la réponse ostéoblastique, mais cela peut ne pas être bénéfique dans un environnement présentant un risque d’infection. Notons ici qu’il n’est pas encore connu le fait que tel ou tel paramètre est le plus important, en regard de chaque réponse biologique spécifique attendue, de sorte que les variables doivent être mesurées et corrélées indépendamment.
Il s’agit là d’une directive méthodologique très importante, qui implique que… au lieu de rechercher un seul chiffre magique, il faut établir une carte des relations entre plusieurs propriétés d’interface et un objectif clinique spécifique.
Le troisième écueil concerne l’épaisseur de la modification. Dans le cadre des modifications physico-chimiques, il faut souligner qu’elles doivent être aussi ténues que possible. Dans l’idéal, il devrait suffire de modifier uniquement les quelques couches moléculaires les plus externes, qui sont de l’ordre de quelques nanomètres, bien qu’en pratique, les couches doivent parfois être plus épaisses de manière à garantir l’uniformité et la durabilité. Un revêtement trop épais peut altérer les propriétés mécaniques et fonctionnelles du dispositif, ainsi qu’augmenter le risque de fissuration et de délamination. Ceci est particulièrement important lorsque l’implant est soumis à la fatigue ou au frottement. Donc, une couche qui semble pourtant prometteuse d’un point de vue biologique, mais qui se décolle mécaniquement après un certain temps, ne résout hélas en aucun cas le problème… En fait, elle en crée simplement un nouveau !
La quatrième idée fausse consiste à considérer la surface comme étant un état statique. Nous pouvons démontrer que certains matériaux peuvent inverser l’organisation de leur surface, lors du passage de l’air vers un environnement aqueux. Une surface mesurée « à sec » peut ne pas être la même que celle que les protéines et les cellules vont trouver dans le corps. Ces aspects ont donc des implications directes pour la recherche. Si l’analyse de surface ne tient pas compte de l’environnement d’utilisation, nous risquons d’optimiser un paramètre qui n’aura plus la même valeur ni la même importance après l’implantation.
Lorsqu’une théorie plus avancée s’impose…
Une approche avancée devient nécessaire lorsque des termes aux aspects intuitifs tels que « plus lisse », « plus hydrophile » ou « plus rugueux » ne suffisent plus. Les surfaces anti-encrassement en sont un exemple parfait. Leur fonction ne résulte pas du fait qu’elles sont lisses/glissantes, mais du fait qu’elles forment une couche d’hydratation stable, dont l’élimination est énergétiquement défavorable à l’adsorption des protéines. Ainsi, les matériaux hydrophiles à base de PEG se lient à l’eau par des liaisons hydrogène, tandis que les matériaux zwitterioniques peuvent le faire de manière encore plus puissante par hydratation induite électrostatiquement. À ce niveau, il faut prendre en compte la chimie fonctionnelle, à laquelle s’ajoutent la densité d’empilement des chaînes, la liberté conformationnelle et la stabilité de l’ancrage de la couche.
Une théorie plus avancée est en outre nécessaire lorsque la surface est censée être non interférente, mais aussi chargée de guider activement le comportement cellulaire. Dans de tels cas, ce qui importe est donc la géométrie à l’échelle micro et nanométrique, la mécanique locale, la taille, la hauteur et l’espacement des caractéristiques topographiques, et parfois même l’ordre ou le désordre du motif. C’est précisément pour cette raison que la recherche utilise aujourd’hui des matrices topographiques et des criblages de surface plus systématiques. Ne voyons pas ici la complexité académique du sujet, mais le seul fait que les cellules distinguent véritablement les échelles et les motifs des caractéristiques, et que la réponse biologique cesse d’être une fonction linéaire d’un seul paramètre.
Pourquoi la surface d’un implant est-elle si importante ? – Résumé
En biomatériaux, le succès d’un implant est fréquemment déterminé non par le matériau « en vrac » lui-même, mais par la surface qu’il présente au corps. C’est la surface qui constitue le premier point de contact avec les protéines, les cellules et les fluides corporels, et qui contrôle donc en grande partie la biocompatibilité.
C’est pour cette raison qu’une conception judicieuse de l’implant implique une séparation des fonctions. Ainsi, le volume est destiné à garantir les propriétés mécaniques et la durabilité, tandis que la surface est destinée à susciter la réponse biologique appropriée. C’est là le fondement de toute la logique consistant à modifier la surface sans changer l’ensemble du matériau. Nous pouvons remodeler la couche externe existante, appliquer un nouveau revêtement ou concevoir un motif et une topographie qui vont influencer l’adsorption des protéines, le comportement cellulaire, l’intégration tissulaire ou la résistance à l’encrassement. À cela s’ajoute une condition, qui est que la modification doit être véritablement interfaciale, fine, durable et adaptée à un objectif clinique spécifique. C’est précisément pour cette raison que, dans le domaine des biomatériaux, la surface n’est pas un détail de finition, mais l’un des principaux éléments et outils de la conception des implants.