Sistemas de equilibrio de fases de aleaciones
Índice
En los metales puros, el curso de las transformaciones suele ser fácil de comprender: la fusión y la solidificación se producen a una temperatura única y definida con precisión, al igual que algunas transformaciones estructurales en estado sólido. Después, las curvas de enfriamiento muestran pausas características, ya que la energía se absorbe o se libera para la propia transformación y no para el cambio de temperatura. En el caso de las aleaciones, la situación ya no es tan «puntual». A menudo, ocurre que una aleación comienza a solidificarse a una temperatura, pero termina a otra, y durante el proceso coexisten fases con composiciones variables.
Por eso, en la ciencia de los materiales se utilizan los diagramas de equilibrio de fases, también conocidos como diagramas de fases. Estos diagramas pueden considerarse como un mapa: muestran qué fases son estables en función de la temperatura y la composición y en qué orden se producen las transformaciones durante el calentamiento y el enfriamiento. Esto permite predecir tanto el curso de la cristalización y las transformaciones posteriores en estado sólido como, en consecuencia, la estructura y las propiedades de la aleación acabada.
Conceptos clave: sistema, fase y componentes
Para leer correctamente los diagramas de equilibrio, es necesario comprender el lenguaje que «hablan». En términos termodinámicos, un sistema es un fragmento separado de la realidad analizado en condiciones determinadas, por ejemplo, una muestra de aleación que estamos enfriando. Una fase se refiere a una parte homogénea de un sistema con propiedades idénticas y una composición química constante separada de otras fases por un límite de fase. Una fase puede ser un líquido, una solución sólida o una fase intermetálica específica, si se forma una.
Los componentes, es decir, las sustancias (normalmente, elementos) que componen la aleación y a partir de las cuales se pueden formar fases también son importantes. En el contexto de los diagramas binarios, solemos referirnos a un sistema compuesto por dos componentes cuyas proporciones varían en la aleación. En la práctica, esto significa que el diagrama no describe un único «material», sino toda una familia de aleaciones con diferentes composiciones, y cada cambio en la composición nos lleva a un lugar diferente en el mapa de fases.
Regla de las fases de Gibbs
Una de las razones por las que el comportamiento de las aleaciones difiere del de los metales puros es el número de variables que «controlan» el sistema. La regla de las fases de Gibbs organiza la relación entre el número de componentes, el número de fases y el número de grados de libertad. En la práctica metalúrgica, a menudo, se asume una presión constante, ya que su efecto sobre las transiciones de fase de los metales suele ser pequeño en comparación con el efecto de la temperatura y la composición.
El sentido práctico es el siguiente: si el sistema tiene poco «margen de maniobra», la transición debe producirse a una única temperatura (de ahí las paradas características). Sin embargo, cuando hay variabilidad en la composición y existe la posibilidad de que coexistan varias fases, el sistema puede pasar por zonas en las que se producen dos fases simultáneamente y sus composiciones cambian con la temperatura. En ese caso, la solidificación o las transformaciones en estado sólido se extienden a lo largo de un determinado intervalo de temperaturas y la estructura se forma por etapas.
¿Cómo se crea un diagrama de equilibrio binario?
Un diagrama binario típico muestra la relación entre la temperatura y la composición química. El eje horizontal representa la composición de la aleación (por ejemplo, el porcentaje de un componente) y el eje vertical representa la temperatura. Para construir dicho diagrama, se realiza una serie de experimentos con muchas aleaciones con diferentes proporciones de componentes y se registran las temperaturas a las que se producen las transformaciones. Esto se hace, normalmente, mediante métodos de análisis térmico basados en curvas de enfriamiento y calentamiento.
Los límites de las áreas de fase son especialmente importantes en el gráfico. Una línea denominada «liquidus» separa el área completamente líquida del área en la que el líquido coexiste con la fase sólida. La línea «solidus» marca el límite por debajo del cual la aleación es completamente sólida. Entre el liquidus y el solidus suele haber una zona de mezcla (por ejemplo, fase líquida + fase sólida), lo que en la práctica significa que, durante el enfriamiento, la aleación pasa por una etapa en la que parte del material ya es sólido y parte permanece líquido.
También es importante la forma en la que se lee la composición de las fases a una temperatura determinada. Esto se hace trazando una línea horizontal (isoterma) a través del gráfico: la intersección con el liquidus muestra la composición del líquido y la intersección con el solidus muestra la composición de la fase sólida en equilibrio a esa temperatura. Esta es la base para inferir lo que realmente ocurre en la aleación durante el enfriamiento.
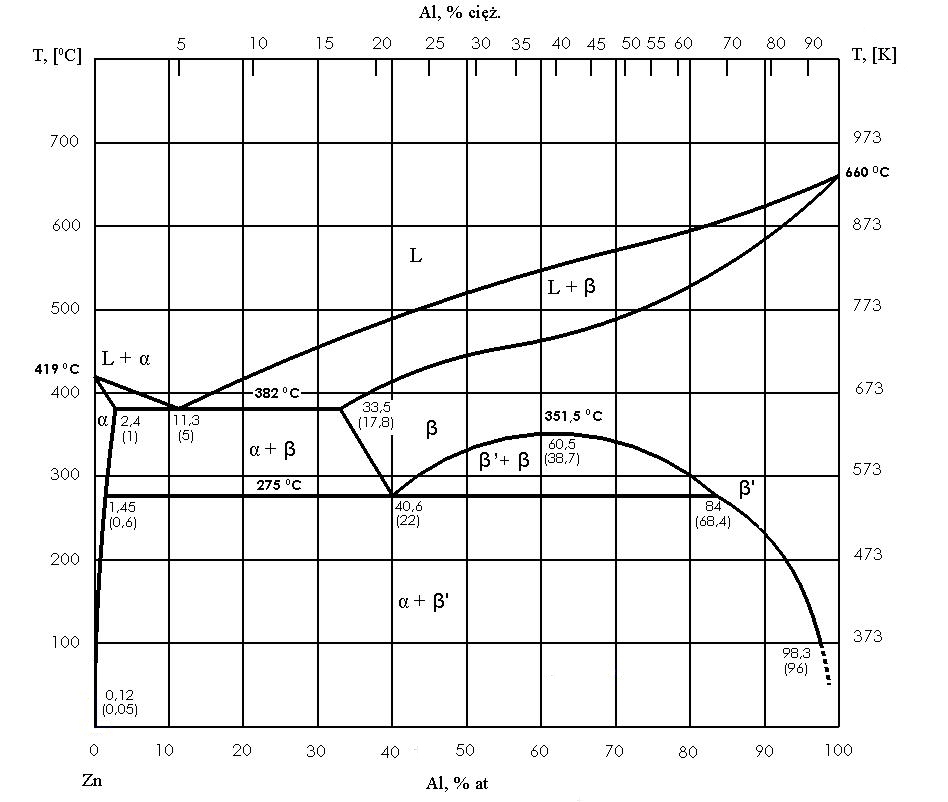
Los tipos más importantes de sistemas de equilibrio
Solución sólida continua
En algunos sistemas, los componentes se mezclan libremente entre sí tanto en estado líquido como sólido. En este caso, por debajo del solidus, hay una fase: una solución sólida con una composición que depende de la posición en el eje de composición. Durante el enfriamiento, la aleación comienza a solidificarse en el liquidus cuando aparecen los primeros cristales de la solución sólida y termina en el solidus cuando desaparece la última parte del líquido. Este es un ejemplo clásico de solidificación en un rango de temperatura sin que se produzca ni una sola parada.
Cabe señalar que en la zona de «solución líquida + sólida», las composiciones de ambas fases son diferentes y cambian con la temperatura. La lectura de la isoterma nos permite determinar qué parte de la aleación se encuentra ya en estado sólido en un momento dado y qué parte sigue siendo líquida.
Eutéctico
Un sistema eutéctico es muy característico cuando los componentes se mezclan en un líquido, pero se disuelven mal o no se disuelven en absoluto en estado sólido. En este caso, existe una composición y una temperatura eutécticas en las que un líquido homogéneo se transforma en dos fases sólidas a la vez. Dicha transformación es isotérmica, por lo que hay una pausa clara en la curva de enfriamiento, como en el caso del metal puro. No obstante, el mecanismo es diferente: en lugar de una sola fase sólida, se forma una mezcla fina de dos fases, normalmente, con una morfología específica y regular.
Las aleaciones con una composición distinta a la eutéctica forman una estructura mixta. Si la aleación es hipereutéctica, primero se separan los cristales primarios de una fase y, solo entonces, el resto del líquido se solidifica como eutéctico. Si la aleación es hipereutéctica, primero aparecen los cristales primarios de la segunda fase, seguidos de los eutécticos. Como resultado, la microestructura depende de la composición: puede predominar el eutéctico, pueden predominar los cristales primarios o ambos componentes pueden tener proporciones similares.
Eutéctico con solubilidad limitada en estado sólido
En la práctica, a menudo se da una situación intermedia: los componentes se mezclan bien en estado líquido, pero en estado sólido solo forman soluciones sólidas en cierta medida. Así pues, en lugar de fases «puras», se forman soluciones sólidas en los límites, comúnmente denominadas α y β, y el eutéctico se convierte en una mezcla de estas dos soluciones con composiciones saturadas a la temperatura eutéctica.
Esto es muy importante porque, con un mayor enfriamiento, la solubilidad en estado sólido suele disminuir, por lo que las soluciones α y β pueden llegar a estar sobresaturadas. Como resultado, pueden producirse separaciones secundarias y una mayor «maduración» de la estructura una vez completada la solidificación. Por lo tanto, el diagrama no es solo una descripción de la cristalización, sino también una guía de los cambios en el estado sólido que afectan a las propiedades del material.
Peritéctico
En los sistemas peritécticos, se produce una transformación en la que el líquido reacciona con la fase sólida existente para formar una nueva fase sólida. Esto ocurre a una temperatura específica porque en el momento de la reacción coexisten tres fases. El mecanismo peritéctico tiene importancia práctica porque la nueva fase a menudo crece sobre los cristales de la fase original y forma una capa que dificulta la difusión posterior de los componentes. Esto puede hacer que el curso real de la transformación se desvíe del equilibrio ideal, especialmente, con un enfriamiento más rápido.
Desde un punto de vista tecnológico, la peritéctica puede ser una fuente de heterogeneidad y estructuras que dependen no solo del diagrama de equilibrio en sí, sino también de la cinética, es decir, la velocidad de los procesos de difusión. Por lo tanto, al interpretar los diagramas, es importante recordar que el diagrama describe el equilibrio y no siempre el estado real «sobre la marcha», sin tiempo para que la composición se equilibre.
Solubilidad limitada en líquido
A veces, incluso en estado líquido, el sistema no es completamente homogéneo. Puede ocurrir que, dentro de un determinado rango de temperaturas, el líquido se separe en dos líquidos con composiciones diferentes, lo que favorece la segregación y la formación de zonas con propiedades diferentes. En un sistema de este tipo, es posible que se produzca una transformación monotéctica en la que un líquido se transforma en otro líquido y en una fase sólida.
Desde el punto de vista de la tecnología de fundición, esto es importante porque la separación de líquidos puede provocar una heterogeneidad no deseada de la aleación. En la práctica, esto a menudo se contrarresta mediante un control adecuado del proceso, incluida la selección de la velocidad de enfriamiento o el método de mezcla del metal líquido con el fin de limitar el tiempo de desarrollo de la segregación.
Compuestos químicos y fases intermetálicas
En muchos sistemas, se forman compuestos químicos y fases intermetálicas. Si un compuesto tiene una composición estequiométrica constante, aparece en el diagrama como una posición característica correspondiente a esta proporción de componentes. Dicho compuesto puede fundirse de forma «similar al metal puro» cuando se transforma en un líquido de la misma composición o puede formarse y desaparecer en transformaciones peritécticas cuando el proceso continúa mediante la reacción con el líquido.
Las fases intermetálicas suelen ser duras y frágiles, y su presencia puede alterar significativamente las propiedades de la aleación. Por esta razón, los diagramas de fases son particularmente importantes en el diseño de aleaciones, ya que nos permiten predecir si, dentro de un rango determinado de composición y temperatura, aparecerá una fase que perjudicará la plasticidad o, por el contrario, fortalecerá la aleación mediante precipitados finos.
Transformaciones en estado sólido: eutectoides y peritectoides
Los diagramas de equilibrio no terminan con la solidificación. En muchas aleaciones, las transformaciones que se producen tras la transición al estado sólido son importantes, especialmente, cuando la solubilidad en las soluciones sólidas cambia con la temperatura o cuando uno de los componentes presenta polimorfismo. La transformación eutectoide, de particular importancia, es equivalente a la eutéctica, pero se produce íntegramente en estado sólido: una solución sólida se descompone en dos fases sólidas a temperatura constante. Esta transformación suele dar lugar a una estructura fina y regular y puede alterar significativamente las propiedades mecánicas.
También existe una transformación peritéctica, análoga al peritéctico, pero sin la participación de líquido: dos fases sólidas reaccionan para formar una tercera fase sólida. En la práctica, las transformaciones en estado sólido pueden ser cruciales, ya que pueden determinar la dureza, la resistencia al impacto o la resistencia a la fluencia, incluso si el proceso de solidificación se ha desarrollado correctamente.
Importancia práctica
La conclusión más importante del análisis de los diagramas es que las propiedades de las aleaciones se deben, principalmente, a su estructura y no solo a los elementos que contienen. Las aleaciones monofásicas suelen ser más homogéneas y sus propiedades suelen cambiar de forma más suave con la composición. En las aleaciones multifásicas, la situación es más compleja, ya que el comportamiento del material viene determinado por el tipo de fases, su proporción, distribución, tamaño de grano y morfología (por ejemplo, la forma de los eutécticos o la naturaleza de los precipitados).
Por lo tanto, un diagrama de fases es una herramienta que ayuda a vincular las condiciones del proceso con el resultado. Si se conoce a qué temperaturas y composiciones se producen determinadas fases, se puede seleccionar conscientemente la composición de la aleación y las condiciones de enfriamiento y tratamiento térmico. En la práctica, esto significa que es posible predecir si la aleación tenderá a segregarse, si aparecerán fases intermetálicas frágiles, si los precipitados pueden utilizarse para reforzarla o si la estructura será estable en las condiciones de funcionamiento.
Sistemas de equilibrio de fase de aleaciones: resumen
Los sistemas de equilibrio de fases son una herramienta que organiza el comportamiento de las aleaciones de forma sistemática y predecible. Se pueden utilizar para determinar qué fases serán estables, cuándo comenzará y terminará la solidificación, si se producirán fenómenos eutécticos o peritécticos y qué transformaciones pueden tener lugar en estado sólido. En la práctica, esto ofrece la capacidad de controlar la microestructura y, por lo tanto, controlar las propiedades mecánicas y físicas del material. La capacidad de leer diagramas de fase es, en consecuencia, una de las habilidades más importantes en la ciencia de los materiales y la metalurgia, ya que permite traducir la teoría de las transformaciones de fase en decisiones de ingeniería reales.