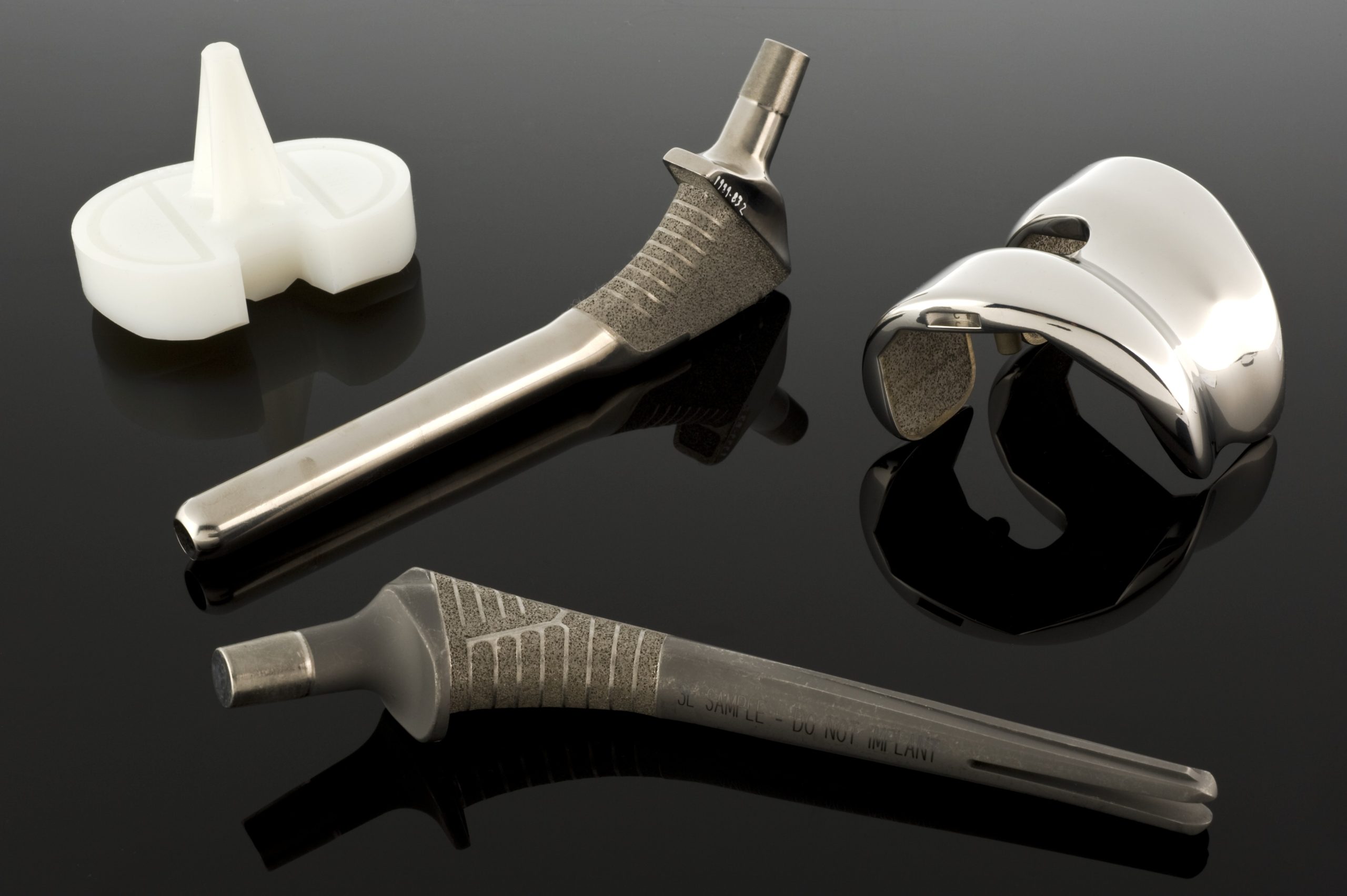
La cerámica como material biomédico

Índice
La cerámica se asocia, a menudo, con la porcelana, el vidrio o los elementos arquitectónicos. Sin embargo, en tecnología biomédica, el término tiene un significado mucho más amplio. La cerámica es un material inorgánico no metálico cuyos componentes principales suelen ser óxidos metálicos, silicatos, carburos o nitruros. Se caracterizan por su gran dureza, su alta resistencia a la compresión, su alto punto de fusión y una muy baja conductividad eléctrica y térmica. A nivel atómico, sus propiedades se deben, principalmente, al predominio de enlaces iónicos o covalentes y al número limitado de posibles planos de deslizamiento en la red cristalina. Por lo tanto, a diferencia de los metales, la cerámica no se deforma fácilmente por deformación plástica.
La consecuencia más importante de esta estructura es la fragilidad. La cerámica tiende a romperse en presencia de microfisuras, inclusiones o muescas afiladas. En lugar de deformarse gradualmente, como lo hacen los metales, se rompen de forma repentina y relativamente violenta cuando la tensión que se produce cerca de un defecto existente supera un valor crítico. Esto explica por qué su resistencia a la tracción es mucho menor que su resistencia a la compresión. Es interesante señalar que, en condiciones ideales, cuando el material está prácticamente libre de defectos, la cerámica puede ser extremadamente resistente. Un ejemplo de ello son las microfibras de vidrio, con una resistencia a la tracción de varios gigapascales, lo que supera la resistencia de muchos tipos de acero de alta calidad.
La cerámica es también un material que, prácticamente, no se deforma a temperatura ambiente. Mientras que los metales pueden deformarse gradualmente bajo una tensión prolongada, la cerámica, gracias a su estructura de enlace rígida, conserva sus propiedades dimensionales hasta que se produce una fisura. Esta propiedad es tanto una ventaja, si pensamos en una transferencia de carga estable, como una desventaja, ya que la incapacidad de «liberar» tensiones mediante deformación plástica favorece las roturas repentinas.
El campo de la biocerámica surgió cuando la cerámica comenzó a utilizarse deliberadamente para entrar en contacto con los tejidos corporales. Se descubrió que las composiciones cerámicas cuidadosamente seleccionadas no solo pueden utilizarse en la electrónica o en industrias donde predominan las altas temperaturas, sino también para sustituir fragmentos óseos, restaurar dientes, construir implantes articulares e incluso elementos que entran en contacto con la sangre, como las válvulas cardíacas artificiales. Sin embargo, deben cumplirse una serie de criterios biológicos fundamentales.
Para ser considerado biocerámico, un material cerámico debe ser no tóxico, no cancerígeno y no alergénico, no debe provocar reacciones inflamatorias crónicas, debe ser biocompatible y debe mantener su biofuncionalidad durante todo el periodo de implantación previsto. En otras palabras, no debe causar daños, debe cumplir su función mecánica o biológica y no debe degradarse de forma impredecible.
Sobre esta base, las biocerámicas se dividen en tres clases principales. La primera clase consiste en cerámicas no reabsorbibles, es decir, cerámicas relativamente biocompatibles que, tras su implantación, prácticamente no se disuelven ni sufren cambios estructurales significativos y están diseñadas para durar muchos años. El segundo grupo está formado por cerámica biodegradable (reabsorbible), diseñada para ser sustituida gradualmente por el tejido en crecimiento del huésped. La tercera categoría está formada por biocerámica bioactiva y reactiva en superficie, cuya función es formar una fuerte unión química con el hueso u otro tejido, principalmente mediante reacciones que tienen lugar solo en la zona superficial.

Biocerámica relativamente biocompatible
La biocerámica relativamente biocompatible conserva sus propiedades físicas y mecánicas durante un uso prolongado en el cuerpo. No se disuelve de forma significativa, es resistente a la corrosión y al desgaste, y el contacto con los tejidos suele reducirse a una adaptación o integración mecánica sin reacciones químicas significativas. El óxido de aluminio, el óxido de circonio y varios tipos de carbono, incluido el carbono pirolítico, son especialmente importantes en este grupo.
El óxido de aluminio, también conocido como alúmina (Al₂O₃), es uno de los materiales cerámicos más utilizados en implantología. En aplicaciones biomédicas, se utiliza una variante alfa muy pura en la que el contenido de Al₂O₃ es superior al 99,5 % y la cantidad de impurezas, como la sílice y los óxidos alcalinos, se limita a un porcentaje de décimas. El óxido de aluminio tiene una estructura cristalina romboédrica y se encuentra en la naturaleza en forma de zafiro o rubí, dependiendo de las impurezas colorantes presentes. Las formas monocristalinas de este material se pueden obtener fundiendo gradualmente el polvo sobre un germen cristalino, del que se «extrae» el cristal en crecimiento.
Las propiedades mecánicas del óxido de aluminio son impresionantes. El módulo de elasticidad es de varios cientos de gigapascales, la resistencia a la flexión es superior a 400 MPa y la dureza varía entre 20 y 30 GPa. Este último valor significa que el óxido de aluminio tiene una puntuación muy alta en la escala de Mohs (9/10), solo superada por el diamante. Sin embargo, la solidez y la fiabilidad del óxido de aluminio policristalino dependen, en gran medida, del tamaño del grano y la porosidad. Al reducir la porosidad y utilizar una estructura de grano fino, se aumenta la solidez y se reduce la dispersión de los resultados.
Esta combinación de dureza, resistencia al desgaste e inercia química en el cuerpo hace que el óxido de aluminio sea el material ideal para la construcción de elementos deslizantes en endoprótesis articulares, en particular, cabezas de prótesis de cadera que interactúan con copas de polietileno de masa molecular ultraalta. Los estudios sobre implantes de óxido de aluminio insertados en el cráneo no han demostrado toxicidad ni signos de rechazo, y han mostrado una muy buena tolerancia durante largos periodos de observación. El óxido de aluminio también se utiliza en implantes dentales, placas y tornillos óseos, reconstrucciones del oído medio y componentes que requieren una alta dureza e inercia química.
El segundo material importante de este grupo es el óxido de circonio (ZrO₂). En su forma pura, tiene un diagrama de fases complejo: a diferentes temperaturas, adopta diferentes estructuras cristalinas, lo que conlleva cambios de volumen considerables. Esta variabilidad es desfavorable desde el punto de vista de la estabilidad dimensional, por lo que en la práctica se utiliza óxido de circonio parcialmente estabilizado con óxidos como Y₂O₃. Gracias a estos aditivos, es posible estabilizar las fases a altas temperaturas (tetragonales o cúbicas) también a temperaturas más bajas, lo que mejora la estabilidad de la estructura después de la sinterización.
El óxido de circonio parcialmente estabilizado tiene un módulo de elasticidad inferior al del óxido de aluminio, lo que lo hace algo más similar al hueso, al tiempo que presenta una resistencia a la fractura especialmente buena. Esto se debe al mecanismo de refuerzo transformacional: se produce una transición de fase local cerca de la fractura que se propaga, acompañada de un ligero aumento de volumen, lo que «cierra» la fractura e impide que siga creciendo. La biocompatibilidad del óxido de circonio es muy buena y los parámetros de fricción y desgaste cuando se utiliza con UHMWPE son tan favorables que este material se ha utilizado en cabezas de endoprótesis articulares y otros elementos de soporte.
Las diferentes formas de carbono desempeñan un papel especial en la cerámica bioinerte. La estructura cristalina del grafito, una forma clásica de carbono, consiste en redes planas hexagonales de átomos unidos entre sí por fuertes enlaces covalentes dispuestos en capas. Entre las capas, se producen interacciones más débiles, lo que facilita su movimiento entre sí y explica el efecto lubricante del grafito. En materiales como el carbono pirolítico o el carbono vítreo, estas capas hexagonales están parcialmente alteradas, deformadas y mezcladas con áreas amorfas. A escala macroscópica, esto da lugar a propiedades mecánicas más isotrópicas.
El carbono pirolítico es especialmente valioso en implantología, ya que se caracteriza por su alta solidez, su considerable módulo de elasticidad y su excelente compatibilidad sanguínea. Este material se utiliza normalmente como recubrimiento que se aplica desde la fase gaseosa a las formas finales de los implantes, por ejemplo, en componentes de válvulas cardíacas o prótesis vasculares. Los parámetros del proceso, como la temperatura, la presión, la composición del gas, la geometría del reactor y el tiempo de deposición permiten obtener un ajuste muy preciso de la densidad, la anisotropía, el tamaño de los cristales y la presencia de defectos en el carbono. Una mayor densidad suele implicar una mayor solidez y módulo de elasticidad, lo que es crucial para la seguridad a largo plazo de los implantes.
También existen compuestos carbono-carbono, en los que las fibras de carbono refuerzan la matriz de carbono. Alcanzan una resistencia muy elevada en la dirección de las fibras, pero son claramente anisotrópicos y porosos. Desde el punto de vista mecánico, pueden resultar atractivos, pero su uso requiere una planificación extremadamente cuidadosa de la distribución de la carga en la carrocería.
Biocerámica biodegradable
En muchas aplicaciones, el objetivo no es sustituir el tejido de forma permanente, sino rellenar temporalmente un defecto, proporcionar soporte mecánico o administrar un medicamento, tras lo cual el por tejido huésped regenerado debe sustituir gradualmente al implante. En tales situaciones, los materiales cerámicos reabsorbibles, que se degradan de forma controlada, son la opción ideal.
Históricamente, el yeso o sulfato de calcio dihidratado fue uno de los primeros materiales de este tipo. Ya se utilizaba a finales del siglo XIX como sustituto óseo. Sin embargo, el verdadero avance se produjo en la segunda mitad del siglo XX, cuando aparecieron en el mercado los fosfatos de calcio totalmente sintéticos y los sistemas más complejos, como la cerámica de fosfato de aluminio y calcio (ALCAP), el fosfato de zinc y calcio (ZCAP), el fosfato de sulfato de zinc y calcio (ZSCAP) y el fosfato de hierro y calcio (FECAP).
El representante más importante de este grupo es el hidroxiapatito (HA), que químicamente es similar a la fase mineral de los huesos y los dientes. Tiene una fórmula similar a Ca₁₀(PO₄)₆(OH)₂ y pertenece a la familia del apatito. Estructuralmente, forma prismas hexagonales en los que los iones hidroxilo se disponen en columnas a lo largo del eje c y algunos iones calcio se unen fuertemente a ellos. Los iones Ca²⁺ restantes completan la red cristalina y proporcionan estabilidad a la estructura. La relación molar entre calcio y fósforo es de 10:6 y la densidad teórica es cercana a 3,2 g/cm³. La sustitución de los iones OH⁻ por iones F⁻ da como resultado una mayor estabilidad química, lo que explica por qué la fluoración fortalece el esmalte dental.
El hidroxiapatito es un material con una biocompatibilidad excepcional, ya que su estructura y composición química son muy similares a las del tejido óseo natural. Tras su implantación en forma de gránulos o bloques porosos, se forma rápidamente hueso poroso nuevo y la frontera entre el implante y el hueso suele adoptar la forma de una unión química directa, sin una zona fibrosa clara.
Las propiedades mecánicas del hidroxiapatito pueden variar considerablemente en función del método de producción, el tamaño del grano y la porosidad. El módulo de elasticidad puede alcanzar un valor similar al de los tejidos duros naturales, como el esmalte, la dentina o el hueso compacto. Esto permite diseñar implantes cuya rigidez se adapte al tejido circundante, lo que reduce el riesgo del fenómeno no deseado de blindaje a la tensión, es decir, la descarga y la pérdida gradual de hueso.
Además de la hidroxiapatita, el trifosfato de calcio β (β-TCP) también desempeña un papel importante. Es más soluble que la HA, por lo que se reabsorbe más rápidamente in vivo, al tiempo que mantiene una buena osteoconductividad. Esto hace que el material sea muy adecuado como relleno temporal para defectos óseos, que desaparece gradualmente a medida que crece el propio hueso del paciente. Al igual que la hidroxiapatita, el TCP se produce a menudo mediante síntesis húmeda a partir de las sales de calcio y fosfato adecuadas, seguida de calcinación y sinterización. Puede formar compuestos con aminoácidos como la cisteína que, cuando se mezclan con agua, se unen y se endurecen en el lugar de la implantación, lo que permite que el material se forme directamente en el defecto.
Los sistemas cerámicos más complejos, como ALCAP, ZCAP, ZSCAP y FECAP, suelen ser polifásicos. Esto significa que su estructura contiene diferentes fases cristalinas con diferente solubilidad y velocidades de reabsorción. Esta estructura permite diseñar materiales que se degradan en varias fases: algunas fases desaparecen más rápidamente, otras más lentamente, y durante este proceso se liberan iones biológicamente importantes, como el zinc o el hierro. También pueden utilizarse como portadores de fármacos: el principio activo se encapsula en una matriz cerámica y se libera gradualmente a medida que el implante se reabsorbe.
Un ejemplo interesante de material reabsorbible natural es la corallina, es decir, el esqueleto de los corales, que se compone principalmente de carbonato cálcico en forma de aragonita. Algunas especies de coral forman estructuras porosas tridimensionales únicas que, en cuanto a tamaño y distribución de los poros, se asemejan al hueso trabecular. Esto hace que materiales como Biocoral sean ideales para rellenar defectos óseos. El carbonato cálcico se reabsorbe gradualmente y se sustituye por hueso. Además, los esqueletos de coral pueden transformarse hidrotérmicamente en hidroxiapatita y conservar su arquitectura porosa natural, lo que combina las ventajas de una gran similitud química con el hueso con una microestructura espacial muy favorable.
Biocerámica bioactiva reactiva en superficie
Entre la cerámica extremadamente inerte y los materiales más rápidamente reabsorbibles, existe un tercer grupo muy importante: la biocerámica bioactiva, es decir, vidrios reactivos en superficie, vitrocerámica y ciertas formas de hidroxiapatita. Su característica especial es que, aunque el volumen total del material permanece relativamente estable, la superficie reacciona activamente con los fluidos corporales y forma una capa que puede establecer una fuerte unión química con el hueso.
Un ejemplo clásico de ello son los vidrios de silicato bioactivos, como los materiales de la familia Bioglass, y sus homólogos cristalizados: las vitrocerámicas. Estos sistemas se basan en sílice (SiO₂) con adiciones de óxido de calcio, óxido de sodio y óxido de fósforo (V). Tras su implantación en el cuerpo, se produce una serie de reacciones en la superficie de estos materiales: en primer lugar, se intercambian iones Na⁺ y Ca²⁺ con el entorno, lo que provoca un cambio local en el pH y la actividad iónica. A continuación, se forma una capa de gel rica en sílice sobre la que se depositan fosfatos de calcio, que con el tiempo se transforman en una estructura similar a la apatita. Esta capa de apatita en la superficie permite que el hueso se ancle directamente en el vidrio, sin la intervención de tejido fibroso.
La bioactividad del vidrio depende, en gran medida, de su composición química, principalmente del contenido de SiO₂ y las proporciones de CaO, Na₂O y P₂O₅. Existe un rango específico de composición en el que se forman simultáneamente una capa de sílice y una capa de fosfato. Fuera de este rango, el material es demasiado poco reactivo para formar una unión duradera con el tejido o demasiado sensible a la disolución.
La vitrocerámica, como el Bioglass o Ceravital cristalizados, se produce mediante cristalización controlada del vidrio. Durante la producción, el material se somete a una serie de tratamientos térmicos que dan lugar a la formación de un gran número de pequeños cristales (con un diámetro de una fracción de micrómetro) distribuidos uniformemente por todo el volumen. Como resultado, la vitrocerámica combina una alta densidad, una gran solidez, una buena resistencia a los arañazos y unas propiedades térmicas adecuadas. Una composición cuidadosamente seleccionada garantiza que se mantenga la bioactividad, al tiempo que se mejoran los parámetros mecánicos en comparación con el vidrio amorfo puro.
A pesar de estas ventajas, el vidrio bioactivo y la vitrocerámica siguen siendo materiales relativamente frágiles. Aunque su resistencia a la tracción ha mejorado, sigue siendo demasiado baja para que se puedan utilizar como componentes independientes en implantes grandes y de soporte, como los vástagos para prótesis articulares. Sin embargo, se utilizan mucho como recubrimiento de implantes metálicos, donde forman una conexión directa con el hueso, y como relleno en composites dentales, materiales para la reconstrucción del oído medio y pequeños implantes craneales.
Deterioro y fatiga de la cerámica en el cuerpo
Al diseñar implantes cerámicos, es importante no solo tener en cuenta las propiedades del material inmediatamente después de su fabricación, sino también cómo cambian estas propiedades con el tiempo bajo la influencia del entorno biológico y las cargas mecánicas.
En el caso de la cerámica no absorbente, la fatiga estática y dinámica desempeñan un papel importante. En un entorno acuático, que se corresponde con las condiciones fisiológicas, el agua puede acelerar el crecimiento de las microfisuras existentes. Si el material contiene aditivos que facilitan la penetración del agua, esto puede provocar una reducción gradual de la resistencia bajo carga prolongada, incluso si las tensiones son inferiores al límite de resistencia determinado en una prueba a corto plazo. Este fenómeno se ha estudiado exhaustivamente, entre otros, en el óxido de aluminio, donde se ha observado la relación entre la presencia de trazas de acción del agua en la superficie de fractura y la disminución de la resistencia.
Los modelos de resistencia estadística, como la distribución de Weibull, se utilizan a menudo para describir el comportamiento de la cerámica, en el que la probabilidad de que aparezcan defectos depende de un parámetro constante de escala y forma m. Cuanto mayor es el valor del parámetro m, menor es la dispersión de la resistencia y mayor es la previsibilidad del comportamiento del material, lo que es crucial en el diseño de componentes de implantes. Los ensayos de prueba, en los que los componentes acabados se someten a tensiones superiores a las cargas de funcionamiento previstas, también son una herramienta práctica para la ingeniería de fiabilidad. Las muestras más débiles se destruyen durante las pruebas y, para las muestras restantes, se puede determinar la vida útil mínima prevista a un nivel de carga determinado.
En el caso de los recubrimientos de carbono sobre metales, las pruebas de fatiga han demostrado que la integridad del recubrimiento depende, en gran medida, del comportamiento del sustrato. Si el sustrato metálico no sufre una deformación plástica significativa, el carbono pirolítico puede permanecer intacto incluso tras un gran número de ciclos de carga, lo que es especialmente importante en el caso de las válvulas cardíacas recubiertas o las prótesis vasculares.
Técnicas de producción para biocerámica
La elección de la técnica de producción de la biocerámica depende en gran medida del uso previsto del implante. Si el objetivo es sustituir el tejido duro y transmitir cargas mecánicas, se dará prioridad a una alta densidad, una gran resistencia y un módulo de elasticidad adecuado. En aplicaciones en las que la integración tisular y la vascularización intensiva son lo más importante, la porosidad abierta elevada y la distribución adecuada del tamaño de los poros desempeñan un papel clave.
Los implantes de soporte utilizan técnicas como el moldeo por inyección, el moldeo por gel y métodos de microemulsión, que permiten alcanzar una alta densidad (por encima del 97‑99 % de la densidad teórica) con una porosidad relativamente baja. Los aditivos seleccionados adecuadamente, entre los que se incluyen los fosfatos de sodio, el litio o el óxido de circonio parcialmente estabilizado, pueden mejorar la sinterabilidad, aumentar la microdureza y la resistencia a la rotura e influir en el desarrollo de la microestructura durante la sinterización. Siempre hay que tener en cuenta que un exceso de aditivos o una selección incorrecta de los mismos puede dar lugar a la formación de fases no biocompatibles o excesivamente solubles.
Si el objetivo es lograr una rápida integración con el hueso y otros tejidos, se diseñan materiales cerámicos con una alta porosidad abierta, con poros cuyo diámetro permite la penetración de vasos sanguíneos y células (normalmente, al menos varias decenas de micrómetros). Para ello se utiliza, entre otros, el método de consolidación con almidón, en el que se mezclan granos de almidón con una suspensión cerámica y luego se hinchan durante el secado. Durante la sinterización, el almidón se quema y deja poros. Ajustando la cantidad de almidón en la mezcla, es posible controlar con precisión la porosidad final y la distribución del tamaño de los poros, con lo que se obtienen estructuras con poros que varían desde unos pocos micrómetros hasta decenas de micrómetros.
Otra técnica es el moldeo por goteo, en el que se forman gotas o gránulos a partir de una suspensión de hidroxiapatita, por ejemplo, haciéndolos gotear sobre moldes especiales o en nitrógeno líquido. Tras el secado, la calcinación y la sinterización, se obtienen gránulos de HA porosos que pueden utilizarse como relleno para defectos óseos. Independientemente de los detalles del proceso, el objetivo es crear una estructura lo suficientemente resistente como para soportar la implantación y la fase inicial de cicatrización y que, al mismo tiempo, ofrezca un alto grado de penetración en los tejidos.
Resumen: la cerámica como material biomédico
La biocerámica es, actualmente, uno de los grupos más importantes de biomateriales utilizados en medicina. Entre ellos, se incluyen cerámicas de óxido relativamente bioinertes, como el óxido de aluminio y el óxido de circonio, así como fosfatos de calcio reabsorbibles, estructuras basadas en coral, sistemas multicomponentes que contienen zinc o hierro, y vidrio y vitrocerámica bioactivos. Cada uno de estos materiales tiene su propia «función» en el cuerpo: algunos están destinados a ser sustitutos óseos estables y durader
os, otros a dar paso gradualmente a tejido nuevo y otros a proporcionar un fuerte anclaje químico para los implantes en los huesos.
La clave para diseñar biocerámica es comprender la relación entre la composición química, la estructura cristalina, la microestructura, el método de producción y el comportamiento en un entorno biológico. Los implantes modernos suelen combinar diferentes materiales: metal para soportar la carga, cerámica bioactiva para una unión duradera con el hueso, andamios reabsorbibles para favorecer la regeneración y recubrimientos de carbono en los componentes que entran en contacto con la sangre. La biocerámica ya no es solo un «material duro», sino que hoy en día es una herramienta diseñada con precisión para la ingeniería de tejidos y la implantología que permite imitar cada vez mejor las funciones biológicas y la estructura de los tejidos corporales.