Proč je povrch implantátu tak důležitý?
V inženýrství biomateriálů se snadno uchýlíme k intuici vycházející z tradiční materiálové vědy: jelikož implantát musí odolávat zatížení, nesmí korodovat, nesmí se nadměrně opotřebovávat a musí fungovat po dlouhá léta, měl by jeho úspěch záviset především na materiálu „uvnitř“. To je však jen část pravdy. Vnitřní materiál skutečně odpovídá za pevnost, tuhost, pružnost, trvanlivost a propustnost. Z pohledu těla však k prvnímu a nejdůležitějšímu kontaktu nedochází s celým blokem materiálu, ale s jeho vnější vrstvou. Právě tato vrstva přichází do styku s krví, bílkovinami, buňkami a tělními tekutinami. V praxi to znamená, že implantát může být mechanicky velmi dobrý, ale biologicky problematický, pokud jeho povrch vysílá tkáním „nesprávný signál“.
Toto zjištění mění způsob, jakým uvažujeme o návrhu implantátů. Místo toho, abychom se ptali pouze „z čeho by měl být implantát vyroben?“, musíme zvážit, jak by měl vypadat povrch implantátu. U biomateriálů není biologická reakce pouhým odrazem chemického složení celé součásti. Jedná se spíše o reakci na to, co se děje na rozhraní mezi materiálem a tkání: chemické vlastnosti povrchu, smáčivost, náboj, drsnost, uspořádání a reaktivita. Proto je úspěch implantátu tak často určen nikoli objemem materiálu, ale právě na fázové hranici.
Tento článek vychází z publikace Biomaterials Science: An Introduction to Materials in Medicine, ed. William R. Wagner et al., 4. vyd., 2020. Následující obsah představuje pouze obecný přehled tématu. Zájemcům o danou problematiku doporučujeme seznámit se s odbornou literaturou.
Jak tělo reaguje na povrch materiálu?
Nejdůležitější výchozí bod je jednoduchý: tělo „nevidí“ celý implantát najednou. Nejprve „čte“ jeho povrch. Autoři knihy Biomaterials Science výslovně uvádějí, že u materiálů, které neuvolňují nežádoucí látky, k přenosu informací z materiálu na proteiny, buňky a celé tělo dochází prostřednictvím povrchové struktury. Tělo tedy reaguje spíše na specifickou chemii a uspořádání vnější vrstvy než na průměrné vlastnosti celého materiálu. Tato zdánlivě drobná změna důrazu má obrovský praktický význam, protože posouvá otázku biokompatibility z úrovně „jaký druh slitiny nebo polymeru máme“ na úroveň „jak vypadá a chová se jeho rozhraní“.
Je důležité si uvědomit, že povrch není pouze tenkou vrstvou materiálu, která se chová stejně jako jeho vnitřek. Kniha zdůrazňuje, že povrch je zónou se zvláštní reaktivitou a téměř nevyhnutelně se liší od vnitřku materiálu. U skutečného kovového materiálu může vnější vrstva obsahovat nejen oxid kovu, ale také adsorbovanou vodu, polární organické sloučeniny a uhlovodíkové kontaminanty. U polymerů se tato jedinečná povrchová zóna může pohybovat v rozmezí přibližně 10 až 100 nm. To je důležité, protože to znamená, že i když je objemový materiál homogenní, jeho biologicky aktivní část může být chemicky a strukturálně komplexní.
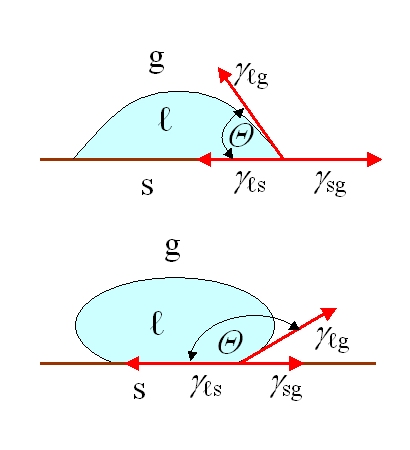
Z biologického hlediska není povrch pouze otázkou chemického složení. Autoři uvádějí mnoho vlastností, které mohou ovlivnit biologické reakce: drsnost, vzory a topografie, smáčivost, povrchová mobilita, chemické složení, elektrický náboj, krystalinita, modul pružnosti a heterogenita. Zároveň upřímně poznamenávají, že zatím není možné identifikovat jedinou univerzální vlastnost, která by byla nejdůležitější pro každou biologickou reakci. V praxi se jedná o velmi technicky orientovanou lekci; návrh nesmí být založen na jediném parametrickém sloganu, jako je „zvýšíme drsnost“ nebo „uděláme povrch hydrofilnějším“, protože reakce těla je výsledkem interakce několika charakteristik najednou.
Tento přístup vysvětluje, proč se dva implantáty vyrobené ze stejného materiálu mohou chovat biologicky odlišně. Ke změně stavu povrchu stačí změna zpracování, sterilizace, skladování nebo balení. Kniha dokonce zdůrazňuje takové banální problémy, jako jsou otisky prstů, přísady migrující z obalu nebo kontaminanty z papíru či fólie. V laboratoři se jedná o detail, ale ve skutečnosti jsou to právě takové detaily, které mohou způsobit, že testujeme povrch, který není ten, který se skutečně nachází na implantátu používaném v klinické praxi.

Jak se povrch promítá do biokompatibility
Pokud je povrch primárním komunikačním jazykem mezi implantátem a tělem, musíme se zeptat, jak tento dialog vypadá. Jedním z klíčových mechanismů je adsorpce proteinů. Zdroj zdůrazňuje, že po implantaci syntetického biomateriálu se adhezivní proteiny adsorbují na jeho povrch velmi rychle, během několika sekund. Tímto způsobem se materiál, který sám o sobě postrádá biologické rozpoznávací motivy, stává pro tělo „čitelným“. Jinými slovy, buňky často nereagují přímo na čistý materiál, ale na vrstvu proteinů, která se na jeho povrchu vytvoří krátce po kontaktu s tělem.
To má zásadní význam pro pochopení biokompatibility. Biokompatibilita neznamená pouze absenci akutní toxicity. Znamená schopnost materiálu vyvolat vhodnou reakci hostitele v konkrétní aplikaci. Tato „vhodná reakce“ může znamenat něco jiného pro stent, něco jiného pro ortopedický implantát a ještě něco jiného pro katétr. V každém z těchto případů povrch řídí počáteční biologické děje: které proteiny se adsorbují, v jaké konfiguraci, které buněčné receptory budou stimulovány a zda signál povede k integraci do tkáně, aktivaci krevních destiček, tvorbě biofilmu nebo reakci na cizí těleso.
Dobrým příkladem je srovnání adhezních a pasivačních proteinů. Kniha popisuje, jak předběžné potažení povrchu fibronektinem zvyšuje adhezi mnoha buněk, zatímco albumin ji může omezit. Nejedná se pouze o zajímavost z oblasti buněčných kultur, ale o model toho, co se děje na implantátech. Povrch není neutrálním pozadím. Stanovuje počáteční podmínky pro následnou buněčnou reakci. V praxi to znamená, že dva povrchy s podobnou mechanickou pevností mohou vést k zcela odlišným průběhům hojení jednoduše proto, že vytvářejí první vrstvu adsorbovaných proteinů odlišně.
Stejně důležité jsou interakce mezi povrchem a mikroorganismy. V kapitole o biofilmech autoři poznamenávají, že smáčivost, náboj, drsnost a topografie ovlivňují bakteriální adhezi. Obecný trend je takový, že větší drsnost často podporuje bakteriální adhezi a hydrofobní povrchy častěji usnadňují bakteriální přilnutí. Zároveň se nejedná o pravidlo bez výjimek, protože extrémně superhydrofilní nebo superhydrofobní systémy mohou působit jako inhibitory biofilmu prostřednictvím jiného mechanismu. V praxi to slouží jako varování: řešení prospěšné pro integraci tkáně nebude vždy stejně prospěšné pro kontrolu bakteriální kolonizace.
Níže je uvedeno video v angličtině s názvem BIOE 5820 Biomaterials Protein Adsorption, což je přednáška o adsorpci proteinů na površích biomateriálů.
Proč modifikovat povrch namísto celého materiálu
To je hlavní důvod povrchové modifikace. Pokud je objemový materiál zodpovědný za nosnost, trvanlivost a mechanickou funkci, zatímco povrch je zodpovědný za biointerakci, dává největší smysl zachovat to, co v objemu funguje dobře, a modifikovat pouze to, co přichází do kontaktu s tkání. Přesně tak to formulují autoři kapitoly o fyzikálně-chemických povrchových úpravách: cílem je zachovat klíčové fyzikální vlastnosti biomateriálu a změnit pouze vnější vrstvu, aby se zlepšila nebo modulovala biologická odezva na rozhraní tkáň–implantát.
Tento přístup má několik velmi praktických výhod. Za prvé, není třeba opouštět materiál, který je mechanicky a technologicky dobře známý. Titan, ocel, technické polymery nebo elastomery mohou i nadále plnit svou strukturální nebo funkční roli. Zadruhé, biologickou reakci lze přesněji přizpůsobit dané aplikaci. Chceme jiný povrch pro kostní implantát, jiný pro součástku přicházející do styku s krví a ještě jiný pro katétr, kde může být prioritou omezení adsorpce bílkovin a adheze buněk nebo bakterií. Za třetí, modifikace povrchu umožňuje vylepšit zařízení, aniž by bylo nutné kompletně přepracovat celou strukturu. Kniha dokonce zdůrazňuje, že u zařízení, která jsou již v klinické praxi dobře zavedena, je to způsob, jak změnit biointerakce, aniž by bylo nutné produkt přepracovat, přestrojit výrobu nebo přeškolit zdravotnický personál na používání nového řešení.
Existuje však jedna podmínka: je třeba rozlišovat mezi skutečnou modifikací rozhraní a kosmetickou změnou v popisu. Pouhé prohlášení, že materiál je „bioaktivní“ nebo „antifoulingový“, má malý význam, pokud není známo, jak vlastně povrch vypadá ve své konečné podobě po zpracování a sterilizaci. Zdroj uvádí, že analyzovaný vzorek by měl co nejvíce odpovídat materiálu nebo zařízení ve formě používané pro biologické testování nebo implantaci. To je důležité, protože povrch vystavený vzduchu nemusí být stejný jako povrch, který materiál vykazuje ve vodním prostředí těla.
Tři hlavní metody povrchové úpravy
První metoda spočívá ve změně stávajícího povrchu bez přidání samostatné nové vrstvy. Atomy, molekuly a vazby již přítomné ve vnější vrstvě materiálu lze chemicky nebo fyzikálně transformovat. Do této skupiny patří mimo jiné leptání, chemická aktivace, mechanické zdrsnění, iontová implantace a některé laserové úpravy. Jde o to, že k implantátu „nepřipojujeme“ novou vrstvu, ale spíše přetváříme jeho vlastní povrch. To je výhodné tam, kde je důležitá silná integrace úpravy se substrátem, stejně jako snížení rizika delaminace a změna vlastností, jako je reaktivita, smáčivost, odolnost proti korozi, tvrdost nebo bioaktivita. Zdroj ukazuje například, že implantace iontů může zlepšit odolnost proti opotřebení nebo korozi a laserové zpracování může kontrolovaně měnit drsnost povrchu, krystalinitu a chemické složení.
Druhý přístup zahrnuje nanesení nové vrstvy nebo povlaku. V tomto případě se na stávající povrch nanese materiál s odlišným složením nebo vlastnostmi. Může se jednat o tenkou vrstvu, naroubovanou vrstvu, polymerní povlak nebo systém navržený jako nešpinivý povrch. Tato strategie je obzvláště cenná, když má substrát ideální mechanické vlastnosti, ale je z biologického hlediska příliš „surový“. Dobrým příkladem jsou povrchy odolné proti nespecifické adsorpci proteinů. Jejich mechanismus obvykle spočívá v silné hydratační vrstvě, která působí jako energetická a fyzikální bariéra pro proteiny. V kapitole o nešpinících površích autoři popisují dvě hlavní strategie pro aplikaci takových systémů: „graft-to-surface“, kde materiál adsorbuje nebo se váže z roztoku, a „graft-from-surface“, kde polymerní kartáče rostou z povrchu. První přístup je technologicky jednodušší; druhý snáze dosahuje vysoké hustoty uspořádání, ale obvykle vyžaduje složitější chemii a přípravu substrátu.
V praxi má tento rozdíl inženýrský význam. Pokud chceme pouze rychle omezit ukládání proteinů na relativně jednoduchém substrátu, může stačit jednodušší řešení. Pokud však požadujeme trvanlivou, nepropustnou a hustě uspořádanou antiadsorpční vrstvu, nemusí stačit pouhé „nalepení“ molekul na povrch. Kniha jasně zdůrazňuje, že volba metody určuje hustotu uspořádání, počet defektů a trvanlivost konečného povrchu. To znamená, že povlaky se nehodnotí pouze na základě jejich deklarované chemie, ale podle toho, zda ve skutečnosti tvoří homogenní, stabilní rozhraní za provozních podmínek.
Třetí přístup zahrnuje vytváření vzorů, textur a topografií. Zde se primární pozornost nezaměřuje na změnu chemického složení, ale na změnu geometrie toho, co buňka nebo protein „vidí“. Zdroj zdůrazňuje, že topografie povrchu ovlivňuje adhezi, proliferaci, migraci, diferenciaci a genovou expresi buněk. Buňky reagují jak na mikro-, tak na nanoměřítkové vlastnosti, nikoli pouze na pouhou přítomnost materiálu. Ve studiích citovaných v knize různé výšky, velikosti a rozestupy topografických struktur měnily stupeň mineralizace, orientaci buněk, buněčnou adhezi a diferenciaci. To znamená, že textura není pouhou ozdobou nebo vedlejším účinkem zpracování, ale aktivním nástrojem pro řízení biologických reakcí.
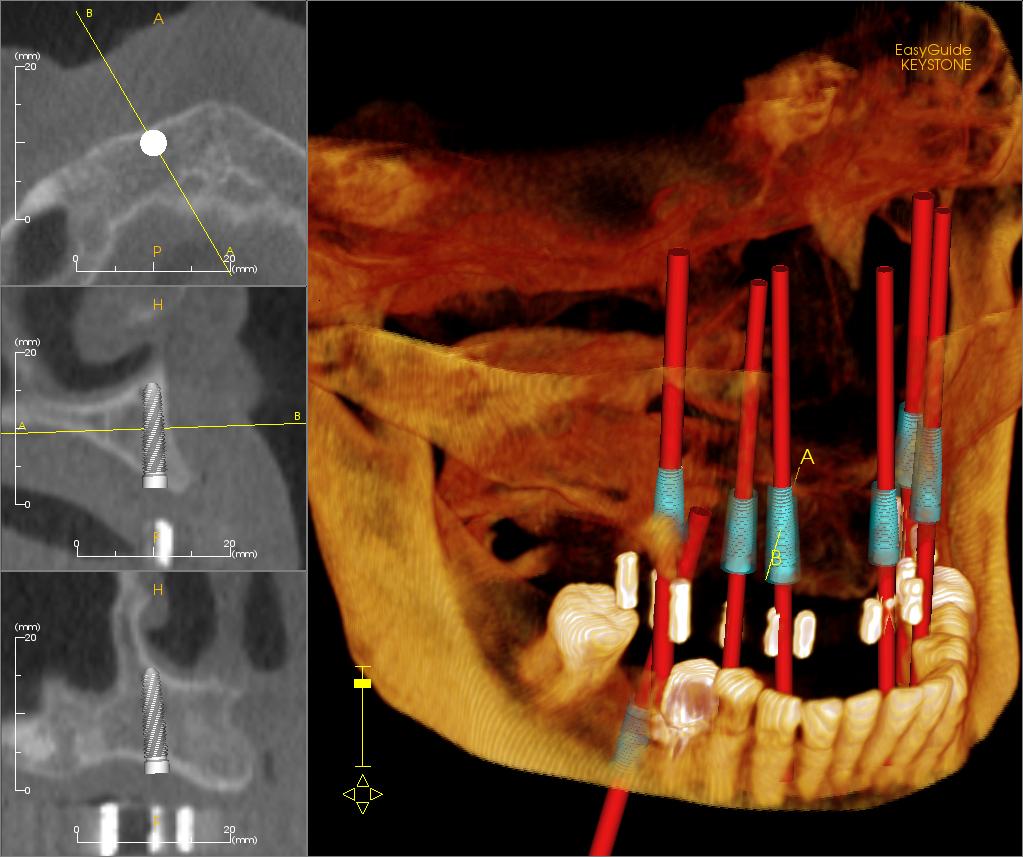
To je zvláště patrné u kostních a zubních implantátů. Kniha popisuje, jak vhodně drsná nebo trojrozměrná povrchová vrstva může urychlit rané fáze hojení, podporovat ukládání fibrinu, vazbu integrinů a mikromechanické propojení s kostí. Výsledkem je zvýšení smykové pevnosti na rozhraní implantát–kost a zlepšení přenosu zatížení. To je dobrý příklad toho, jak texturování není „slepým vylepšením“, ale pokusem o řízení konkrétního mechanismu na rozhraní. Je však třeba opatrnosti, protože stejná drsnost, která napomáhá osseointegraci, může v jiné aplikaci zvýšit riziko bakteriální kolonizace nebo bránit kontrole povrchu.

Časté chyby, úskalí a falešné stopy
Nejčastější chybou je ztotožňování „lepšího materiálu“ s „lepší biologickou reakcí“. Je to příliš zjednodušující. Pevnost, odolnost proti únavě a chemická stabilita zatím nevysvětlují, co se stane na rozhraní s tkání. U biomateriálů můžete mít vynikající konstrukční materiál a špatné biologické rozhraní. Můžete také čelit opačnému problému: vysoce biologicky aktivní povrch namontovaný na substrátu, který nesplňuje mechanické požadavky. Právě proto je při návrhu užitečná premisa, že materiál poskytuje implantátu pevnost, zatímco povrch určuje reakci těla. Nutí nás to oddělit dvě otázky, které jsou v klasickém inženýrství často spojovány dohromady.
Druhým úskalím je přesvědčení, že jediná vlastnost povrchu vyřeší celý problém. V praxi neexistuje žádné univerzální „nastavení biokompatibility“. Zvýšení hydrofilnosti může omezit adsorpci určitých proteinů, ale nemusí nutně zlepšit integraci s tkání. Zvýšení drsnosti může podpořit reakci osteoblastů, ale nemusí být prospěšné pro prostředí s rizikem infekce. Samotná kniha poznamenává, že zatím není známo, který parametr je pro každou konkrétní biologickou reakci nejdůležitější, takže proměnné je třeba měřit a korelovat nezávisle. Jedná se o velmi důležitou metodologickou zásadu: místo hledání jediného magického čísla je třeba sestavit mapu vztahů mezi několika vlastnostmi rozhraní a konkrétním klinickým cílem.
Třetí úskalí se týká tloušťky modifikace. Autoři kapitoly o fyzikálně-chemických modifikacích zdůrazňují, že modifikace by měly být co nejtenčí. V ideálním případě by stačilo změnit pouze několik nejvnějších molekulárních vrstev – v řádu několika nanometrů –, avšak v praxi musí být vrstvy někdy silnější, aby byla zajištěna rovnoměrnost a trvanlivost. Příliš silný povlak může změnit mechanické a funkční vlastnosti zařízení a také zvýšit riziko praskání a delaminace. To je zvláště důležité v případech, kdy je implantát vystaven únavě nebo tření. Vrstva, která vypadá slibně z biologického hlediska, ale po určité době se mechanicky odlupuje, problém nevyřeší; pouze vytvoří nový.
Čtvrtým omylem je považovat povrch za statický stav. Zdroj dokazuje, že některé materiály mohou při přechodu ze vzduchu do vodního prostředí zvrátit svou povrchovou organizaci. Povrch měřený „v suchých podmínkách“ nemusí být stejný povrch, s nímž se v těle setkávají proteiny a buňky. To má přímé důsledky pro výzkum. Pokud analýza povrchu nezohledňuje provozní prostředí, může dojít k optimalizaci parametru, který po implantaci přestane mít stejnou hodnotu nebo význam.
Kdy je zapotřebí pokročilejší teorie
Pokročilý přístup se stává nezbytným, když intuitivní pojmy jako „hladší“, „hydrofilnější“ nebo „drsnější“ již nestačí. Příkladem jsou povrchy odolné proti znečištění. Jejich funkce nevyplývá pouze ze skutečnosti, že jsou kluzké, ale ze skutečnosti, že tvoří stabilní hydratační vrstvu, jejíž odstranění je z energetického hlediska nevýhodné pro adsorbující proteiny. Kniha ukazuje, že hydrofilní materiály na bázi PEG vážou vodu prostřednictvím vodíkových vazeb, zatímco zwitteriontové materiály to dokážou ještě silněji prostřednictvím elektrostaticky indukované hydratace. Na této úrovni je třeba zohlednit nejen funkční chemii, ale také hustotu uspořádání řetězců, konformační svobodu a stabilitu ukotvení vrstvy.
Pokročilá teorie je rovněž potřebná, pokud má povrch nejen nezasahovat, ale aktivně řídit chování buněk. V takových případech záleží na geometrii v mikro- a nanoměřítku, lokální mechanice, velikosti, výšce a rozestupech topografických prvků a někdy dokonce i na uspořádanosti či neuspořádanosti vzoru. Právě proto dnešní výzkum využívá topografické matice a systematičtější screening povrchů. Nejde o akademickou složitost tématu, ale o skutečnost, že buňky skutečně rozlišují mezi měřítky a vzory prvků a biologická odezva přestává být lineární funkcí jediného parametru.
Proč je povrch implantátu tak důležitý? – shrnutí
U biomateriálů není úspěch implantátu často určen samotným objemovým materiálem, ale povrchem, který se tělu prezentuje. Právě povrch je prvním bodem kontaktu s proteiny, buňkami a tělními tekutinami, a tím do značné míry určuje biokompatibilitu. Z tohoto důvodu zahrnuje rozumný návrh implantátu oddělení funkcí: objem má zajistit mechanické vlastnosti a trvanlivost, zatímco povrch má vyvolat odpovídající biologickou reakci. To je základem celé logiky úpravy povrchu bez změny celého materiálu. Lze přetvořit stávající vnější vrstvu, aplikovat nový povlak nebo navrhnout vzor a topografii, které ovlivní adsorpci proteinů, chování buněk, integraci do tkáně nebo odolnost proti znečištění. Existuje však jedna podmínka: úprava musí být skutečně mezifázová, tenká, trvanlivá a přizpůsobená konkrétnímu klinickému cíli. Právě proto není povrch u biomateriálů pouhým detailem povrchové úpravy, ale jedním z hlavních nástrojů při návrhu implantátů.