Biomatériaux métalliques

Table des matières
Les métaux jouent un rôle complètement différent, dans l’ingénierie biomédicale, que les céramiques ou les polymères. Ces métaux se distinguent principalement par leurs excellentes propriétés mécaniques, ainsi que leur conductivité électrique et thermique élevée. Cela est dû à la nature même de la liaison métallique. Certains électrons sont délocalisés, formant un nuage d’« électrons libres » qui sont responsables de la conductivité et de la liaison forte, bien que non directionnelle, entre les ions métalliques. Cette structure permet aux atomes du réseau cristallin de se déplacer les uns par rapport aux autres sans perturber l’ordre, ce qui confère aux métaux leur plasticité caractéristique et leur capacité à subir d’importantes déformations, sans destruction soudaine.
Ce trait distinctif est utilisé de manière très consciente dans les biomatériaux. Les métaux servent à la fois de substituts passifs aux tissus durs, notamment dans les prothèses de hanche et de genou, les plaques osseuses, les vis, les clous intramédullaires, les implants dentaires. Ils servent aussi de matériaux pour des dispositifs plus « actifs », tels que les stents vasculaires, les guides de cathéter, les fils orthodontiques et les implants cochléaires. Dans ces applications, ce n’est pas uniquement la résistance qui compte, mais aussi la formabilité, l’élasticité, la conductivité et la facilité de la fabrication de précision.
L’histoire des biomatériaux métalliques a commencé avec les alliages d’acier. Le premier alliage développé spécifiquement pour les applications orthopédiques était l’acier au vanadium, utilisé pour fabriquer des plaques et des vis destinées à la fixation des fractures (connues sous le nom de plaques Sherman). Au fil du temps, ce matériau a été remplacé par les aciers inoxydables, puis par les alliages de cobalt et de chrome et les alliages de titane. Ces alliages utilisent un certain nombre de métaux, tels que fer (Fe), chrome (Cr), cobalt (Co), nickel (Ni), titane (Ti), tantale (Ta), niobium (Nb), molybdène (Mo) et tungstène (W). Ces métaux, à forte dose, sont toxiques pour l’organisme, mais sous forme d’alliages stables et résistants à la corrosion, sont bien tolérés.
Le principal défi lié à l’utilisation des métaux est la corrosion dans l’environnement in vivo. Les produits de corrosion peuvent entraîner à la fois un affaiblissement de l’implant lui-même et des réactions biologiques indésirables qui peuvent être une inflammation locale, une décoloration des tissus, des lésions organiques ou des réponses immunitaires. C’est pourquoi l’ingénierie moderne des biomatériaux métalliques se concentre sur les alliages capables de former des couches protectrices durables et passives à leur surface et sur la modification consciente de la surface, afin de combiner une bonne résistance générale, une haute résistance à la corrosion en particulier et une réponse biologique appropriée.
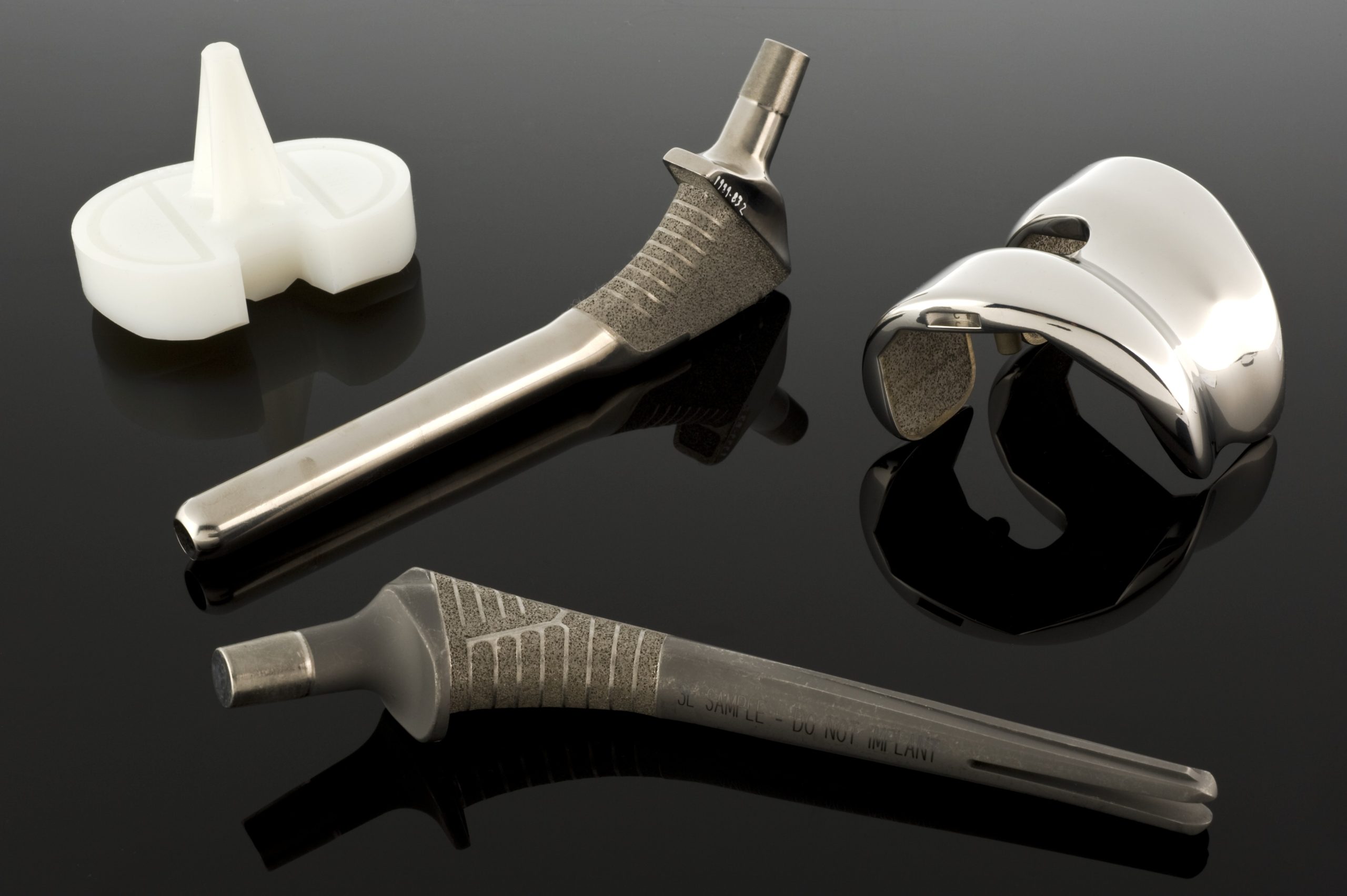
Les aciers inoxydables comme matériaux d’implants
L’acier inoxydable a été l’un des premiers matériaux à remplacer avec succès l’acier au vanadium dans les implants. Au départ, était utilisé de l’acier 18-8 (type 302), contenant environ 18 % de chrome et 8 % de nickel, qui offrait une résistance à la corrosion nettement supérieure à celle des classiques aciers au carbone. Au fil du temps, une variante du 18-8 avec ajout de molybdène (18-8sMo) est apparue, connue aujourd’hui sous le nom d’acier 316, suivie d’une modification avec une teneur réduite en carbone, nommé l’acier 316L. La réduction de la teneur en carbone d’environ 0,08 % à un maximum de 0,03 % diminue la tendance des carbures de chrome à se former aux joints de grains, ce qui améliore la résistance à la corrosion dans les environnements riches en chlorure tels que les fluides corporels.
Le chrome est principalement responsable de la résistance à la corrosion des aciers inoxydables. Même avec une teneur en Cr de 11 %, une fine couche d’oxyde protectrice se forme à la surface, donnant à l’acier un état dit passif. L’ajout de molybdène augmente la résistance à la corrosion par piqûres, dans les environnements chlorés, rendant ainsi les aciers 316/316L plus adaptés aux conditions physiologiques. Le nickel, quant à lui, stabilise la phase austénitique (structure γ, fcc) à température ambiante, rendant le matériau non magnétique et améliorant sa résistance à la corrosion.
Les aciers austénitiques ne peuvent pas être durcis par un traitement thermique conventionnel, mais ils réagissent très bien à l’écrouissage. Cela permet d’ajuster un large éventail de propriétés mécaniques, allant de structures plus ductiles et souples jusqu’à des structures nettement durcies, présentant une résistance élevée à la traction. Les données mécaniques relatives à l’acier 316L montrent que, selon le degré de déformation à froid, différentes combinaisons de résistance et de ductilité peuvent être obtenues, ce qui est important pour adapter le matériau à la fonction spécifique de l’implant.
Malgré leurs nombreux avantages, les aciers 316 et 316L ne sont toutefois pas des matériaux idéaux. Dans des conditions de forte contrainte, en particulier dans les zones où l’accès à l’oxygène est limité, comme autour de filetages de vis ou de connexions de plaques osseuses, une corrosion par crevasses et par piqûres peut se produire et à long terme, une corrosion par fatigue peut également apparaître.
C’est pourquoi les aciers inoxydables sont le plus souvent utilisés dans les implants temporaires tels que les plaques, les vis, les clous et les fils de fixation, qui peuvent être retirés une fois l’os guéri. Pour améliorer leurs propriétés, des modifications de surface sont largement utilisées, du polissage et de la passivation à l’acide nitrique à l’anodisation ou à l’implantation d’azote par décharge luminescente, ce qui augmente la résistance à la corrosion, à l’usure et à la fatigue.
Alliages de cobalt et de chrome
Lorsque les exigences mécaniques dépassent les capacités des aciers inoxydables, les alliages de cobalt et de chrome entrent en jeu. Il existe deux grands groupes d’alliages de ce type dans les biomatériaux, qui sont : l’alliage CoCrMo coulé, utilisé notamment dans les cupules et les têtes d’endoprothèses et l’alliage CoNiCrMo forgé, utilisé dans les composants soumis à des charges élevées tels que les tiges de prothèses de hanche ou de genou. Les normes ASTM décrivent plusieurs versions de ces matériaux (F75, F90, F562, F563), mais dans la pratique clinique, le CoCrMo et le CoNiCrMo dominent.
Le cobalt et le chrome forment une solution solide jusqu’à environ 65 % de Co et l’ajout de molybdène provoque un affinage du grain et, par conséquent, une résistance accrue après moulage ou forgeage. Le chrome joue donc ici un double rôle… Il augmente la résistance à la corrosion, en formant une couche d’oxyde passive et participe au renforcement de la solution. En pratique clinique, les alliages Co-Cr se caractérisent par un module d’élasticité très élevé, qui est de l’ordre de 220 à 234 GPa, supérieur à celui des aciers inoxydables et présente une très bonne résistance à l’usure.
Cependant, cette rigidité élevée a des conséquences. Un implant trop rigide peut supporter une charge trop importante, entraînant un effet de protection envers les contraintes, c’est-à-dire une réduction de la charge sur l’os du patient et sa résorption progressive. Bien que la signification clinique de cet effet ne soit pas tout à fait claire, il s’agit d’un facteur important dans la conception et la forme des tiges prothétiques. D’autre part, la dureté et la résistance à l’abrasion font des alliages de cobalt et de chrome un excellent choix pour les couples de frottement « métal-métal », où il est indispensable de minimiser l’usure à long terme. Les études sur les endoprothèses à long terme avec de tels couples indiquent un taux d’usure linéaire très faible, de l’ordre de quelques micromètres par an.
Une autre question importante concerne la libération d’ions par les alliages Co-Cr et leur toxicité potentielle. Des expériences menées dans une solution de Ringer ont montré que le taux de libération de nickel par l’alliage CoNiCrMo et l’acier 316L est très similaire après un certain temps, même si l’alliage de cobalt contient environ trois fois plus de nickel. Des études in vitro ont montré que les particules de cobalt peuvent être toxiques pour les cellules responsables de la formation osseuse, tandis que les particules de chrome et d’alliage Co-Cr sont beaucoup mieux tolérées. Des concentrations élevées d’ions Co et Ni perturbent clairement le métabolisme cellulaire dans les cultures, tandis que les ions chrome présentent une toxicité moindre.
Le titane et ses alliages
Parmi les métaux utilisés comme biomatériaux, le titane occupe une place particulière. Dans la série électrochimique, c’est un élément « actif », mais dans un environnement physiologique, il est recouvert d’une couche d’oxyde passive très stable, grâce à laquelle son courant de corrosion dans les solutions physiologiques est extrêmement faible, de l’ordre de 10⁻⁸ A/cm². En pratique, les implants en titane restent visuellement inchangés après une longue période dans le corps.
Le titane pur (cp-Ti) et l’alliage Ti–6Al–4V qui est le plus populaire, combinent une très bonne résistance à la corrosion et un rapport résistance/poids favorable. Leur module d’élasticité est inférieur à celui de l’acier ou des alliages Co–Cr, ce qui les rapproche de l’os et réduit potentiellement le risque de protection contre les contraintes. En revanche, le titane n’est pas aussi rigide ni aussi résistant à la traction que les meilleurs aciers ou alliages de cobalt. La conception d’éléments porteurs nécessite donc une analyse précise des contraintes et souvent une section transversale plus importante.
Au cours des dernières décennies, des alliages de titane, présentant un module d’élasticité réduit et une résistance à la corrosion accrue, ont également été développés. Ils contiennent notamment du Nb et du Zr, par exemple Ti–13Nb–13Zr et sont spécialement conçus pour les prothèses articulaires. En outre, le durcissement de surface des alliages de titane (par exemple, traitement thermochimique ou nitruration) a été développé, ce qui permet de combiner une bonne biocompatibilité du substrat, avec une résistance élevée à l’usure dans les zones de frottement.
Les alliages nickel-titane (NiTi), qui présentent une mémoire de forme et une superélasticité, constituent un groupe particulier. Grâce à la transformation martensitique, ils peuvent reproduire une forme préalablement enregistrée lorsqu’ils sont chauffés au-dessus de la température de transformation ou présenter une déformabilité élastique très élevée dans une plage de contraintes étroite. Cette caractéristique est notamment utilisée dans les stents vasculaires, les arcs orthodontiques et les guides de cathéter, permettant alors une insertion atraumatique des dispositifs et leur expansion stable après dilatation.
Dans le cas du titane, les propriétés de surface sont particulièrement importantes. Des études montrent que la rugosité et la chimie de surface régulent le comportement des ostéoblastes et des cellules ostéogéniques. Elles influencent l’adhérence, la prolifération et la production de facteurs de croissance et de cytokines. Un traitement chimique approprié de la surface du titane et de ses alliages peut les rendre bioactifs, c’est-à-dire capables de former une couche d’apatite au contact des fluides corporels, ce qui favorise la liaison directe avec l’os.

Métaux en dentisterie et autres applications spéciales
Les métaux précieux et les métaux communs sont tous deux utilisés en dentisterie. L’or est pratiquement résistant à la corrosion, d’une résistance de type immunitaire, il offre une excellente durabilité et une stabilité chimique dans les reconstructions prothétiques. Cependant, ses limites sont sa densité élevée, sa résistance insuffisante pour les charges lourdes et son coût, ce qui signifie qu’il n’est pratiquement pas utilisé en orthopédie.
L’amalgame dentaire, un alliage d’argent, d’étain et de mercure, est couramment utilisé. Bien que les phases individuelles de ce matériau soient passives à un pH neutre, dans la pratique, l’amalgame se corrode souvent, en particulier en présence de différences d’aération sous la plaque bactérienne et de microcellules galvaniques locales. Il s’agit effectivement du matériau le plus sujet à la corrosion, utilisé en dentisterie, ce qui se manifeste par une décoloration et la formation de produits de corrosion à la surface des obturations.
Le groupe des métaux spéciaux comprend également les métaux du groupe du platine et de leurs alliages, utilisés lorsque la résistance chimique et le contrôle de la conductivité sont essentiels, ainsi que les alliages Ni-Cu et d’autres systèmes utilisés en hyperthermie, c’est-à-dire le chauffage délibéré de tissus cancéreux à l’aide d’un champ magnétique induit. Ces types d’alliages sont conçus de manière que leur réponse thermique dans un champ électromagnétique soit bien contrôlée, ce qui permet de fournir avec précision l’énergie thermique à la tumeur.
Corrosion des implants métalliques dans un environnement biologique
La corrosion est un phénomène central pour les biomatériaux métalliques. Dans le corps, nous avons affaire à un fluide électrolytique contenant des ions (Na⁺, Cl⁻, HCO₃⁻, phosphates), un pH variable et des différences de potentiel entre différentes zones, tous ces facteurs favorisent les réactions électrochimiques.
Les diagrammes de Pourbaix, qui montrent la relation entre le potentiel électrochimique et le pH, sont utilisés pour décrire la stabilité des métaux. Ils distinguent les zones de corrosion (activité), de passivité et d’immunité. Dans le corps humain, les différents fluides ont des niveaux de pH et d’oxygénation différents. Le liquide tissulaire a généralement un pH d’environ 7,4, mais à proximité d’une plaie, il peut descendre jusqu’à 3,5 et dans une plaie infectée, il peut monter jusqu’à 9,0. Cela signifie qu’un métal qui fonctionne bien, dans une zone du corps, peut se corroder dans une autre.
Cependant, les diagrammes de Pourbaix ont leurs limites. Ils sont basés sur des états d’équilibre dans un système simple métal-eau-produits de réaction. La présence d’ions chlorure ou de molécules organiques complexes peut modifier considérablement le comportement du métal et la passivité prévue peut se révéler trop optimiste dans la pratique. C’est pourquoi sont utilisées, en complément de ces diagrammes, des courbes de polarisation qui permettent de déterminer le courant de corrosion et, sur cette base, de calculer le nombre d’ions libérés dans les tissus et le taux de perte de matière. Nous pouvons également mesurer la perte de masse de l’échantillon durant son exposition dans une solution similaire aux fluides corporels.
La corrosion des matériaux destinés à l’implantation peut prendre différentes formes. Une corrosion uniforme entraîne une perte de matière relativement homogène, mais les formes localisées sont beaucoup plus dangereuses. La corrosion par piqûres provoque des pertes profondes et localisées, car les aciers inoxydables y sont particulièrement sensibles, en présence de chlorures. La corrosion caverneuse se produit dans les zones où l’accès à l’oxygène est limité, comme les espaces entre la vis et la plaque, là où les conditions chimiques locales (pH, concentration ionique) diffèrent considérablement de celles de l’environnement environnant. Le frottement est une corrosion associée aux micro-mouvements de deux surfaces en contact, ce qui fait que l’abrasion mécanique détruit la couche passive, exposant le métal frais et accélérant sa corrosion.
La corrosion sous contrainte et la corrosion par fatigue sont des formes particulières de corrosion. En présence de contraintes mécaniques, notamment répétitives, le taux de corrosion peut augmenter, ce qui fait que les microfissures peuvent se propager plus rapidement. Dans les implants en acier inoxydable, par exemple, des fractures de clous et de broches de hanche ont été observées lorsque des charges de flexion et un environnement physiologique agressif étaient simultanément présents. Dans de tels cas, il est difficile de parler de corrosion « pure ». Nous pouvons dire qu’il s’agit toujours d’une interaction dynamique entre la chimie, la mécanique et la microstructure.
De multiples métaux se comportent différemment, à cet égard.
Les métaux précieux, tels que l’or, sont pratiquement résistants à la corrosion, car leur potentiel électrochimique standard est positif et, dans les diagrammes de Pourbaix, ils occupent la zone d’immunité.
Le titane et les alliages Co-Cr sont basés sur la passivité, étant donné qu’ils forment une couche d’oxyde bien adhérente et étanche, grâce à laquelle leurs courants de corrosion sont très faibles et la surface reste stable.
Les aciers inoxydables bénéficient également de la passivité du chrome, mais leur couche passive est moins stable, ce qui les rend plus sensibles à la corrosion par piqûres et par crevasses.
L’amalgame dentaire, en revanche, bien que partiellement passif sur le plan thermodynamique, est en pratique un matériau très sensible à la corrosion, en particulier en présence de biofilm.
Fabrication et traitement d’implants métalliques
La fabrication d’implants métalliques ne consiste donc pas uniquement à façonner la géométrie, mais à contrôler la microstructure et l’état de surface, qui déterminent la résistance à la fatigue, la résistance à la corrosion et la réponse biologique.
Dans le cas des aciers inoxydables, il est primordial que les aciers austénitiques durcissent très rapidement, sous compression. Cela signifie que lors du travail à froid (laminage, étirage, pliage), leur résistance augmente, mais, simultanément leur plasticité diminue. Afin de rétablir le niveau de déformabilité requis, est utilisé un recuit intermédiaire, dans lequel il faut éviter les températures et les durées propices à la précipitation de carbures de chrome aux joints de grains, qui affaiblissent la résistance à la corrosion. Après le formage, les composants sont nettoyés, désoxydés (chimiquement ou par abrasion) et passivés, généralement dans une solution d’acide nitrique conformément à la norme ASTM F86.
Les alliages Co-Cr se comportent différemment. Ils sont notamment très sensibles au durcissement lors de la déformation, ce qui rend souvent difficile le forgeage conventionnel. C’est pourquoi les composants à géométrie complexe, tels que les têtes et les cupules prothétiques, sont souvent fabriqués par moulage de précision (méthode dite à cire perdue). Le processus consiste à préparer un modèle en cire précis, à le recouvrir d’un matériau réfractaire, à fondre la cire et à couler l’alliage Co-CrMo liquide dans le moule à haute température. La température du moule et le temps de refroidissement ont une incidence sur la taille des grains et la taille et la répartition des carbures. Ainsi, une microstructure fine augmente la résistance, mais peut réduire la résistance à la rupture fragile, tandis que des grains et des carbures plus gros améliorent la ductilité au détriment de la résistance. Le concepteur doit donc trouver un compromis entre résistance et… résistance à la rupture !
Pour les alliages de titane, les processus de moulage, de forgeage et de traitement thermique, ainsi que le traitement de surface, sont également essentiels. Le titane nécessite une atmosphère protectrice durant le traitement à haute température, car il réagit facilement avec l’oxygène et l’azote pour former des couches superficielles fragiles. Après le traitement mécanique initial, les surfaces des implants en titane sont sablées, gravées à l’acide, anodisées ou soumises à une combinaison de ces procédés, ce qui permet de bénéficier d’une rugosité micrométrique favorable et d’une couche d’oxyde modifiée. Des études indiquent que les surfaces ainsi préparées favorisent une croissance osseuse plus rapide et la formation d’une liaison mécanique solide et, potentiellement, chimique.
Les processus de fabrication des alliages à mémoire de forme constituent une catégorie à part. Dans leur cas, il est indispensable de contrôler avec précision la composition chimique ainsi que le traitement thermique, car tous deux déterminent les températures de transformation martensitique et la plage de superélasticité. Les stents ou les arcs orthodontiques en NiTi doivent atteindre la déformation souhaitée et reprendre leur forme dans une plage de température strictement définie, y compris dans des conditions physiologiques.
Biomatériaux métalliques – Résumé
Les biomatériaux métalliques constituent une vaste famille, dans laquelle chaque matériau occupe une niche fonctionnelle bien définie. Les aciers inoxydables, en particulier le type 316L, sont des matériaux relativement peu coûteux et faciles à traiter, dotés de bonnes propriétés mécaniques et d’une résistance suffisante à la corrosion. C’est pourquoi ils sont principalement utilisés dans les implants temporaires et les composants moins critiques.
Les alliages Co-Cr offrent une très grande résistance, en dureté et en résistance à l’usure, ce qui en fait le matériau de choix pour les cupules et les têtes prothétiques, ainsi que pour les tiges, dans lesquelles la durabilité sous des charges lourdes est importante. Le titane et ses alliages, qui combinent une très bonne résistance à la corrosion, un module d’élasticité favorable et une biocompatibilité élevée, sont devenus la « norme de référence » pour les implants à long terme, en particulier en orthopédie et en implantologie dentaire.
Les alliages spéciaux, tels que le NiTi à mémoire de forme, jouent également un rôle important, permettant des stratégies thérapeutiques totalement nouvelles, des stents auto-expansibles aux arcs orthodontiques superélastiques. L’or et les amalgames restent encore importants en dentisterie, bien que leurs applications soient en cours de révision et d’évolution, à la lumière d’exigences esthétiques et de sécurité.
Le dénominateur commun à tous les biomatériaux métalliques est la nécessité de contrôler la corrosion et l’interaction avec les tissus. Les diagrammes de Pourbaix, les courbes de polarisation, les essais de fatigue et les études de toxicité ionique constituent la base de la conception technique de ces matériaux. L’ingénierie de surface est tout aussi importante, car elle détermine la qualité de la couche passive, la résistance à l’usure, l’adhérence cellulaire et la nature de la liaison avec l’os.
Par conséquent, l’ingénierie moderne des biomatériaux ne considère pas les métaux de manière isolée, mais elle les traite comme faisant partie de systèmes complexes. Il en va ainsi d’un noyau métallique qui peut être recouvert de céramiques bioactives, entouré d’un composite polymère, ou bien associé à des structures céramiques poreuses qui favorisent la régénération.
Les métaux offrent une capacité de charge et une plasticité, les céramiques offrent une bioactivité et une résistance à l’abrasion et les polymères offrent une flexibilité et la capacité de former des structures souples. Ensemble, ils constituent les fondations de l’implantologie moderne, dont l’objectif n’est plus de « remplacer des parties », mais de parvenir à une reconstruction fonctionnelle, biologiquement intégrée à des organes.