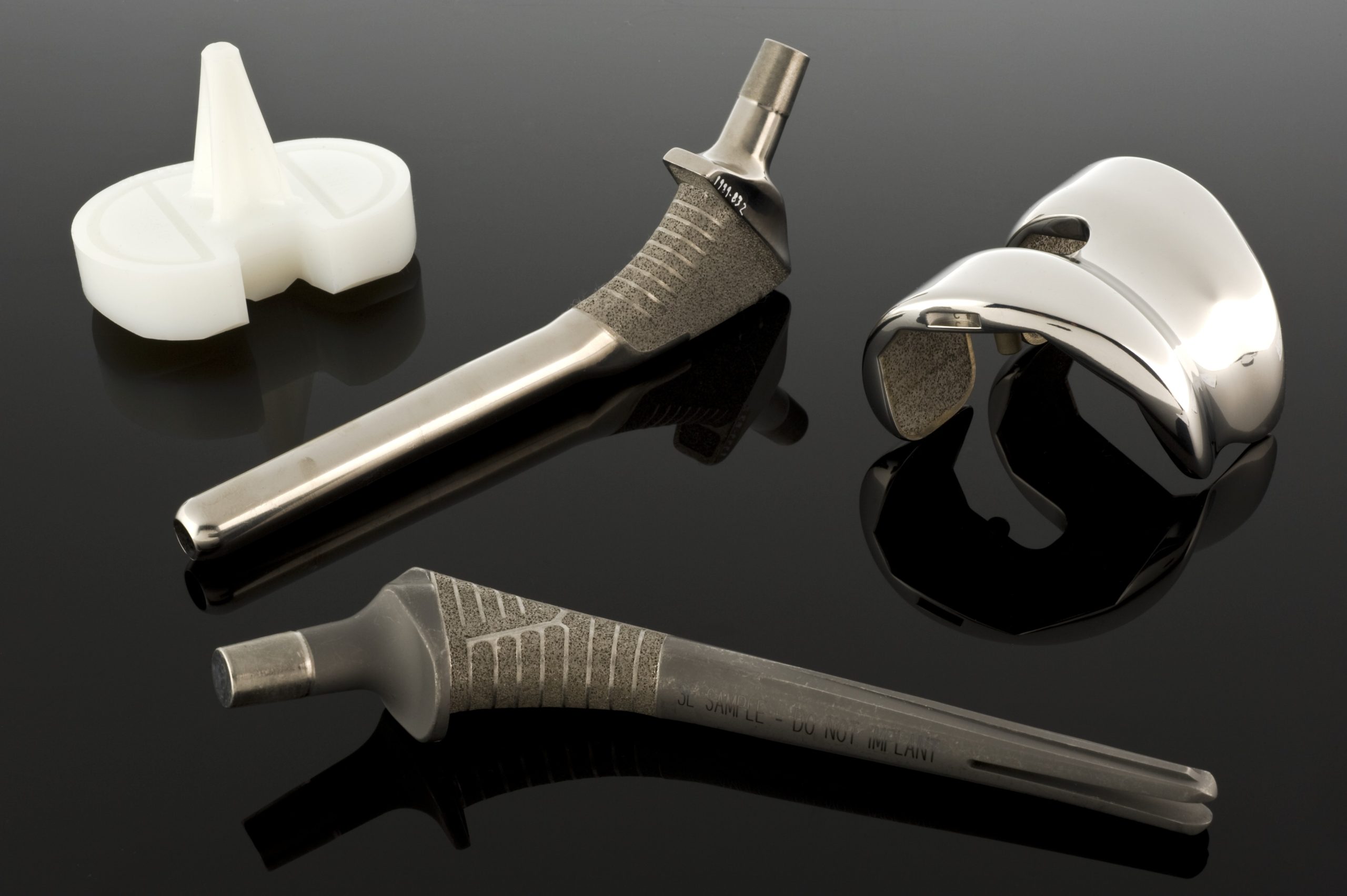
De ce este atât de importantă suprafața unui implant?
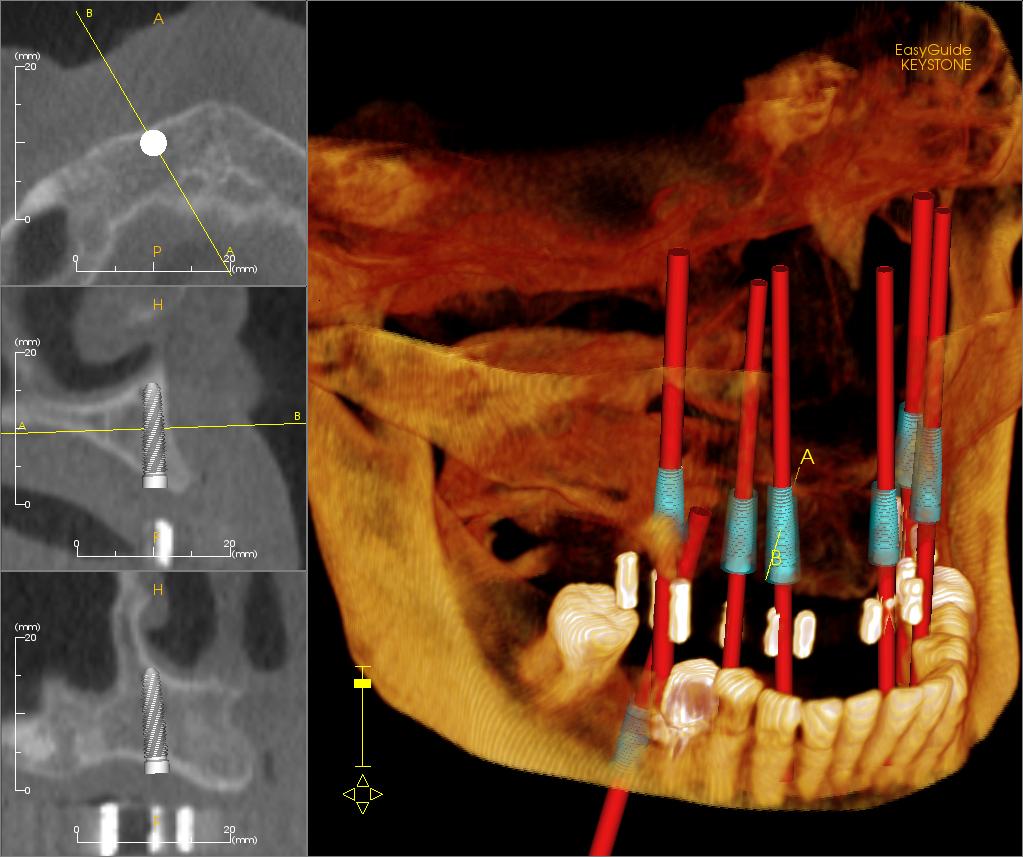
În ingineria biomaterialelor, este ușor să ne bazăm pe intuiția derivată din știința tradițională a materialelor: întrucât un implant trebuie să reziste la sarcini, să nu se corodeze, să nu se uzeze excesiv și să funcționeze ani de zile, succesul său ar trebui să depindă în primul rând de materialul „din interior”. Aceasta este doar o parte a adevărului. Materialul din interior este într-adevăr responsabil pentru rezistență, rigiditate, elasticitate, durabilitate și permeabilitate. Cu toate acestea, din perspectiva organismului, primul și cel mai important contact nu are loc cu întregul bloc de material, ci cu stratul său exterior. Acest strat este cel care intră în contact cu sângele, proteinele, celulele și fluidele corporale. În practică, aceasta înseamnă că un implant poate fi foarte bun din punct de vedere mecanic, dar problematic din punct de vedere biologic dacă suprafața sa transmite „semnalul greșit” țesuturilor.
Această observație schimbă modul în care gândim despre proiectarea implanturilor. În loc să ne întrebăm doar „din ce ar trebui să fie făcut implantul?”, trebuie să luăm în considerare cum ar trebui să fie suprafața implantului. În cazul biomaterialelor, răspunsul biologic nu este o simplă reflectare a compoziției chimice a întregii componente. Mai degrabă, este un răspuns la ceea ce se întâmplă la interfața material-țesut: chimia suprafeței, umectabilitatea, sarcina electrică, rugozitatea, organizarea și reactivitatea. De aceea, succesul unui implant este atât de des determinat nu de volumul materialului, ci tocmai la granița de fază.
Acest articol se bazează pe Biomaterials Science: An Introduction to Materials in Medicine, ed. William R. Wagner et al., ediția a 4-a, 2020. Conținutul următor este doar o prezentare generală a subiectului. Pentru cei interesați de subiect, recomandăm consultarea literaturii de specialitate.
Cum reacționează organismul la suprafața unui material?
Cel mai important punct de plecare este simplu: organismul nu „vede” întregul implant dintr-o dată. Mai întâi, el „citește” suprafața acestuia. Autorii lucrării Biomaterials Science afirmă în mod explicit că, în cazul materialelor care nu eliberează substanțe nedorite, transferul de informații de la material către proteine, celule și întregul organism are loc prin structura suprafeței. Prin urmare, organismul răspunde la chimia și organizarea specifică a stratului exterior, mai degrabă decât la proprietățile medii ale întregului material. Această schimbare aparent minoră de accent are o semnificație practică enormă, deoarece mută problema biocompatibilității de la nivelul „ce fel de aliaj sau polimer avem” la nivelul „cum arată și se comportă interfața sa”.
Este important să ne amintim că suprafața nu este pur și simplu o porțiune subțire a materialului care se comportă la fel ca interiorul său. Cartea subliniază faptul că suprafața este o zonă cu reactivitate particulară și diferă aproape inevitabil de masa materialului. Pentru un material metalic real, stratul exterior poate include nu numai oxid de metal, ci și apă adsorbită, compuși organici polari și contaminanți hidrocarburi. Pentru polimeri, zona unică a suprafeței poate varia de la aproximativ 10 la 100 nm. Acest lucru este important deoarece înseamnă că, chiar dacă materialul din interior este omogen, porțiunea sa biologic activă poate fi complexă din punct de vedere chimic și structural.
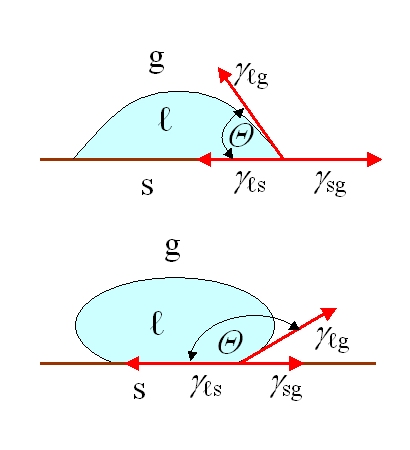
Din perspectivă biologică, suprafața nu este doar o chestiune de compoziție chimică. Autorii enumeră multe caracteristici care pot influența răspunsurile biologice: rugozitate, modele și topografie, umectabilitate, mobilitate de suprafață, compoziție chimică, sarcină electrică, cristalinitate, modul de elasticitate și eterogenitate. În același timp, ei notează sincer că nu este încă posibil să se identifice o singură caracteristică universală care să fie cea mai importantă pentru fiecare răspuns biologic. În practică, aceasta este o lecție foarte orientată spre inginerie; nu trebuie să ne bazăm proiectarea pe un singur slogan parametric, cum ar fi „să creștem rugozitatea” sau „să facem suprafața mai hidrofilă”, deoarece răspunsul organismului este rezultatul interacțiunii mai multor caracteristici simultan.
Această abordare explică de ce două implanturi realizate din același material de bază se pot comporta diferit din punct de vedere biologic. O schimbare în procesare, sterilizare, depozitare sau ambalare este suficientă pentru a altera starea suprafeței. Cartea evidențiază chiar și aspecte banale precum amprentele digitale, aditivii care migrează din ambalaj sau contaminanții proveniți de la hârtie sau folie. În laborator, acesta este un detaliu, dar în realitate, tocmai astfel de detalii ne pot determina să testăm o suprafață care nu este cea prezentă efectiv pe implantul utilizat clinic.

Cum se traduce suprafața în biocompatibilitate
Dacă suprafața este limbajul principal de comunicare între implant și organism, trebuie să ne întrebăm cum arată acest dialog. Unul dintre mecanismele cheie este adsorbția proteinelor. Sursa subliniază că, după implantarea unui biomaterial sintetic, proteinele adezive se adsorb pe suprafața acestuia foarte rapid, în câteva secunde. În acest fel, un material care în sine nu are motive de recunoaștere biologică devine „lizibil” pentru organism. Cu alte cuvinte, celulele adesea nu reacționează direct la materialul pur, ci la stratul de proteine care se formează pe suprafața acestuia la scurt timp după contactul cu organismul.
Acest lucru are o implicație fundamentală pentru înțelegerea biocompatibilității. Biocompatibilitatea nu înseamnă doar absența toxicității acute. Ea semnifică capacitatea materialului de a provoca o reacție adecvată a gazdei într-o aplicație specifică. Acest „răspuns adecvat” poate însemna un lucru pentru un stent, altceva pentru un implant ortopedic și încă altceva pentru un cateter. În fiecare dintre aceste cazuri, suprafața controlează evenimentele biologice inițiale: ce proteine se vor adsorbi, în ce configurație, ce receptori celulari vor fi stimulați și dacă semnalul va duce la integrarea țesutului, activarea trombocitelor, formarea biofilmului sau o reacție la corp străin.
Un bun exemplu este comparația dintre proteinele de adeziune și proteinele de pasivare. Cartea descrie modul în care preacoperirea unei suprafețe cu fibronectină crește adeziunea multor celule, în timp ce albumina o poate limita. Aceasta nu este doar o curiozitate din cultura celulară, ci un model al ceea ce se întâmplă pe implanturi. Suprafața nu este un fundal neutru. Aceasta stabilește condițiile inițiale pentru răspunsul celular ulterior. În practică, aceasta înseamnă că două suprafețe cu rezistență mecanică similară pot duce la traiectorii de vindecare complet diferite, pur și simplu deoarece ele formează primul strat de proteine adsorbite în mod diferit.
La fel de importante sunt interacțiunile dintre suprafață și microorganisme. În capitolul dedicat biofilmelor, autorii menționează că umectabilitatea, sarcina electrică, rugozitatea și topografia influențează aderența bacteriană. Tendința generală este că o rugozitate mai mare favorizează adesea aderența bacteriană, iar suprafețele hidrofobe facilitează mai frecvent atașarea bacteriană. În același timp, aceasta nu este o regulă fără excepții, deoarece sistemele extrem de superhidrofile sau superhidrofobe pot acționa ca inhibitori ai biofilmului printr-un mecanism diferit. În practică, acest lucru servește ca o notă de precauție: o soluție benefică pentru integrarea țesuturilor nu va fi întotdeauna la fel de benefică pentru controlul colonizării bacteriene.
Mai jos se află un videoclip în limba engleză intitulat BIOE 5820 Biomaterials Protein Adsorption, care este o prelegere despre adsorbția proteinelor pe suprafețele biomaterialelor.
De ce să modificăm suprafața în loc de întregul material
Acesta este principalul raționament din spatele modificării suprafeței. Dacă materialul de bază este responsabil pentru capacitatea de susținere a sarcinii, durabilitate și funcția mecanică, în timp ce suprafața este responsabilă pentru biointeracțiune, este cel mai logic să păstrăm ceea ce funcționează bine în materialul de bază și să modificăm doar ceea ce intră în contact cu țesutul. Exact așa au formulat-o autorii capitolului despre modificările fizico-chimice ale suprafeței: scopul este de a păstra proprietățile fizice cheie ale biomaterialului, modificând doar stratul exterior pentru a îmbunătăți sau modula răspunsul biologic la interfața țesut-dispozitiv.
Această abordare are câteva avantaje foarte practice. În primul rând, nu este nevoie să renunțăm la un material bine înțeles din punct de vedere mecanic și tehnologic. Titanul, oțelul, polimerii tehnici sau elastomerii își pot îndeplini în continuare rolul structural sau funcțional. În al doilea rând, răspunsul biologic poate fi adaptat mai precis la o anumită aplicație. Ne dorim o suprafață diferită pentru un implant osos, una diferită pentru o componentă care intră în contact cu sângele și încă una pentru un cateter, unde prioritatea poate fi limitarea adsorbției proteinelor și a aderenței celulelor sau bacteriilor. În al treilea rând, modificarea suprafeței permite îmbunătățirea unui dispozitiv fără a fi necesară reproiectarea completă a întregii structuri. Cartea subliniază chiar că, pentru dispozitivele deja bine stabilite în practica clinică, aceasta este o modalitate de a modifica biointeracțiunile fără a reproiecta produsul, a reechipa producția sau a recalifica personalul medical pentru a utiliza noua soluție.
Există, totuși, o condiție: trebuie să se facă distincția între o modificare reală a interfeței și o schimbare cosmetică în descriere. Simpla declarație că un material este „bioactiv” sau „antifouling” nu înseamnă mare lucru dacă nu se știe cum arată suprafața reală în forma sa finală după procesare și sterilizare. Sursa menționează că proba analizată ar trebui să corespundă cât mai mult posibil materialului sau dispozitivului în forma utilizată pentru testarea biologică sau implantare. Acest lucru este important deoarece suprafața expusă la aer poate să nu fie aceeași suprafață pe care materialul o prezintă în mediul apos al corpului.
Trei metode principale de modificare a suprafeței
Prima metodă implică modificarea suprafeței existente fără a adăuga un strat nou, separat. Atomii, moleculele și legăturile deja prezente în stratul exterior al materialului pot fi transformate chimic sau fizic. Acest grup include, printre altele, gravarea, activarea chimică, asperizarea mecanică, implantarea de ioni și anumite tratamente cu laser. Ideea este că nu „atașăm” un strat nou la implant, ci mai degrabă remodelăm propria sa suprafață. Acest lucru este avantajos atunci când este importantă o integrare puternică a modificării cu substratul, precum și reducerea riscului de delaminare și modificarea proprietăților precum reactivitatea, umectabilitatea, rezistența la coroziune, duritatea sau bioactivitatea. Sursa arată, de exemplu, că implantarea ionică poate îmbunătăți rezistența la uzură sau la coroziune, iar prelucrarea cu laser poate modifica în mod controlat rugozitatea suprafeței, cristalinitatea și compoziția chimică.
A doua abordare implică aplicarea unui strat sau a unui înveliș nou. În acest caz, un material cu o compoziție sau proprietăți diferite este plasat pe suprafața existentă. Acesta poate fi un film subțire, un strat grefat, un înveliș polimeric sau un sistem conceput ca o suprafață anti-fouling. Această strategie este deosebit de valoroasă atunci când substratul are proprietăți mecanice ideale, dar este prea „brut” din punct de vedere biologic. Un bun exemplu îl constituie suprafețele rezistente la adsorbția nespecifică a proteinelor. Mecanismul lor se bazează de obicei pe un strat puternic de hidratare, care acționează ca o barieră energetică și fizică pentru proteine. În capitolul dedicat suprafețelor anti-fouling, autorii descriu două strategii principale pentru aplicarea unor astfel de sisteme: „graft-to-surface”, în care materialul se adsorbe sau se leagă din soluție, și „graft-from-surface”, în care perii polimerici cresc de pe suprafață. Prima abordare este mai simplă din punct de vedere tehnologic; a doua atinge mai ușor o densitate de împachetare ridicată, dar necesită de obicei o chimie și o pregătire a substratului mai complexe.
În practică, această diferență are o importanță inginerescă. Dacă dorim doar să limităm rapid depunerea de proteine pe un substrat relativ simplu, soluția mai simplă poate fi suficientă. Cu toate acestea, dacă avem nevoie de un strat anti-adsorbție durabil, impermeabil și dens împachetat, simpla „lipire” a moleculelor de suprafață s-ar putea să nu fie suficientă. Cartea subliniază clar că alegerea metodei determină densitatea de împachetare, numărul de defecte și durabilitatea suprafeței finale. Aceasta înseamnă că acoperirile nu sunt evaluate exclusiv pe baza compoziției chimice declarate, ci pe baza faptului dacă formează efectiv o interfață omogenă și stabilă în condiții de funcționare.
A treia abordare implică crearea de modele, texturi și topografii. Aici, accentul principal nu se pune pe schimbarea compoziției chimice, ci pe modificarea geometriei a ceea ce „vede” celula sau proteina. Sursa subliniază că topografia suprafeței influențează aderența, proliferarea, migrația, diferențierea și expresia genică a celulelor. Celulele răspund atât la caracteristicile la scară micro, cât și la cele la scară nano, nu doar la simpla prezență a materialului. În studiile citate în carte, înălțimile, dimensiunile și distanțele variabile ale structurilor topografice au modificat gradul de mineralizare, orientarea celulară, aderența celulară și diferențierea. Aceasta înseamnă că textura nu este un simplu ornament sau un efect secundar al procesării, ci un instrument activ pentru controlul răspunsurilor biologice.
Acest lucru este evident în special în cazul implanturilor osoase și dentare. Cartea descrie modul în care un strat de suprafață adecvat de rugozitate sau tridimensional poate accelera etapele incipiente ale vindecării, poate favoriza depunerea de fibrină, legarea integrinelor și interconectarea micromecanică cu osul. Ca rezultat, rezistența la forfecare la interfața implant-os crește, iar transferul de sarcină se îmbunătățește. Acesta este un bun exemplu al faptului că texturarea nu este o „îmbunătățire oarbă”, ci o încercare de a controla un mecanism interfacial specific. Cu toate acestea, este necesară prudență, deoarece aceeași rugozitate care ajută la osteointegrare poate, într-o altă aplicație, să crească riscul de colonizare bacteriană sau să împiedice controlul suprafeței.

Greșeli comune, capcane și piste false
Cea mai comună greșeală este echivalarea „materialului mai bun” cu „răspunsul biologic mai bun”. Este prea simplist. Rezistența, rezistența la oboseală și stabilitatea chimică nu explică încă ce se va întâmpla la interfața țesutului. În cazul biomaterialelor, se poate avea un material structural excelent și o interfață biologică slabă. Se poate confrunta, de asemenea, cu problema opusă: o suprafață foarte activă din punct de vedere biologic montată pe un substrat care nu îndeplinește cerințele mecanice. Tocmai de aceea, premisa conform căreia materialul conferă rezistență implantului, în timp ce suprafața determină răspunsul organismului, este utilă în proiectare. Aceasta ne obligă să separăm două aspecte care sunt adesea combinate în ingineria clasică.
A doua capcană este convingerea că o singură proprietate a suprafeței va rezolva întreaga problemă. În practică, nu există o „setare universală de biocompatibilitate”. Creșterea hidrofilicității poate limita adsorbția anumitor proteine, dar nu îmbunătățește neapărat integrarea țesutului. Creșterea rugozității poate favoriza răspunsul osteoblastelor, dar s-ar putea să nu fie benefică pentru un mediu expus riscului de infecție. Cartea însăși menționează că nu se știe încă care parametru este cel mai important pentru fiecare răspuns biologic specific, așa că variabilele trebuie măsurate și corelate independent. Aceasta este o orientare metodologică foarte importantă: în loc să căutăm un singur număr magic, trebuie să construim o hartă a relațiilor dintre mai multe proprietăți ale interfeței și un obiectiv clinic specific.
A treia capcană se referă la grosimea modificării. Autorii capitolului privind modificările fizico-chimice subliniază că modificările ar trebui să fie cât mai subțiri posibil. În mod ideal, ar fi suficientă modificarea doar a celor câteva straturi moleculare exterioare – de ordinul câtorva nanometri –, deși, în practică, straturile trebuie uneori să fie mai groase pentru a asigura uniformitatea și durabilitatea. Un strat de acoperire prea gros poate altera proprietățile mecanice și funcționale ale dispozitivului, precum și crește riscul de fisurare și delaminare. Acest lucru este deosebit de important în cazul în care implantul este supus la oboseală sau frecare. Un strat care pare promițător din punct de vedere biologic, dar care se desprinde mecanic după o anumită perioadă de timp, nu rezolvă problema; ci doar creează una nouă.
A patra concepție greșită este tratarea suprafeței ca pe o stare statică. Sursa demonstrează că unele materiale își pot inversa organizarea suprafeței la trecerea de la aer la un mediu apos. O suprafață măsurată „în condiții uscate” poate să nu fie aceeași suprafață cu care proteinele și celulele intră în contact în organism. Acest lucru are implicații directe pentru cercetare. Dacă analiza suprafeței nu ține cont de mediul de funcționare, s-ar putea optimiza un parametru care încetează să mai aibă aceeași valoare sau semnificație după implantare.
Când este necesară o teorie mai avansată
O abordare avansată devine necesară atunci când termeni intuitivi precum „mai neted”, „mai hidrofil” sau „mai aspru” nu mai sunt suficienți. Suprafețele anti-fouling sunt un exemplu. Funcția lor nu rezultă pur și simplu din faptul că sunt alunecoase, ci din faptul că formează un strat de hidratare stabil, a cărui îndepărtare este nefavorabilă din punct de vedere energetic pentru proteinele adsorbante. Cartea demonstrează că materialele hidrofile pe bază de PEG leagă apa prin legături de hidrogen, în timp ce materialele zwitterionice pot face acest lucru și mai puternic prin hidratare indusă electrostatic. La acest nivel, trebuie să se ia în considerare nu numai chimia funcțională, ci și densitatea de împachetare a lanțului, libertatea conformațională și stabilitatea ancorării stratului.
Este necesară o teorie avansată și atunci când suprafața nu este menită doar să nu interfereze, ci să ghideze activ comportamentul celular. În astfel de cazuri, ceea ce contează este geometria la scară micro și nano, mecanica locală, dimensiunea, înălțimea și spațierea caracteristicilor topografice și, uneori, chiar ordinea sau dezordinea modelului. Tocmai de aceea cercetarea de astăzi utilizează matrice topografice și screeninguri de suprafață mai sistematice. Nu este vorba despre complexitatea academică a subiectului, ci despre faptul că celulele disting cu adevărat între scări și modele de caracteristici, iar răspunsul biologic încetează să mai fie o funcție liniară a unui singur parametru.
De ce este atât de importantă suprafața unui implant? – rezumat
În cazul biomaterialelor, succesul unui implant este adesea determinat nu de materialul în sine, ci de suprafața pe care o prezintă organismului. Suprafața este primul punct de contact cu proteinele, celulele și fluidele corporale și, prin urmare, controlează în mare măsură biocompatibilitatea. Din acest motiv, proiectarea rațională a implantului implică separarea funcțiilor: volumul are rolul de a asigura proprietățile mecanice și durabilitatea, în timp ce suprafața are rolul de a provoca răspunsul biologic adecvat. Aceasta este baza întregii logici de modificare a suprafeței fără a schimba întregul material. Se poate remodela stratul exterior existent, se poate aplica un nou strat de acoperire sau se poate proiecta un model și o topografie care vor influența adsorbția proteinelor, comportamentul celular, integrarea țesuturilor sau rezistența la depuneri. Există o singură condiție: modificarea trebuie să fie cu adevărat interfacială, subțire, durabilă și adaptată unui obiectiv clinic specific. Tocmai de aceea, în cazul biomaterialelor, suprafața nu este un detaliu de finisare, ci unul dintre principalele instrumente în proiectarea implanturilor.