Systèmes d’équilibre de phase des alliages
Table des matières
Dans les métaux purs, le déroulement des transformations est généralement facile à comprendre : la fusion et la solidification se produisent à une température unique et précisément définie, tout comme certaines transformations structurelles à l’état solide. Les courbes de refroidissement présentent alors des pauses caractéristiques, car l’énergie est absorbée ou libérée pour la transformation elle-même, plutôt que pour le changement de température. Dans le cas des alliages, la situation n’est plus aussi « ponctuelle ». Il arrive souvent qu’un alliage commence à se solidifier à une certaine température mais finisse à une autre, et pendant le processus, des phases de compositions variables coexistent.
C’est pourquoi les diagrammes d’équilibre de phase, également appelés diagrammes de phase, sont utilisés en science des matériaux. Un tel diagramme peut être considéré comme une carte : il indique quelles phases sont stables en fonction de la température et de la composition, et dans quel ordre les transformations se produisent pendant le chauffage et le refroidissement. Cela permet de prédire à la fois le déroulement de la cristallisation et les transformations ultérieures à l’état solide, et, par conséquent, la structure et les propriétés de l’ alliage fini.
Concepts clés : système, phase et composants
Pour lire correctement les diagrammes d’équilibre, vous devez comprendre le langage qu’ils « parlent ». En termes thermodynamiques, un système est un fragment distinct de la réalité analysé dans des conditions données, par exemple un échantillon d’alliage que nous refroidissons. Une phase désigne une partie homogène d’un système présentant des propriétés identiques et une composition chimique constante, séparée des autres phases par une limite de phase. Une phase peut être un liquide, une solution solide ou une phase intermétallique spécifique, si elle est formée.
Les constituants, c’est-à-dire les substances (généralement des éléments) qui composent l’alliage et à partir desquelles des phases peuvent se former, sont également importants. Dans le contexte des diagrammes binaires, nous faisons généralement référence à un système composé de deux constituants dont les proportions varient dans l’alliage. En pratique, cela signifie que le diagramme ne décrit pas un seul « matériau », mais plutôt toute une famille d’alliages de compositions différentes, et chaque changement de composition nous amène à un endroit différent sur la carte des phases.
Règle de Gibbs
L’une des raisons pour lesquelles le comportement des alliages diffère de celui des métaux purs est le nombre de variables qui « contrôlent » le système. La règle des phases de Gibbs organise la relation entre le nombre de composants, le nombre de phases et le nombre de degrés de liberté. Dans la pratique métallurgique, on suppose souvent une pression constante, car son effet sur les transitions de phase métalliques est généralement faible par rapport à l’effet de la température et de la composition.
En pratique, cela signifie que si le système dispose d’une faible « marge de manœuvre », la transition doit se produire à une seule température (d’où les arrêts caractéristiques). Cependant, lorsqu’il existe une variabilité dans la composition et la possibilité de coexistence de plusieurs phases, le système peut passer par des zones où deux phases coexistent simultanément et où leurs compositions changent avec la température. La solidification ou les transformations à l’état solide s’étendent alors sur une certaine plage de températures et la structure se forme par étapes.
Comment crée-t-on un diagramme d’équilibre binaire ?
Un diagramme binaire typique montre la relation entre la température et la composition chimique. L’axe horizontal représente la composition de l’alliage (par exemple, le pourcentage d’un composant), et l’axe vertical représente la température. Pour construire un tel diagramme, une série d’expériences est réalisée sur de nombreux alliages avec différentes proportions de composants, et les températures auxquelles les transformations se produisent sont enregistrées, le plus souvent par des méthodes d’analyse thermique, basées sur des courbes de refroidissement et de chauffage.
Les limites des zones de phase sont particulièrement importantes dans le graphique. Une ligne appelée « liquidus » sépare la zone complètement liquide de la zone où le liquide coexiste avec la phase solide. La ligne « solidus » marque la limite en dessous de laquelle l’alliage est complètement solide. Entre le liquidus et le solidus, il existe généralement une zone de mélange (par exemple, phase liquide + phase solide), ce qui signifie en pratique que pendant le refroidissement, l’alliage passe par une étape où une partie du matériau est déjà solide et une autre partie reste liquide.
La manière dont la composition des phases à une température donnée est lue est également importante. Pour ce faire, on trace une ligne horizontale (isotherme) à travers le graphique : l’intersection avec le liquidus indique la composition du liquide, et l’intersection avec le solidus indique la composition de la phase solide en équilibre à cette température. C’est sur cette base que l’on peut déduire ce qui se passe réellement dans l’alliage pendant le refroidissement.
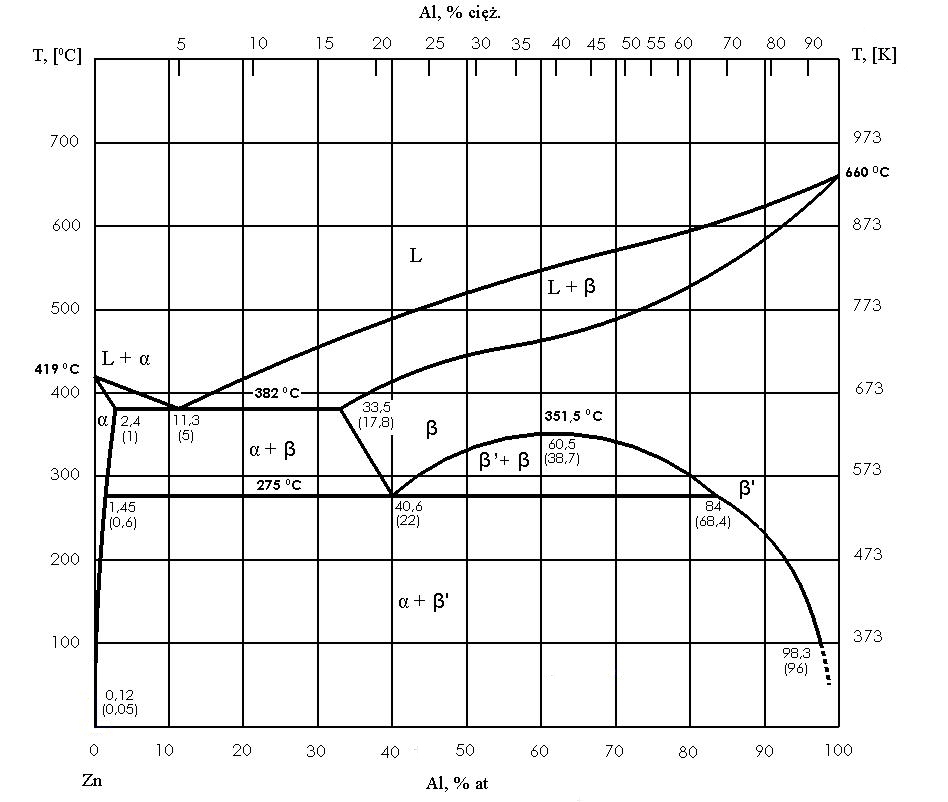
Les types les plus importants de systèmes d’équilibre
Solution solide continue
Dans certains systèmes, les composants se mélangent librement entre eux à l’état liquide et à l’état solide. Dans ce cas, en dessous du solidus, il existe une seule phase, une solution solide dont la composition dépend de la position sur l’axe de composition. Pendant le refroidissement, l’alliage commence à se solidifier au liquidus lorsque les premiers cristaux de la solution solide apparaissent, et se termine au solidus lorsque la dernière partie du liquide disparaît. Il s’agit d’un exemple classique de solidification dans une plage de températures, sans arrêt unique.
Il convient de noter que dans la zone « solution liquide + solide », les compositions des deux phases sont différentes et varient en fonction de la température. La lecture de l’isotherme nous permet de déterminer quelle partie de l’alliage est déjà à l’état solide à un moment donné et quelle partie est encore liquide.
Eutectique
Un système eutectique est très caractéristique lorsque les composants se mélangent dans un liquide mais se dissolvent mal ou pas du tout à l’état solide. Dans ce cas, il existe une composition et une température eutectiques auxquelles un liquide homogène se transforme en deux phases solides à la fois. Une telle transformation est isotherme, il y a donc une pause nette sur la courbe de refroidissement, comme dans le cas d’un métal pur, mais le mécanisme est différent : au lieu d’une seule phase solide, un fin mélange de deux phases se forme, généralement avec une morphologie spécifique et régulière.
Les alliages dont la composition est différente de celle de l’eutectique forment une structure mixte. Si l’alliage est hypereutectique, les cristaux primaires d’une phase se séparent d’abord, puis le reste du liquide se solidifie sous forme d’eutectique. Si l’alliage est hypereutectique, les cristaux primaires de la deuxième phase apparaissent d’abord, suivis de l’eutectique. En conséquence, la microstructure dépend de la composition : l’eutectique peut dominer, les cristaux primaires peuvent dominer, ou les deux composants peuvent avoir des proportions similaires.
Eutectique à solubilité limitée à l’état solide
Dans la pratique, on rencontre souvent une situation intermédiaire : les composants se mélangent bien à l’état liquide, mais à l’état solide, ils ne forment des solutions solides que dans une mesure limitée. Alors, au lieu de phases « pures », des solutions solides limites se forment, communément désignées par α et β, et l’eutectique devient un mélange de ces deux solutions avec des compositions saturées à la température eutectique.
Ceci est très important car, avec un refroidissement supplémentaire, la solubilité à l’état solide diminue souvent, de sorte que les solutions α et β peuvent devenir sursaturées. En conséquence, des séparations secondaires et une « maturation » supplémentaire de la structure peuvent se produire après la solidification complète. Le diagramme n’est donc pas seulement une description de la cristallisation, mais aussi un guide des changements à l’état solide qui affectent les propriétés du matériau.
Peritectique
Dans les systèmes péritectiques, une transformation se produit dans laquelle le liquide réagit avec la phase solide existante pour former une nouvelle phase solide. Cela se produit à une température spécifique, car trois phases coexistent au moment de la réaction. Le mécanisme péritectique revêt une importance pratique, car la nouvelle phase se développe souvent sur les cristaux de la phase d’origine, formant une couche qui empêche la diffusion des composants. Cela peut entraîner un écart entre le déroulement réel de la transformation et l’équilibre idéal, en particulier en cas de refroidissement plus rapide.
D’un point de vue technologique, la péritectie peut être une source d’hétérogénéité et de structures qui dépendent non seulement du diagramme d’équilibre lui-même, mais aussi de la cinétique, c’est-à-dire de la vitesse des processus de diffusion. Par conséquent, lors de l’interprétation des diagrammes, il est important de garder à l’esprit que le diagramme décrit l’équilibre et pas toujours l’état réel « à la volée », sans laisser le temps à la composition de s’équilibrer.
Solubilité limitée dans les liquides
Parfois, même à l’état liquide, le système n’est pas complètement homogène. Il peut arriver que, dans une certaine plage de températures, le liquide se sépare en deux liquides de compositions différentes, ce qui favorise la ségrégation et la formation de zones aux propriétés différentes. Dans un tel système, une transformation monotectique est possible, dans laquelle un liquide se transforme en un autre liquide et en une phase solide.
Du point de vue de la technologie de moulage, cela est important car la séparation des liquides peut entraîner une hétérogénéité indésirable de l’alliage. Dans la pratique, ce phénomène est souvent contré par un contrôle approprié du processus, notamment par le choix de la vitesse de refroidissement ou de la méthode de mélange du métal liquide, afin de limiter le temps nécessaire au développement de la ségrégation.
Composés chimiques et phases intermétalliques
Dans de nombreux systèmes, des composés chimiques et des phases intermétalliques se forment. Si un composé a une composition stœchiométrique constante, il apparaît sur le diagramme comme une position caractéristique correspondant à cette proportion de composants. Un tel composé peut fondre de manière « purement métallique » lorsqu’il se transforme en un liquide de même composition, ou il peut se former et disparaître dans des transformations péritectiques lorsque le processus se poursuit par réaction avec le liquide.
Les phases intermétalliques sont souvent dures et cassantes, et leur présence peut modifier considérablement les propriétés de l’alliage. C’est pourquoi les diagrammes de phases sont particulièrement importants dans la conception des alliages, car ils permettent de prédire si, dans une plage donnée de composition et de température, une phase apparaîtra qui altérera la plasticité ou, au contraire, renforcera l’alliage grâce à de fins précipités.
Transformations à l’état solide : eutectoïde et péritectoïde
Les diagrammes d’équilibre ne s’arrêtent pas à la solidification. Dans de nombreux alliages, les transformations qui se produisent après le passage à l’état solide sont importantes, en particulier lorsque la solubilité dans les solutions solides varie avec la température ou lorsqu’un des composants présente un polymorphisme. La transformation eutectoïde, qui est équivalente à l’eutectique mais se produit entièrement à l’état solide, revêt une importance particulière : une solution solide se décompose en deux phases solides à température constante. Cette transformation conduit souvent à une structure fine et régulière et peut modifier considérablement les propriétés mécaniques.
Il existe également une transformation péritectique, analogue à la péritectique, mais sans intervention de liquide : deux phases solides réagissent pour former une troisième phase solide. Dans la pratique, les transformations à l’état solide peuvent être cruciales, car elles peuvent déterminer la dureté, la résistance aux chocs ou la résistance au fluage, même si le processus de solidification s’est déroulé correctement.
Importance pratique
La conclusion la plus importante tirée de l’analyse des diagrammes est que les propriétés des alliages résultent principalement de leur structure, et pas seulement des éléments qu’ils contiennent. Les alliages monophasés sont généralement plus homogènes et leurs propriétés varient souvent de manière plus progressive en fonction de leur composition. Dans les alliages multiphases, la situation est plus complexe car le comportement du matériau est déterminé par le type de phases, leur proportion, leur distribution, la taille des grains et leur morphologie (par exemple, la forme des eutectiques ou la nature des précipités).
Par conséquent, un diagramme de phases est un outil qui aide à relier les conditions du processus au résultat. Si vous connaissez les températures et les compositions auxquelles certaines phases se produisent, vous pouvez choisir consciemment la composition de l’alliage et les conditions de refroidissement et de traitement thermique. En pratique, cela signifie qu’il est possible de prédire si l’alliage aura tendance à se séparer, si des phases intermétalliques fragiles apparaîtront, si des précipités peuvent être utilisés pour le renforcement ou si la structure sera stable dans les conditions d’utilisation.
Systèmes d’équilibre de phase des alliages – résumé
Les systèmes d’équilibre de phase sont un outil qui permet d’organiser le comportement des alliages de manière systématique et prévisible. Ils peuvent être utilisés pour déterminer quelles phases seront stables, quand la solidification commencera et se terminera, si des phénomènes eutectiques ou péritectiques se produiront et quelles transformations peuvent avoir lieu à l’état solide. En pratique, cela signifie la capacité à contrôler la microstructure et donc à contrôler les propriétés mécaniques et physiques du matériau. La capacité à lire les diagrammes de phase est donc l’une des compétences les plus importantes en science des matériaux et en métallurgie, car elle permet de traduire la théorie des transformations de phase en décisions d’ingénierie concrètes.