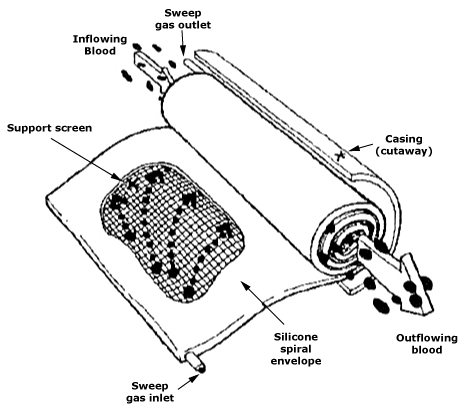
Dlaczego powierzchnia implantu jest tak ważna?
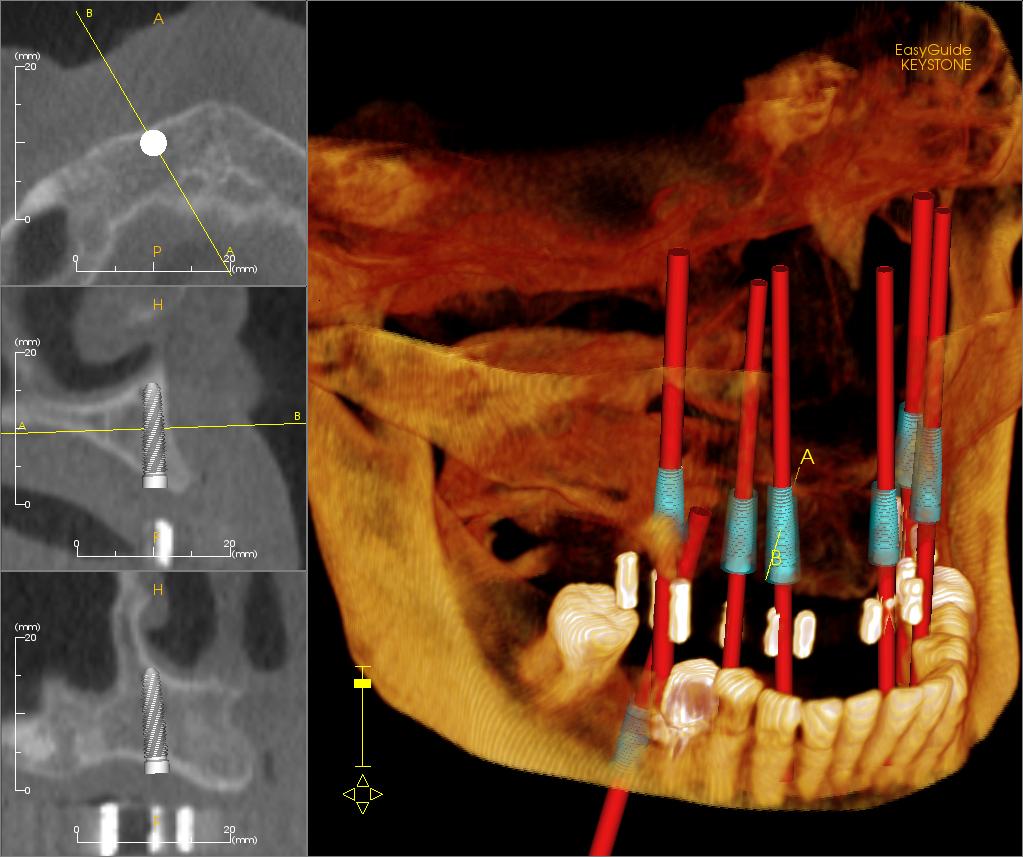
W inżynierii biomateriałów łatwo wpaść w intuicję wyniesioną z klasycznej materiałoznawczej praktyki: skoro implant ma wytrzymać obciążenia, nie korodować, nie ścierać się nadmiernie i działać przez lata, to o jego powodzeniu powinien decydować przede wszystkim materiał „w środku”. To tylko część prawdy. Materiał objętościowy rzeczywiście odpowiada za wytrzymałość, sztywność, sprężystość, trwałość czy przepuszczalność. Jednak z punktu widzenia organizmu pierwszy i najważniejszy kontakt zachodzi nie z całym blokiem materiału, lecz z jego warstwą zewnętrzną. To ona spotyka się z krwią, białkami, komórkami i płynami ustrojowymi. W praktyce oznacza to, że implant może być mechanicznie bardzo dobry, a mimo to biologicznie kłopotliwy, jeśli jego powierzchnia wysyła do tkanek „zły sygnał”.
Ta obserwacja zmienia sposób myślenia o projektowaniu implantów. Zamiast pytać wyłącznie „z czego zrobić implant?”, trzeba zastanowić się jaka ma być powierzchnia implantu. W biomateriałach odpowiedź biologiczna nie jest prostym odczytem składu chemicznego całego elementu. Jest raczej odpowiedzią na to, co dzieje się na styku materiał–tkanka: jaka jest chemia powierzchni, jej zwilżalność, ładunek, chropowatość, organizacja i reaktywność. To dlatego powodzenie implantu tak często rozstrzyga się nie w objętości materiału, lecz właśnie na granicy faz.
Artykuł został opracowany na podstawie Biomaterials Science: An Introduction to Materials in Medicine, red. William R. Wagner i in., wyd. 4, 2020. Poniższe treści są tylko ogólnym przedstawieniem poruszanego zagadnienia. Dla osób zaciekawionych tematem, polecamy zagłębienie się w literaturę.
Jak organizm reaguje na powierzchnię materiału?
Najważniejszy punkt wyjścia jest prosty: organizm nie „widzi” całego implantu naraz. W pierwszej kolejności „czyta” jego powierzchnię. Autorzy Biomaterials Science piszą wprost, że dla materiałów, które nie uwalniają niepożądanych substancji, przekaz informacji z materiału do białek, komórek i całego organizmu odbywa się przez strukturę powierzchni. Ciało odpowiada więc na konkretną chemię i organizację warstwy zewnętrznej, a nie na uśrednione właściwości całego materiału. To pozornie drobne przesunięcie akcentu ma ogromne znaczenie praktyczne, bo przenosi problem biozgodności z poziomu „jaki mamy stop lub polimer” na poziom „jak wygląda i zachowuje się jego interfejs”.
Trzeba przy tym pamiętać, że powierzchnia nie jest po prostu cienkim końcem materiału, który zachowuje się tak samo jak jego wnętrze. W książce podkreślono, że powierzchnia jest strefą o szczególnej reaktywności i niemal nieuchronnie różni się od objętości. Dla rzeczywistego materiału metalicznego warstwa zewnętrzna może obejmować nie tylko tlenek metalu, ale także zaadsorbowaną wodę, polarne związki organiczne i węglowodorowe zanieczyszczenia. Dla polimerów unikatowa strefa powierzchniowa może sięgać od około 10 do 100 nm. To ważne, bo oznacza, że nawet jeśli materiał w objętości jest jednorodny, jego aktywna biologicznie część bywa chemicznie i strukturalnie złożona.
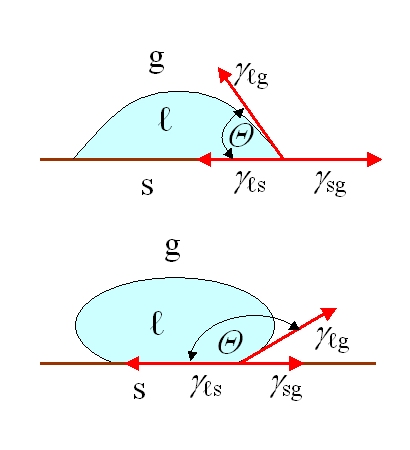
Z punktu widzenia biologii powierzchnia nie sprowadza się tylko do składu chemicznego. Autorzy wyliczają wiele cech, które mogą wpływać na reakcję biologiczną: chropowatość, wzory i topografię, zwilżalność, ruchliwość powierzchni, skład chemiczny, ładunek elektryczny, krystaliczność, moduł sprężystości i heterogeniczność. Jednocześnie uczciwie zaznaczają, że nie da się jeszcze wskazać jednej uniwersalnej cechy najważniejszej dla każdej odpowiedzi biologicznej. W praktyce to bardzo inżynierska lekcja; nie wolno opierać projektu na jednym parametrycznym haśle w rodzaju „zwiększmy chropowatość” albo „zróbmy powierzchnię bardziej hydrofilową”, bo odpowiedź organizmu jest wynikiem współdziałania kilku cech naraz.
To podejście dobrze tłumaczy, dlaczego dwa implanty wykonane z tego samego materiału objętościowego mogą zachowywać się biologicznie inaczej. Wystarczy zmiana sposobu obróbki, sterylizacji, przechowywania czy pakowania, aby zmienić stan powierzchni. Książka zwraca uwagę nawet na tak przyziemne sprawy jak odciski palców, dodatki migrujące z opakowań albo zanieczyszczenia z papieru czy folii. W laboratorium to detal, ale w rzeczywistości właśnie takie detale mogą sprawić, że zbadamy nie tę powierzchnię, którą faktycznie ma implant używany klinicznie.

Jak powierzchnia przekłada się na biozgodność
Jeżeli powierzchnia jest pierwszym językiem komunikacji między implantem a organizmem, to trzeba zapytać, jak wygląda ten dialog. Jednym z kluczowych mechanizmów jest adsorpcja białek. W źródle podkreślono, że po implantacji syntetycznego biomateriału białka adhezyjne bardzo szybko, w skali sekund, adsorbują się na jego powierzchni. W ten sposób materiał, który sam w sobie nie ma biologicznych motywów rozpoznawczych, staje się dla organizmu „czytelny”. Innymi słowy, komórki często nie reagują bezpośrednio na czysty materiał, lecz na warstwę białek, która utworzyła się na jego powierzchni chwilę po kontakcie z ustrojem.
To ma zasadniczą konsekwencję dla rozumienia biozgodności. Biozgodność nie oznacza tylko braku ostrej toksyczności. Oznacza zdolność materiału do działania z odpowiednią odpowiedzią gospodarza w konkretnej aplikacji. Owa „odpowiednia odpowiedź” może oznaczać coś innego dla stentu, coś innego dla implantu ortopedycznego, a jeszcze coś innego dla cewnika. W każdym z tych przypadków powierzchnia steruje pierwszymi zdarzeniami biologicznymi: jakie białka się zaadsorbują, w jakiej konfiguracji, które receptory komórkowe zostaną pobudzone i czy dalej pójdzie sygnał w stronę integracji z tkanką, aktywacji płytek, tworzenia biofilmu albo reakcji na ciało obce.
Dobry przykład daje porównanie białek adhezyjnych i białek pasywujących. W książce opisano, że uprzednie pokrycie powierzchni fibryonektyną zwiększa adhezję wielu komórek, podczas gdy albumina może ją ograniczać. To nie jest ciekawostka z hodowli komórkowej, tylko model tego, co dzieje się na implantach. Powierzchnia nie jest neutralnym tłem. Ona selekcjonuje warunki startowe dla dalszej odpowiedzi komórkowej. W praktyce oznacza to, że dwie powierzchnie o zbliżonej wytrzymałości mechanicznej mogą prowadzić do zupełnie innej trajektorii gojenia tylko dlatego, że inaczej ustawiają pierwszą warstwę adsorbowanych białek.
Równie ważne są relacje między powierzchnią a drobnoustrojami. W rozdziale o biofilmach autorzy przypominają, że zwilżalność, ładunek, chropowatość i topografia wpływają na adhezję bakterii. Ogólna tendencja jest taka, że większa chropowatość często sprzyja adhezji bakteryjnej, a powierzchnie hydrofobowe częściej ułatwiają przyleganie bakterii. Jednocześnie nie jest to reguła bezwyjątkowa, bo ekstremalnie superhydrofilowe lub superhydrofobowe układy mogą działać przeciwbiofilmowo innym mechanizmem. W praktyce to przestroga: rozwiązanie korzystne dla integracji tkankowej nie zawsze będzie równie korzystne dla kontroli kolonizacji bakteryjnej.
Poniżej znajduje się anglojęzyczny filmik BIOE 5820 Biomaterials Protein Adsorption, który jest wykładem o adsorpcji białek na powierzchniach biomateriałów.
Dlaczego modyfikuje się powierzchnię, a nie cały materiał
Stąd wynika główna logika modyfikacji powierzchni. Jeżeli materiał objętościowy odpowiada za nośność, trwałość i funkcję mechaniczną, a powierzchnia za biointerakcję, to najrozsądniej jest zachować to, co działa dobrze w objętości, i zmienić tylko to, co styka się z tkanką. Właśnie tak formułują to autorzy rozdziału o fizykochemicznych modyfikacjach powierzchni: celem jest zachowanie kluczowych właściwości fizycznych biomateriału przy jednoczesnej zmianie jedynie zewnętrznej warstwy tak, aby poprawić lub modulować odpowiedź biologiczną na granicy tkanka–urządzenie.
To podejście ma kilka bardzo praktycznych zalet. Po pierwsze, nie trzeba rezygnować z materiału, który jest dobrze poznany mechanicznie i technologicznie. Tytan, stal, polimery konstrukcyjne czy elastomery mogą dalej pełnić swoją funkcję nośną albo funkcjonalną. Po drugie, można precyzyjniej stroić odpowiedź biologiczną pod dane zastosowanie. Innej powierzchni chcemy dla implantu kostnego, innej dla elementu kontaktującego się z krwią, a jeszcze innej dla cewnika, gdzie priorytetem może być ograniczenie adsorpcji białek i adhezji komórek lub bakterii. Po trzecie, modyfikacja powierzchni pozwala ulepszać urządzenie bez konieczności pełnego przeprojektowania całej konstrukcji. W książce podkreślono nawet, że przy już dobrze znanych klinicznie urządzeniach jest to sposób na zmianę biointerakcji bez przebudowy wyrobu, przestawiania produkcji i ponownego uczenia personelu medycznego obsługi nowego rozwiązania.
Jest jednak warunek: trzeba odróżnić realną modyfikację interfejsu od kosmetycznej zmiany opisu. Sama deklaracja, że materiał jest „bioaktywny” albo „antyfoulingowy”, niewiele znaczy, jeśli nie wiadomo, jak wygląda rzeczywista powierzchnia w finalnej postaci po obróbce i sterylizacji. W źródle zaznaczono, że analizowana próbka powinna jak najwierniej odpowiadać materiałowi lub urządzeniu w formie używanej do testów biologicznych albo implantacji. To ważne, bo powierzchnia w powietrzu może nie być tą samą powierzchnią, którą materiał pokaże w środowisku wodnym organizmu.
Trzy główne drogi modyfikacji powierzchni
Pierwsza droga polega na zmianie istniejącej powierzchni bez dokładania odrębnej, nowej warstwy. Można chemicznie albo fizycznie przekształcać atomy, cząsteczki i wiązania obecne już w zewnętrznej strefie materiału. Do tej grupy należą między innymi trawienie, aktywacja chemiczna, chropowacenie mechaniczne, implantacja jonów czy niektóre zabiegi laserowe. Ich sens polega na tym, że nie „doklejamy” nowej skóry do implantu, tylko przebudowujemy jego własne oblicze. To bywa korzystne tam, gdzie ważna jest silna integracja modyfikacji z podłożem, ograniczenie ryzyka odspajania oraz zmiana takich cech jak reaktywność, zwilżalność, odporność korozyjna, twardość czy bioaktywność. W źródle pokazano na przykład, że implantacja jonów może poprawiać zużycie lub odporność korozyjną, a obróbka laserowa może w kontrolowany sposób zmieniać chropowatość, krystaliczność i chemię powierzchni.
Druga droga to nałożenie nowej warstwy albo powłoki. Wtedy na istniejącej powierzchni umieszcza się materiał o innym składzie lub innych właściwościach. To może być cienki film, warstwa graftowana, powłoka polimerowa albo układ zaprojektowany jako powierzchnia niefoulingowa. Taka strategia jest szczególnie cenna wtedy, gdy podłoże ma idealne własności mechaniczne, ale z biologicznego punktu widzenia jest zbyt „surowe”. Dobrym przykładem są powierzchnie odporne na nieswoistą adsorpcję białek. Ich działanie opiera się zwykle na silnej warstwie hydratacyjnej, która stanowi energetyczną i fizyczną barierę dla białek. W rozdziale o nonfouling surfaces autorzy opisują dwie główne strategie nanoszenia takich układów: „graft-to-surface”, gdzie materiał adsorbuje się lub wiąże z roztworu, oraz „graft-from-surface”, gdzie szczotki polimerowe rosną z powierzchni. Pierwsze podejście jest prostsze technologicznie, drugie łatwiej daje wysoką gęstość upakowania, ale zwykle wymaga bardziej wymagającej chemii i przygotowania podłoża.
W praktyce ta różnica ma znaczenie inżynierskie. Jeżeli chcemy jedynie szybko ograniczyć osadzanie się białek na stosunkowo prostym podłożu, prostsze rozwiązanie może być wystarczające. Jeżeli jednak zależy nam na trwałej, szczelnej i gęsto upakowanej warstwie przeciwadsorpcyjnej, samo „przyklejenie” cząsteczek do powierzchni może nie wystarczyć. Książka wyraźnie podkreśla, że wybór metody decyduje o gęstości upakowania, liczbie defektów i trwałości końcowej powierzchni. To oznacza, że powłoki nie ocenia się tylko po deklarowanej chemii, ale po tym, czy rzeczywiście tworzy jednorodny, stabilny interfejs w warunkach pracy.
Trzecia droga to tworzenie wzorów, tekstur i topografii. Tutaj nie chodzi przede wszystkim o zmianę składu chemicznego, ale o zmianę geometrii tego, co „widzi” komórka albo białko. Źródło podkreśla, że topografia powierzchni wpływa na adhezję, proliferację, migrację, różnicowanie i ekspresję genów komórek. Komórki reagują zarówno na cechy mikro-, jak i nanoskali, a nie tylko na samą obecność materiału. W badaniach przywołanych w książce różne wysokości, rozmiary i odstępy struktur topograficznych zmieniały stopień mineralizacji, ukierunkowanie komórek, ich przyczepność i różnicowanie. To oznacza, że tekstura nie jest ozdobą ani ubocznym skutkiem obróbki, ale aktywnym narzędziem sterowania odpowiedzią biologiczną.
Szczególnie wyraźnie widać to w implantach kostnych i stomatologicznych. W książce opisano, że odpowiednio chropowata lub trójwymiarowa warstwa powierzchniowa może przyspieszać wczesne etapy gojenia, sprzyjać odkładaniu fibryny, wiązaniu integryn i mikromechanicznemu zazębieniu z kością. W efekcie rośnie wytrzymałość ścinająca na granicy implant–kość i poprawia się transfer obciążeń. To dobry przykład, że teksturowanie nie jest „ulepszaniem na ślepo”, lecz próbą sterowania konkretnym mechanizmem interfejsowym. Trzeba jednak uważać, bo ta sama chropowatość, która pomaga osteointegracji, w innym zastosowaniu może zwiększyć ryzyko kolonizacji bakteryjnej albo utrudnić kontrolę powierzchni.

Typowe błędy, pułapki i fałszywe tropy
Najczęstszy błąd polega na utożsamieniu „lepszego materiału” z „lepszą odpowiedzią biologiczną”. To zbyt proste. Wytrzymałość, odporność zmęczeniowa i stabilność chemiczna nie tłumaczą jeszcze, co wydarzy się na styku z tkanką. W biomateriałach można mieć świetny materiał konstrukcyjny i słaby interfejs biologiczny. Można też mieć odwrotny problem: bardzo aktywną biologicznie powierzchnię osadzoną na podłożu, które nie spełnia wymagań mechanicznych. Właśnie dlatego teza, że materiał daje implantowi wytrzymałość, a powierzchnia decyduje o odpowiedzi organizmu, jest użyteczna projektowo. Zmusza do rozdzielenia dwóch pytań, które w klasycznej inżynierii często wrzuca się do jednego worka.
Druga pułapka to wiara, że jedna cecha powierzchni rozwiąże cały problem. W praktyce nie istnieje uniwersalne „ustawienie biozgodności”. Zwiększenie hydrofilowości może ograniczyć adsorpcję pewnych białek, ale nie musi automatycznie poprawić integracji z tkanką. Zwiększenie chropowatości może wspomóc odpowiedź osteoblastów, ale nie musi być korzystne dla środowiska zagrożonego infekcją. Sama książka zaznacza, że nie wiadomo jeszcze, który parametr jest najważniejszy dla każdej konkretnej odpowiedzi biologicznej, dlatego zmienne trzeba mierzyć i korelować niezależnie. To bardzo ważna wskazówka metodologiczna: zamiast szukać jednej magicznej liczby, trzeba budować mapę zależności między kilkoma cechami interfejsu a konkretnym celem klinicznym.
Trzecia pułapka dotyczy grubości modyfikacji. Autorzy rozdziału o modyfikacjach fizykochemicznych podkreślają, że modyfikacje powinny być możliwie cienkie. Idealnie wystarczyłaby zmiana kilku najbardziej zewnętrznych warstw molekularnych, rzędu kilku nanometrów, choć w praktyce warstwy muszą być czasem grubsze, aby zapewnić jednorodność i trwałość. Zbyt gruba powłoka może zmienić właściwości mechaniczne i funkcjonalne urządzenia, a także zwiększyć ryzyko pękania i delaminacji. To szczególnie ważne tam, gdzie implant pracuje zmęczeniowo albo doświadcza tarcia. Warstwa, która z biologicznego punktu widzenia wygląda obiecująco, ale mechanicznie odspaja się po pewnym czasie, nie rozwiązuje problemu, tylko tworzy nowy.
Czwarty fałszywy trop to traktowanie powierzchni jako stanu stałego. W źródle pokazano, że niektóre materiały mogą odwracać organizację powierzchni po przejściu z powietrza do środowiska wodnego. Powierzchnia zmierzona „na sucho” nie musi być tą samą powierzchnią, z którą spotkają się białka i komórki w organizmie. To ma bezpośrednie konsekwencje dla badań. Jeżeli analiza powierzchni nie uwzględnia środowiska pracy, można zoptymalizować parametr, który po implantacji przestaje mieć tę samą wartość albo znaczenie.
Kiedy potrzebna jest bardziej zaawansowana teoria
Zaawansowane podejście staje się potrzebne wtedy, gdy nie wystarcza już intuicyjne hasło „bardziej gładko”, „bardziej hydrofilowo” albo „bardziej chropowato”. Przykładem są powierzchnie niefoulingowe. Ich działanie nie wynika po prostu z tego, że są śliskie, ale z tego, że tworzą stabilną warstwę hydratacyjną, której usunięcie jest energetycznie niekorzystne dla adsorbujących się białek. W książce pokazano, że materiały hydrofilowe oparte na PEG wiążą wodę przez wiązania wodorowe, a materiały zwitterionowe mogą robić to jeszcze silniej przez hydratację indukowaną elektrostatycznie. Na tym poziomie trzeba już myśleć nie tylko o chemii funkcjonalnej, ale też o gęstości upakowania łańcuchów, swobodzie konformacyjnej i trwałości zakotwienia warstwy.
Zaawansowana teoria jest potrzebna także wtedy, gdy powierzchnia ma nie tylko nie przeszkadzać, ale aktywnie kierować zachowaniem komórek. Wtedy liczy się geometria mikro- i nanoskali, lokalna mechanika, rozmiar, wysokość i odstępy cech topograficznych, a czasem nawet zorganizowanie albo nieuporządkowanie wzoru. To właśnie dlatego w badaniach wykorzystuje się dziś macierze topograficzne i bardziej systematyczne przesiewy powierzchni. Nie chodzi o akademicką komplikację tematu, ale o to, że komórki naprawdę rozróżniają skale i układy cech, a odpowiedź biologiczna przestaje być liniową funkcją jednego parametru.
Dlaczego powierzchnia implantu jest tak ważna? – podsumowanie
W biomateriałach o powodzeniu implantu często nie decyduje sam materiał objętościowy, lecz to, jaką powierzchnię pokazuje on organizmowi. To powierzchnia jest pierwszym miejscem kontaktu z białkami, komórkami i płynami ustrojowymi, a więc w dużej mierze steruje biozgodnością. Z tego powodu sensowne projektowanie implantów polega na rozdzieleniu funkcji: objętość ma zapewnić mechanikę i trwałość, a powierzchnia ma ustawić właściwą odpowiedź biologiczną. Stąd bierze się cała logika modyfikacji powierzchni bez zmieniania całego materiału. Można przebudować istniejącą warstwę zewnętrzną, nałożyć nową powłokę albo zaprojektować wzór i topografię, które wpłyną na adsorpcję białek, zachowanie komórek, integrację z tkanką czy odporność na fouling. Warunek jest jeden: modyfikacja musi być naprawdę interfejsowa, cienka, trwała i dopasowana do konkretnego celu klinicznego. Właśnie dlatego w biomateriałach powierzchnia nie jest detalem wykończeniowym, lecz jednym z głównych narzędzi projektowania implantu.