Ingegneria biomedica nel contesto della scienza dei materiali
Indice
L’ingegneria biomedica è oggi un vasto ecosistema di conoscenze, in cui la scienza dei materiali, la meccanica dei fluidi e i fenomeni di trasporto, le tecniche di misurazione e l’ingegneria dei sistemi si intrecciano con la fisiologia e la pratica clinica. La seconda edizione di The Biomedical Engineering Handbook, a cura di J.D. Bronzino, sintetizza questi temi, dimostrando come la scelta del materiale e delle sue condizioni superficiali, attraverso la progettazione di sensori e le caratteristiche di flusso di massa, influenzi la progettazione di organi artificiali e la loro produzione di precisione. Questo articolo ci aiuterà a comprendere questa prospettiva utilizzando esempi tratti dai campi dei biomateriali, del rilevamento biomedico, dell’ingegneria dei tessuti e degli organi artificiali, evidenziando le implicazioni per la tecnologia di produzione e il controllo qualità.
Nell’ingegneria biomedica non esistono decisioni isolate: la scelta della classe di materiale, la topografia e la chimica della superficie, le condizioni di flusso e di trasferimento di massa, l’architettura del dispositivo e il processo di produzione formano un insieme sistemico che deve essere progettato per una specifica indicazione clinica e un regime di carico biologico.
Il ruolo della scienza dei materiali nell’ingegneria biomedica
In termini enciclopedici, un biomateriale è un materiale destinato al contatto diretto con i tessuti in un dispositivo medico, progettato per sostituire in modo sicuro ed efficace la struttura o la funzione del corpo. Una panoramica generale delle classi e delle questioni di progettazione è fornita nella sezione “Biomateriali”, che tratta metalli, ceramiche, polimeri, compositi, polimeri biodegradabili e materiali di origine biologica, nonché questioni relative alla manutenzione e al fissaggio delle endoprotesi. La struttura dei capitoli conduce dalla selezione delle classi di base dei materiali alle questioni di integrazione con i tessuti duri e molli, riflettendo bene la natura sistemica del campo.
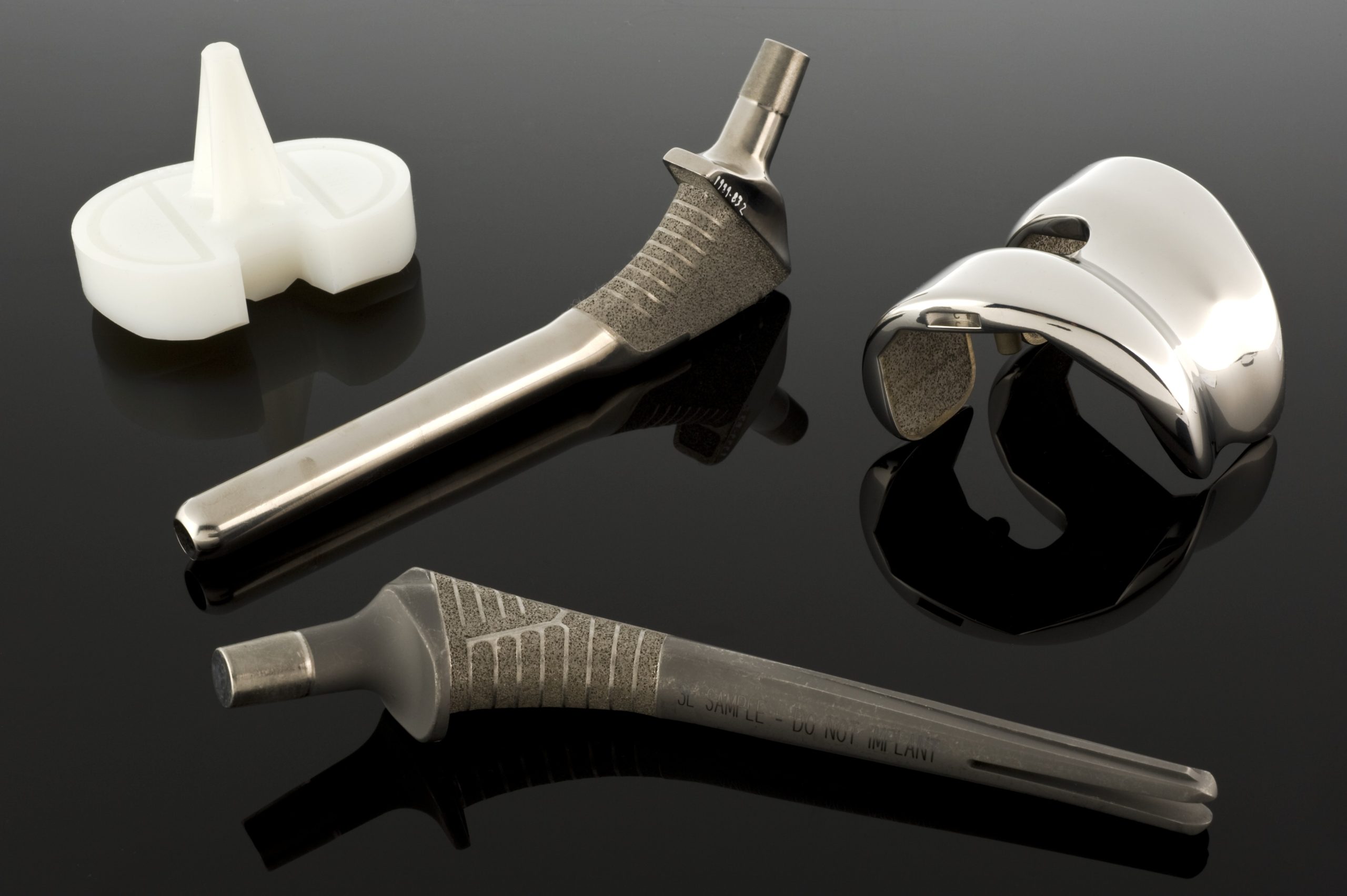
Nei metalli (acciai Cr-Ni-Mo, leghe Co-Cr, leghe di titanio), la resistenza alla corrosione e alla fatica, nonché la capacità di modellare con precisione la microstruttura, sono fondamentali. Da un punto di vista pratico, il libro sottolinea che la storia della lavorazione (fusione, deformazione plastica, trattamento termico, pulizia e persino micro-lavorazione finale) è correlata alla resistenza alla corrosione interstiziale e da tensione e alla rottura per fatica. È importante sottolineare che, per quanto riguarda la produzione di precisione, il capitolo sui metalli tratta anche la “Produzione di impianti”, confermando l’inseparabilità tra la progettazione dei materiali e la tecnologia di produzione in medicina.
Le ceramiche (allumina, zirconia, carboni, vetroceramiche, sistemi a base di fosfato di calcio) offrono durezza, resistenza chimica e, nel caso delle vetroceramiche bioattive, la capacità di formare legami chimici con i tessuti. Allo stesso tempo, la monografia ci ricorda la fragilità e i meccanismi di deterioramento della ceramica e descrive le tecniche di produzione delle bioceramiche in termini di sostituzione dei tessuti duri e integrazione dei tessuti; è qui che la progettazione della geometria, della porosità e della qualità della superficie incontra il rigoroso controllo dei difetti critici per la resistenza alla frattura.
I polimeri sono il coltellino svizzero della biomedicina, che spazia dal PVC e PE al PMMA e PU, e comprende sistemi in poliestere biodegradabile, tutti dotati di un ricco arsenale di modifiche superficiali per migliorare la biocompatibilità. Di particolare importanza è il fatto che questa classe consente il controllo delle proprietà attraverso il peso molecolare e la distribuzione, la struttura chimica e la reticolazione, nonché la combinazione della funzione di barriera meccanica con motivi chimici bioattivi. Vengono inoltre discussi la sterilizzazione e il suo impatto sulle proprietà e i metodi di modellazione del gradiente chimico dell’interfaccia proteina-superficie, che si traduce direttamente in emocompatibilità e adesione cellulare.
Nei compositi, grazie alla loro struttura (particelle, fibre, porosità), è possibile combinare requisiti contrastanti: modulare l’anisotropia, adattare il modulo all’osso, migliorare lo smorzamento delle vibrazioni e ottenere transizioni graduali nelle proprietà. La monografia organizza questi temi, discutendo i confini delle proprietà, la porosità e la biocompatibilità. Dal punto di vista della produzione, il controllo della distribuzione di fase e dei difetti all’interfaccia matrice-rinforzo diventa importante quanto il materiale stesso.
La selezione e la qualificazione di un biomateriale non possono essere separate dalla tecnologia utilizzata per lavorarlo e dal metodo di carico previsto. Lo stesso materiale con una microstruttura, una topografia e una pulizia superficiale diverse presenterà un profilo diverso di corrosione, usura, adsorbimento proteico e integrazione tissutale. Pertanto, nel processo di progettazione, è necessario controllare contemporaneamente la microstruttura volumetrica e l’interfaccia biofisico-chimica.
Sensori biomedici e interfacce materiale-biologia
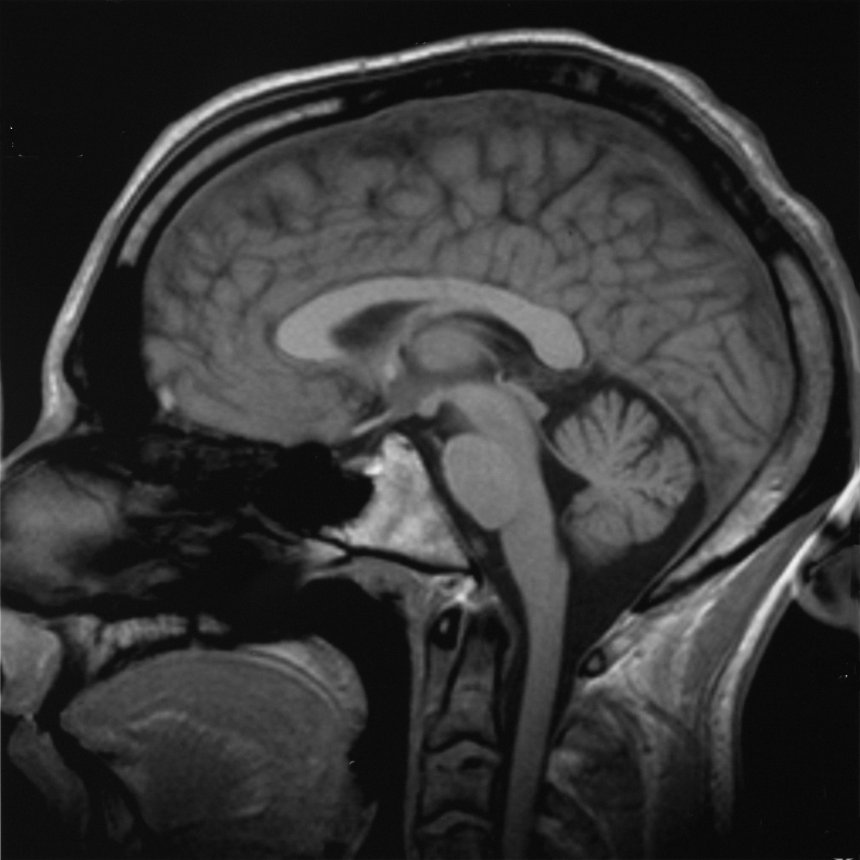
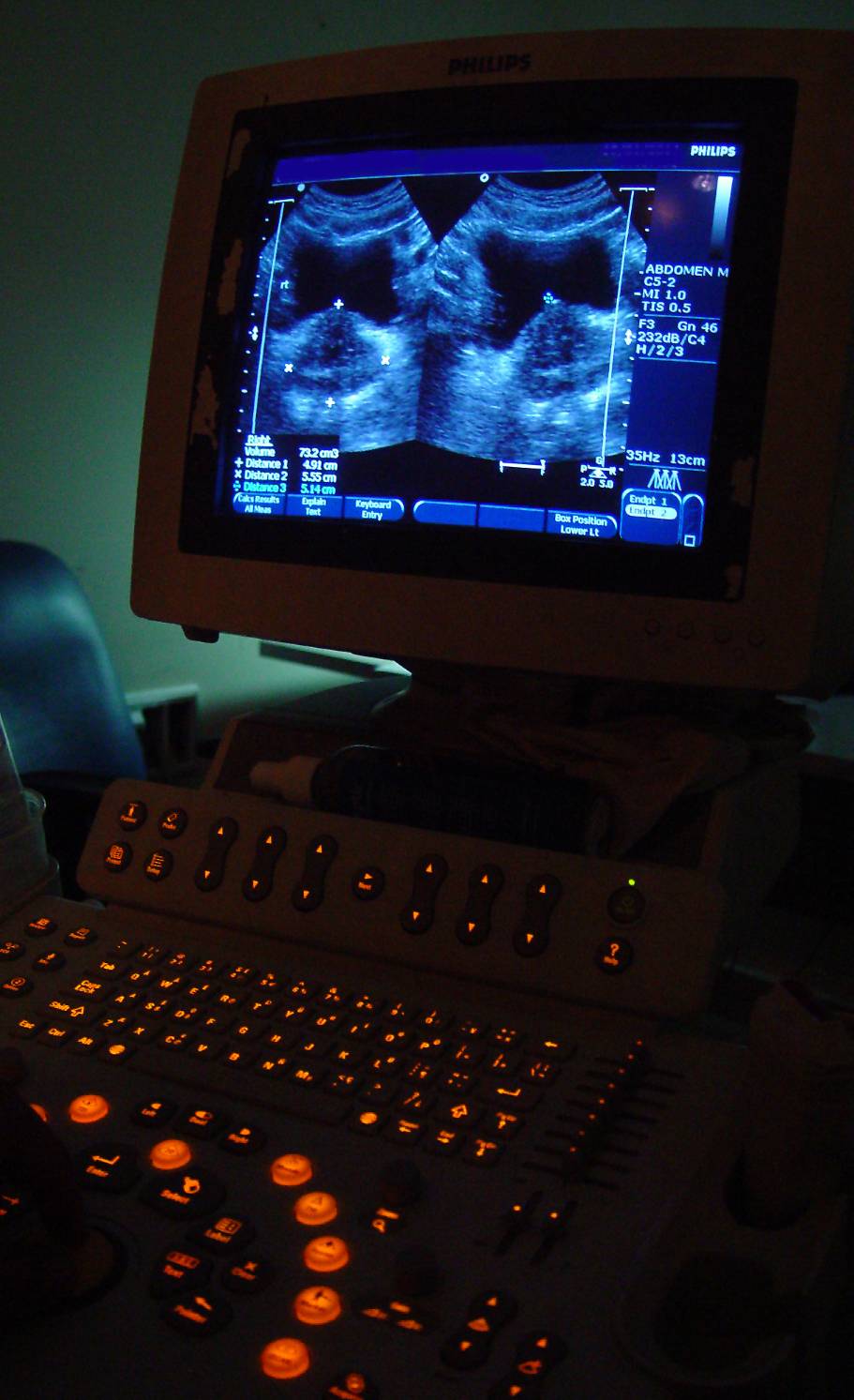
I sensori biomedici fungono da interfaccia tra il sistema biologico e il sistema elettronico, convertendo quantità geometriche, meccaniche, termiche, idrauliche o chimiche in segnali elettrici. Il compendio evidenzia una doppia classificazione: sensori fisici, che misurano, tra le altre cose, lo spostamento muscolare, la pressione sanguigna e il flusso dei fluidi, e sensori chimici, che identificano composti, concentrazioni e attività, dai sistemi elettrochimici e fotometrici ai sistemi analitici complessi. I sensori ottici sono evidenziati come uno strumento altamente versatile sia per il rilevamento che per la trasmissione grazie alla fibra ottica.
Gli elettrodi biopotenziali, essenziali nella diagnostica e nella terapia, occupano un posto speciale. Il loro funzionamento dipende non solo dal sistema elettronico e dalla geometria, ma soprattutto dal modo in cui interagiscono con l’ambiente biologico. Diverse applicazioni, dall’Ag/AgCl di superficie agli aghi EMG e ai microelettrodi a film sottile per la registrazione intracardiaca e del sistema nervoso centrale, richiedono diverse configurazioni di materiali, rivestimenti e progettazione meccanica, nonché diverse procedure di qualificazione. Il problema del rigetto e delle reazioni ai corpi estranei riduce la stabilità del segnale e la durata dell’interfaccia; quindi, non è solo una questione di elettronica, ma anche di chimica, topografia superficiale e pulizia del processo.
Il libro organizza anche i metodi di applicazione del sensore al paziente, che vanno dai metodi senza contatto al contatto con la pelle, ai sensori intra-corporei minimamente invasivi e a quelli impiantabili. Ciascuno di questi metodi ha requisiti diversi in termini di biocompatibilità, stabilità del segnale e strategie di disinfezione/sterilizzazione, che hanno conseguenze dirette sulla scelta del materiale e della tecnologia di produzione.
La progettazione di un sensore biomedico è simile alla progettazione di un’interfaccia, in cui i parametri elettrici e meccanici sono fondamentali quanto la scelta del materiale di contatto, i suoi rivestimenti, la preparazione della superficie e il metodo di montaggio, che insieme determinano la bioreazione e la deriva del segnale nel tempo.
Fenomeni di trasporto e vincoli meccanici
L’ingegneria dei tessuti e la progettazione di organi artificiali derivano dalla comprensione che il trasporto di massa, energia e quantità di moto su una scala che va dai micron ai centimetri controlla la funzione dei tessuti e dei dispositivi. I redattori della sezione “Ingegneria dei tessuti” sottolineano due temi ingegneristici: le proprietà e lo sviluppo dei materiali su due scale di lunghezza (molecolare e cellulare) e l’analisi dei processi di velocità. A livello superficiale, ciò comporta l’ingegneria biomolecolare (immobilizzazione di ligandi adesivi, controllo della densità dei motivi) e i fenomeni di adsorbimento delle proteine che modellano l’ulteriore risposta cellulare. A livello mesoscopico, sono fondamentali gli scaffold e i modelli di rigenerazione con dimensioni dei pori, permeabilità e degradazioni definite con precisione.
Inoltre, sono coinvolti anche gli stress tangenziali derivanti dal flusso, nonché le velocità di diffusione e convezione di nutrienti, ossigeno e metaboliti. I capitoli dedicati all’influenza delle sollecitazioni di taglio sulle cellule e al ruolo del trasporto di massa nella funzione dei tessuti mostrano che l’ambiente meccanico e i gradienti di concentrazione si traducono in morfologia, riorganizzazione citoscheletrica, trasduzione del segnale, secrezione di metaboliti e regolazione genica nelle cellule endoteliali, e quindi nello sviluppo, nella stabilità e nella funzione dei neotessuti. La conclusione è semplice: senza il controllo del flusso e dello scambio di massa, anche il materiale meglio scelto non funzionerà in modo prevedibile.
Nell’ingegneria dei tessuti e degli organi artificiali, i parametri di flusso e diffusione sono materiali di progettazione al pari dei polimeri o delle ceramiche. I bioreattori, la struttura dei pori e le proprietà di flusso del prodotto devono essere regolati come variabili di progettazione.
Ingegneria dei tessuti
L’ingegneria dei tessuti è definita come l’applicazione di principi scientifici alla progettazione, costruzione, modifica, crescita e manutenzione di tessuti viventi. Secondo Bronzino et al., affinché ciò sia possibile, è necessario selezionare una linea cellulare e una fonte cellulare, progettare un’interfaccia matrice-cellula e un controllo dell’organizzazione dei tessuti e garantire l’apporto metabolico. È qui che i materiali incontrano la biologia: i ligandi adesivi immobilizzati, il controllo dell’adsorbimento delle proteine e la microarchitettura dello scaffold determinano l’adesione, la proliferazione e la differenziazione.
In pratica, il nucleo è costituito da scaffold con dimensioni comprese tra 10 e 100 µm, che determinano il trasporto, la colonizzazione cellulare e la direzione di crescita dei tessuti. Da questo punto di vista, la classe dei polimeri biodegradabili è fondamentale: il capitolo sui polimeri biodegradabili descrive sia i poliesteri alifatici derivati dal glicolide e dal lattide che le famiglie alternative, nonché la modellizzazione della loro degradazione. L’autore sottolinea due vantaggi: la scomparsa della reazione cronica al corpo estraneo con il progredire del riassorbimento e la capacità di fungere da scaffold temporanei per la rigenerazione dei tessuti.
I materiali a base di collagene, in quanto sistemi di origine tissutale, offrono un’architettura della matrice extracellulare biologicamente familiare. La sezione sul collagene descrive sia la struttura chimica e le proprietà fisico-chimiche, sia le tecnologie per la produzione di membrane, schiume porose, gel e compositi. Inoltre, delinea i criteri di progettazione per gli impianti di collagene riassorbibili, tra cui porosità, densità apparente, idrofilia, permeabilità e stabilità in vivo. Questi parametri, che sono anche parametri del processo di produzione, tra cui velocità di essiccazione, condizioni di liofilizzazione, agenti reticolanti e purezza dei reagenti, si traducono direttamente in risultati biologici.
All’intersezione tra la meccanica dei materiali e quella dei fluidi, emergono dispositivi e bioreattori. I sistemi a fibre capillari e microcarrier consentono di mantenere il metabolismo alle densità cellulari necessarie per la ricostruzione dei tessuti, a condizione che siano controllati gli sforzi di taglio e i gradienti di concentrazione. La stessa logica si applica su scala clinica quando lo scaffold viene colonizzato in situ: la perfusione, la diffusione e i vincoli meccanici dell’ospite determinano il destino dell’impianto.
Organi artificiali e medicina sostitutiva
La sezione “Protesi e organi artificiali” mostra che la sostituzione della funzione organica può essere ponte (ad esempio, circolazione extracorporea), intermittente e ripetibile (emodialisi, CAPD) o a lungo termine con impianto. Allo stesso tempo, gli autori sottolineano onestamente i limiti: come qualsiasi macchina, un organo artificiale ha una durata di vita limitata a causa dell’attrito, dell’usura e dell’invecchiamento dei materiali nell’ambiente caldo, umido e corrosivo del corpo. L’equilibrio dei benefici, quindi, dipende dalla combinazione della durata di vita prevista del dispositivo, dal metodo di manutenzione/sostituzione e dalla prognosi delle condizioni del paziente. Questo realismo ingegneristico coesiste con un dato demografico: milioni di pazienti vivono grazie a pacemaker, valvole, dialisi o sistemi di drenaggio.
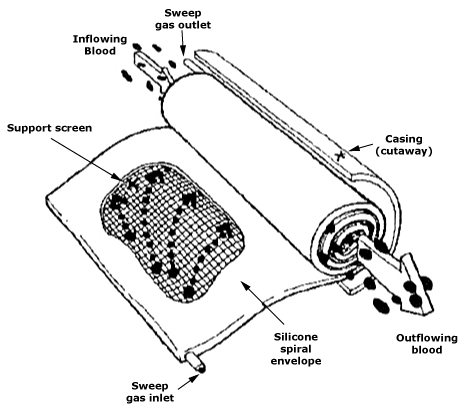
L’esempio del rene artificiale è particolarmente istruttivo: si tratta di un dispositivo che incarna il trasporto di massa. Nella dialisi, sono le membrane, i coefficienti di permeabilità, le clearance e le condizioni di flusso, nonché la farmacocinetica e l’adeguatezza della procedura, a determinare l’effetto clinico. Ciascuna di queste variabili è correlata alla scienza dei materiali (chimica e architettura delle membrane), alla meccanica dei fluidi (flusso laminare/turbolento, fenomeni di parete) e all’affidabilità operativa. Di conseguenza, c’è stato un intenso sviluppo dell’emodiafiltrazione, della modifica delle superfici e dei nuovi polimeri delle membrane.
Nel sistema cardiovascolare esiste un conflitto tra i requisiti di emocompatibilità e di durata meccanica. La progettazione delle valvole comporta sia una valutazione emodinamica (cadute di pressione, perdite di energia, riflussi e aree di ristagno) sia questioni relative alla deposizione di trombi e alla durata ciclica. Negli innesti vascolari, la trombosi e l’iperplasia neointimale vengono combattute introducendo modifiche ai materiali e alla geometria che influenzano la distribuzione dello stress da taglio e le caratteristiche del flusso. Qualsiasi cambiamento nel materiale o nella topografia della superficie non è puramente estetico, ma piuttosto un intervento nella biologia della trombogenesi e della guarigione delle ferite.
Gli organi bioibridi, d’altra parte, sono dispositivi che incorporano elementi viventi e combinano tecnologie di trapianto con strutture sintetiche, promettendo funzioni più vicine alla natura, ma imponendo requisiti in termini di materiali e processi. Si tratta di un campo in cui l’ingegneria tissutale e gli apparati di sostituzione di massa stanno spingendo nella stessa direzione: verso interfacce sempre più funzionali e resilienti.
Produzione di precisione e controllo qualità
Il modo e il materiale con cui un prodotto è realizzato ne determinano lo stato finale. Nei metalli, i metodi di lavorazione come la laminazione, la forgiatura, il trattamento termico, il taglio, nonché la pulizia e la passivazione, determinano la struttura, la dimensione dei grani, le sollecitazioni residue e la composizione dello strato superficiale che controllano la fatica, la corrosione e l’adesione cellulare. Per l’acciaio, le leghe di Co-Cr e Ti, la monografia discute non solo le proprietà, ma anche le specificità della produzione di impianti, colmando il divario tra l’ingegneria dei materiali e la tecnologia. Questo passaggio dalla scheda tecnica alla scheda di processo è assolutamente fondamentale in medicina.
Nella ceramica, la scelta dei metodi di sintesi e sinterizzazione, il controllo delle frazioni di fase e dei difetti e il trattamento superficiale si traducono in resistenza alla frattura e capacità bioattive. Nelle bioceramiche vetroceramiche e nelle idrossiapatiti in particolare, il controllo preciso della composizione, della cristallinità e della porosità è direttamente correlato all’integrazione dei tessuti e alla resistenza alla compressione. Si tratta di aree in cui la metrologia della porosità, della topografia e dei difetti diventa parte integrante della sicurezza clinica.
Nei polimeri, il processo determina le proprietà del materiale, compresa la sua storia termomeccanica, l’ambiente di ricottura, la scelta della sterilizzazione e gli additivi stabilizzanti, che influenzano il degrado e l’invecchiamento. La monografia richiama l’attenzione su due aree: le modifiche superficiali (fisiche e chimiche) come strumento per migliorare la biocompatibilità e l’adesione delle proteine/cellule e la creazione di superfici con gradiente chimico che consentono lo studio e la manipolazione del comportamento biologico. Dal punto di vista della produzione, ciò significa che la preparazione della superficie, come il plasma, la silanizzazione e gli strati innestati, dovrebbe essere un’operazione di processo convalidata e ripetibile, non un’arte.
Nell’ingegneria tissutale e nella produzione di organi bioibridi, la tecnologia comprende la costruzione di microarchitetture di scaffold, metodi per sterilizzarle senza comprometterne la funzione biologica e il controllo dei parametri del bioreattore e delle procedure di colonizzazione cellulare. Quando si progettano capsule immunoprotettive o architetture aperte, è necessario controllare contemporaneamente la diffusione, la permeabilità e la meccanica delle pareti.
Classi di materiali
Applicando i principi di cui sopra alle indicazioni cliniche, in ortopedia la scelta della coppia portante e della strategia di fissaggio dell’endoprotesi comporta un compromesso tra usura, stabilità meccanica e alla fatica e integrazione biologica con l’osso. Questo è il motivo per cui nella letteratura si è assistito a un intenso sviluppo di rivestimenti porosi e bioattivi e di modifiche superficiali di polimeri ad altissimo peso molecolare. In odontoiatria, una logica simile viene applicata agli impianti e ai restauri, dove ceramiche bioinerte e bioattive, così come titanio/zirconio, sono combinate con la necessità di micro e nano-texture che promuovono l’osteointegrazione e la tenuta biologica della transizione mucosa. Nel sistema cardiovascolare, la progettazione di valvole e innesti è un derivato diretto dell’emodinamica e delle conseguenze procoagulanti della geometria locale e della rugosità.
Nell’area renale, i dispositivi a membrana dimostrano come la teoria della clearance, della permeabilità e del trasporto totale si traduca in un regime terapeutico reale, nella farmacocinetica dei farmaci e nella valutazione dell’adeguatezza della dialisi, e come lievi differenze nelle membrane, nei flussi e nell’idraulica determinino differenze clinicamente significative. La traduzione in ambito clinico richiede la mappatura dei requisiti fisiologici in termini di materiali, geometria, trasporto e parametri di produzione; non esiste un materiale migliore al di fuori del contesto di un’applicazione e di un carico specifici.
Gli editori della monografia indicano la direzione dell’evoluzione: dispositivi che integrano componenti viventi con strutture sintetiche, come organi bioibridi e protesi informative, che forniscono al corpo segnali sostitutivi o modulati per correggere una condizione medica. Non si tratta solo di algoritmi di controllo, ma anche di materiali e interfacce superficiali che devono funzionare in modo prevedibile per anni. Lo sviluppo di dispositivi di robotica morbida e sensori con elevata specificità biologica (enzima-substrato, antigene-anticorpo, ligando-recettore) richiede ai progettisti la padronanza delle tecnologie di micro e nanofabbricazione, nonché la stabilizzazione degli strati attivi.
Ingegneria biomedica nel contesto della scienza dei materiali – sintesi
La seconda edizione del The Biomedical Engineering Handbook fornisce una roadmap completa dell’ingegneria biomedica, che comprende classi di biomateriali, sensori e misurazioni, nonché ingegneria dei tessuti e organi artificiali. Tre temi ricorrono in questa roadmap. Il primo è la sistematicità: materiale, superficie, trasporto, meccanica dei fluidi, elettronica e processo di produzione sono inseparabili e insieme determinano la sicurezza e l’efficacia. Il secondo è la scalabilità: dalle molecole e dai ligandi adesivi, passando per architetture da 10-100 µm, fino ai dispositivi completi, i parametri su una scala devono essere coerenti con i requisiti su altre. Il terzo è la producibilità: la sterilizzazione, la pulizia, il controllo della porosità e della rugosità, la passivazione e le modifiche superficiali non sono elementi aggiuntivi, ma elementi del progetto.
Di conseguenza, il progettista biomedico agisce come un direttore d’orchestra, coordinando materiali, flussi, segnali e processi per innescare la risposta biologica desiderata e ottenere collettivamente la stabilità operativa. Questa prospettiva, sviluppata in modo coerente nella monografia, rimane una base attuale per i professionisti della biomedicina, dell’odontoiatria e della produzione di precisione.
Bibliografia
Bronzino, J.D. (ed.). The Biomedical Engineering Handbook. Second Edition. CRC Press, Boca Raton, 2000.