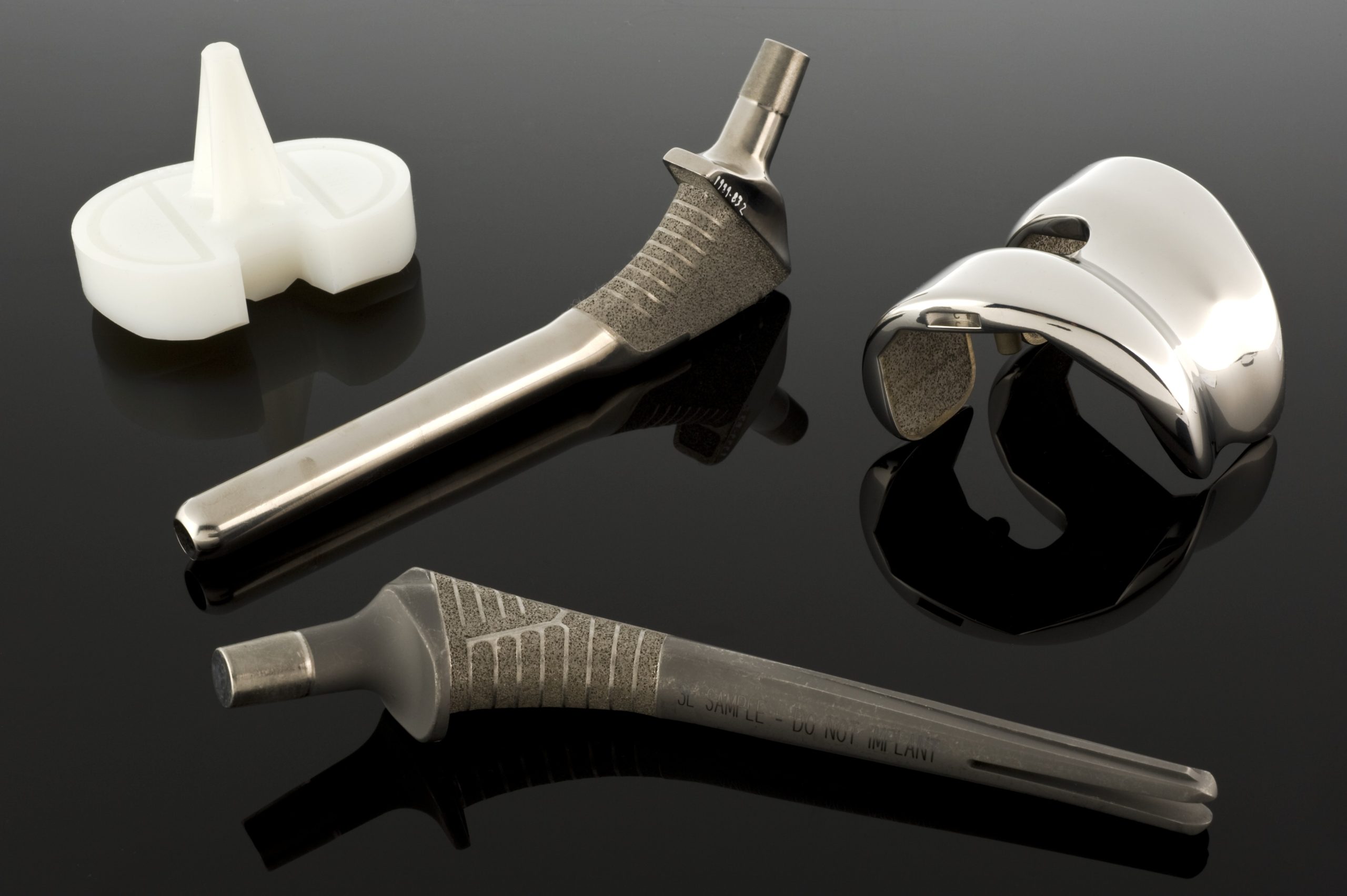
Waarom is het oppervlak van een implantaat zo belangrijk?
In de biomaterialenwetenschap is het verleidelijk om terug te vallen op de intuïtie uit de traditionele materiaalkunde: aangezien een implantaat belastingen moet weerstaan, niet mag corroderen, niet overmatig mag slijten en jarenlang moet functioneren, zou het succes ervan in de eerste plaats moeten afhangen van het materiaal “van binnen”. Dit is echter slechts een deel van de waarheid. Het materiaal zelf is inderdaad verantwoordelijk voor de sterkte, stijfheid, elasticiteit, duurzaamheid en doorlaatbaarheid. Vanuit het perspectief van het lichaam vindt het eerste en belangrijkste contact echter niet plaats met het gehele materiaalblok, maar met de buitenste laag. Het is deze laag die in contact komt met bloed, eiwitten, cellen en lichaamsvloeistoffen.
In de praktijk betekent dit dat een implantaat mechanisch gezien zeer goed kan zijn, maar biologisch problematisch als het oppervlak het ‘verkeerde signaal’ naar de weefsels stuurt. Deze observatie verandert de manier waarop we denken over het ontwerp van implantaten. In plaats van alleen te vragen “waaruit moet het implantaat bestaan?”, moeten we ons afvragen hoe het oppervlak van het implantaat eruit moet zien. Bij biomaterialen is de biologische reactie geen eenvoudige weerspiegeling van de chemische samenstelling van het gehele onderdeel. Het is veeleer een reactie op wat er gebeurt op het grensvlak tussen materiaal en weefsel: de oppervlaktechemie, bevochtigbaarheid, lading, ruwheid, organisatie en reactiviteit. Dit is de reden waarom het succes van een implantaat zo vaak niet wordt bepaald door het volume van het materiaal, maar juist aan het grensvlak.
Dit artikel is gebaseerd op Biomaterials Science: An Introduction to Materials in Medicine, red. William R. Wagner et al., 4e druk, 2020. De volgende inhoud is slechts een algemeen overzicht van het onderwerp. Voor wie geïnteresseerd is in het onderwerp, raden we aan zich te verdiepen in de literatuur.
Hoe reageert het lichaam op het oppervlak van een materiaal?
Het belangrijkste uitgangspunt is eenvoudig: het lichaam ‘ziet’ niet het gehele implantaat in één keer. Eerst ‘leest’ het het oppervlak. De auteurs van Biomaterials Science stellen expliciet dat voor materialen die geen ongewenste stoffen afgeven, de overdracht van informatie van het materiaal naar eiwitten, cellen en het gehele lichaam plaatsvindt via de oppervlaktestructuur. Het lichaam reageert dus op de specifieke chemische samenstelling en organisatie van de buitenste laag, in plaats van op de gemiddelde eigenschappen van het gehele materiaal.
Deze ogenschijnlijk kleine verschuiving in nadruk heeft een enorme praktische betekenis, aangezien het de kwestie van biocompatibiliteit verplaatst van het niveau van ‘wat voor soort legering of polymeer we hebben’ naar het niveau van ‘hoe het grensvlak eruitziet en zich gedraagt’. Het is belangrijk om te onthouden dat het oppervlak niet simpelweg een dunne voortzetting van het materiaal is die zich op dezelfde manier gedraagt als het binnenste. Het boek benadrukt dat het oppervlak een zone is met een bijzondere reactiviteit en bijna onvermijdelijk verschilt van de bulk. Bij een echt metaal kan de buitenste laag niet alleen metaaloxide bevatten, maar ook geadsorbeerd water, polaire organische verbindingen en koolwaterstofverontreinigingen. Bij polymeren kan de unieke oppervlaktezone variëren van ongeveer 10 tot 100 nm.
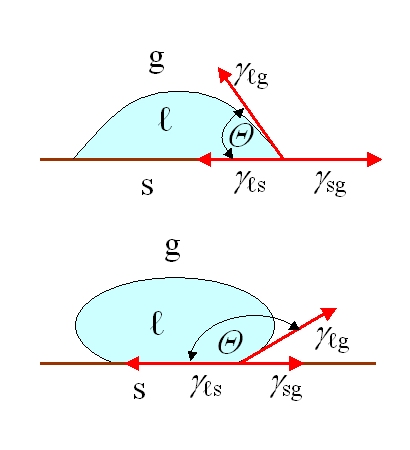
Dit is belangrijk omdat het betekent dat zelfs als het materiaal in de bulk homogeen is, het biologisch actieve deel ervan chemisch en structureel complex kan zijn. Vanuit biologisch perspectief is het oppervlak niet louter een kwestie van chemische samenstelling. De auteurs noemen vele kenmerken die biologische reacties kunnen beïnvloeden: ruwheid, patronen en topografie, bevochtigbaarheid, oppervlaktemobiliteit, chemische samenstelling, elektrische lading, kristalliniteit, elasticiteitsmodulus en heterogeniteit. Tegelijkertijd merken zij eerlijk op dat het nog niet mogelijk is om één enkel universeel kenmerk te identificeren dat voor elke biologische reactie het belangrijkst is. In de praktijk is dit een zeer technisch georiënteerde les; men mag een ontwerp niet baseren op één enkele parametrische slogan zoals “laten we de ruwheid verhogen” of “laten we het oppervlak hydrofieler maken”, omdat de reactie van het lichaam het resultaat is van de interactie van meerdere kenmerken tegelijk.
Deze benadering verklaart waarom twee implantaten gemaakt van hetzelfde basismateriaal zich biologisch verschillend kunnen gedragen. Een verandering in de verwerking, sterilisatie, opslag of verpakking is voldoende om de toestand van het oppervlak te wijzigen. Het boek belicht zelfs alledaagse zaken als vingerafdrukken, additieven die uit de verpakking migreren, of verontreinigingen van papier of folie. In het laboratorium is dit een detail, maar in de praktijk zijn het juist zulke details die ertoe kunnen leiden dat we een oppervlak testen dat niet overeenkomt met het oppervlak dat daadwerkelijk op het klinisch gebruikte implantaat aanwezig is.

Hoe het oppervlak zich vertaalt naar biocompatibiliteit
Als het oppervlak de primaire communicatietaal is tussen het implantaat en het lichaam, moeten we ons afvragen hoe deze dialoog eruitziet. Een van de belangrijkste mechanismen is eiwitadsorptie. De bron benadrukt dat na implantatie van een synthetisch biomateriaal adhesieve eiwitten zich zeer snel, binnen enkele seconden, aan het oppervlak hechten. Op deze manier wordt een materiaal dat op zichzelf geen biologische herkenningsmotieven heeft, “leesbaar” voor het lichaam.
Met andere woorden, cellen reageren vaak niet direct op het zuivere materiaal, maar op de laag eiwitten die zich kort na contact met het lichaam op het oppervlak vormt. Dit heeft fundamentele implicaties voor het begrip van biocompatibiliteit. Biocompatibiliteit betekent niet louter de afwezigheid van acute toxiciteit. Het duidt op het vermogen van het materiaal om in een specifieke toepassing een passende reactie van de gastheer op te wekken. Deze ‘passende reactie’ kan voor een stent het ene betekenen, voor een orthopedisch implantaat iets anders, en voor een katheter weer iets anders.
In elk van deze gevallen bepaalt het oppervlak de eerste biologische gebeurtenissen: welke eiwitten zullen adsorberen, in welke configuratie, welke celreceptoren zullen worden gestimuleerd, en of het signaal zal leiden tot weefselintegratie, bloedplaatjesactivatie, biofilmvorming of een reactie op een vreemd lichaam. Een goed voorbeeld is de vergelijking van adhesie-eiwitten en passiverende eiwitten. Het boek beschrijft hoe het vooraf coaten van een oppervlak met fibronectine de adhesie van veel cellen verhoogt, terwijl albumine deze kan beperken. Dit is niet alleen een curiositeit uit de celcultuur, maar een model van wat er op implantaten gebeurt.
Het oppervlak is geen neutrale achtergrond. Het bepaalt de uitgangsvoorwaarden voor de daaropvolgende cellulaire respons. In de praktijk betekent dit dat twee oppervlakken met vergelijkbare mechanische sterkte tot totaal verschillende genezingstrajecten kunnen leiden, simpelweg omdat ze de eerste laag geadsorbeerde eiwitten op verschillende wijze tot stand brengen. Even belangrijk zijn de interacties tussen het oppervlak en micro-organismen. In het hoofdstuk over biofilms merken de auteurs op dat bevochtigbaarheid, lading, ruwheid en topografie de bacteriële adhesie beïnvloeden.
De algemene trend is dat een grotere ruwheid vaak de bacteriële hechting bevordert, en dat hydrofobe oppervlakken vaker de hechting van bacteriën vergemakkelijken. Tegelijkertijd is dit geen regel zonder uitzonderingen, aangezien extreem superhydrofiele of superhydrofobe systemen via een ander mechanisme als biofilmremmers kunnen fungeren. In de praktijk dient dit als een waarschuwing: een oplossing die gunstig is voor weefselintegratie zal niet altijd even gunstig zijn voor het beheersen van bacteriële kolonisatie. Hieronder staat een Engelstalige video getiteld BIOE 5820 Biomaterials Protein Adsorption, een lezing over eiwitadsorptie op oppervlakken van biomaterialen.
Waarom het oppervlak modificeren in plaats van het gehele materiaal
Dit is de belangrijkste reden achter oppervlaktemodificatie. Als het bulkmateriaal verantwoordelijk is voor draagvermogen, duurzaamheid en mechanische functie, terwijl het oppervlak verantwoordelijk is voor bio-interactie, is het het meest logisch om te behouden wat goed werkt in de bulk en alleen datgene te modificeren wat in contact komt met het weefsel. Dit is precies hoe de auteurs van het hoofdstuk over fysisch-chemische oppervlakteaanpassingen het formuleren: het doel is om de belangrijkste fysische eigenschappen van het biomateriaal te behouden en alleen de buitenste laag te wijzigen om de biologische respons op het grensvlak tussen weefsel en implantaat te verbeteren of te moduleren. Deze aanpak heeft verschillende zeer praktische voordelen. Ten eerste is het niet nodig om af te zien van een materiaal waarvan de mechanische en technologische eigenschappen goed bekend zijn.
Titanium, staal, technische polymeren of elastomeren kunnen hun structurele of functionele rol blijven vervullen. Ten tweede kan de biologische reactie nauwkeuriger worden afgestemd op een bepaalde toepassing. We willen een ander oppervlak voor een botimplantaat, een ander voor een onderdeel dat in contact komt met bloed, en weer een ander voor een katheter, waarbij de prioriteit wellicht ligt bij het beperken van eiwitadsorptie en de hechting van cellen of bacteriën. Ten derde maakt oppervlaktebehandeling het mogelijk een hulpmiddel te verbeteren zonder de gehele structuur volledig opnieuw te hoeven ontwerpen.
Het boek benadrukt zelfs dat dit voor hulpmiddelen die al goed ingeburgerd zijn in de klinische praktijk een manier is om bio-interacties te wijzigen zonder het product opnieuw te ontwerpen, de productie om te schakelen of medisch personeel opnieuw te trainen in het gebruik van de nieuwe oplossing. Er is echter een voorwaarde: men moet onderscheid maken tussen een echte wijziging van het grensvlak en een cosmetische verandering in de beschrijving. De loutere bewering dat een materiaal “bioactief” of “antifouling” is, zegt weinig als onbekend is hoe het oppervlak er in zijn uiteindelijke vorm na verwerking en sterilisatie daadwerkelijk uitziet. De bron merkt op dat het geanalyseerde monster zo nauw mogelijk moet overeenkomen met het materiaal of hulpmiddel in de vorm die wordt gebruikt voor biologische tests of implantatie. Dit is belangrijk omdat het oppervlak dat aan de lucht wordt blootgesteld, mogelijk niet hetzelfde oppervlak is dat het materiaal vertoont in de waterige omgeving van het lichaam.
Drie hoofdmethoden van oppervlaktemodificatie
De eerste methode houdt in dat het bestaande oppervlak wordt gewijzigd zonder een aparte, nieuwe laag toe te voegen. Atomen, moleculen en bindingen die al in de buitenste laag van het materiaal aanwezig zijn, kunnen chemisch of fysisch worden getransformeerd. Tot deze groep behoren onder andere etsen, chemische activering, mechanische opruwing, ionenimplantatie en bepaalde laserbehandelingen. Het punt is dat we geen nieuwe laag aan het implantaat ‘bevestigen’, maar juist het eigen oppervlak ervan hermodelleren. Dit biedt voordelen wanneer een sterke integratie van de modificatie met het substraat belangrijk is, en vermindert bovendien het risico op delaminatie en verandert eigenschappen zoals reactiviteit, bevochtigbaarheid, corrosiebestendigheid, hardheid of bioactiviteit. De bron laat bijvoorbeeld zien dat ionenimplantatie de slijtvastheid of corrosiebestendigheid kan verbeteren, en dat laserbewerking de oppervlakteruwheid, kristalliniteit en chemische samenstelling op gecontroleerde wijze kan wijzigen.
De tweede benadering betreft het aanbrengen van een nieuwe laag of coating. In dit geval wordt een materiaal met een andere samenstelling of eigenschappen op het bestaande oppervlak aangebracht. Dit kan een dunne film, een geënte laag, een polymeercoating of een systeem zijn dat is ontworpen als een niet-aangroeiend oppervlak. Deze strategie is met name waardevol wanneer het substraat ideale mechanische eigenschappen heeft, maar vanuit biologisch oogpunt te ‘ruw’ is. Een goed voorbeeld zijn oppervlakken die bestand zijn tegen niet-specifieke eiwitadsorptie. Hun mechanisme berust meestal op een sterke hydratatielaag, die fungeert als een energetische en fysieke barrière voor eiwitten.
In het hoofdstuk over niet-aangroeiende oppervlakken beschrijven de auteurs twee belangrijke strategieën voor het toepassen van dergelijke systemen: “graft-to-surface”, waarbij het materiaal uit een oplossing adsorbeert of zich bindt, en “graft-from-surface”, waarbij polymeerborstels vanaf het oppervlak groeien. De eerste benadering is technologisch eenvoudiger; de tweede bereikt gemakkelijker een hoge pakkingsdichtheid, maar vereist doorgaans complexere chemie en voorbereiding van het substraat. In de praktijk heeft dit verschil technische betekenis. Als we alleen snel eiwitafzetting op een relatief eenvoudig substraat willen beperken, kan de eenvoudigere oplossing volstaan. Als we echter een duurzame, ondoordringbare en dicht gepakte anti-adsorptielaag nodig hebben, is het simpelweg “plakken” van moleculen aan het oppervlak wellicht niet voldoende. Het boek benadrukt duidelijk dat de keuze van de methode bepalend is voor de pakkingsdichtheid, het aantal defecten en de duurzaamheid van het uiteindelijke oppervlak.
Dit betekent dat coatings niet uitsluitend worden beoordeeld op basis van hun opgegeven chemische samenstelling, maar op basis van de vraag of ze onder bedrijfsomstandigheden daadwerkelijk een homogeen, stabiel grensvlak vormen. De derde benadering betreft het creëren van patronen, texturen en topografieën. Hier ligt de primaire focus niet op het veranderen van de chemische samenstelling, maar op het wijzigen van de geometrie van wat de cel of het eiwit ‘ziet’. De bron benadrukt dat oppervlaktetopografie invloed heeft op celadhesie, proliferatie, migratie, differentiatie en genexpressie. Cellen reageren op zowel micro- als nanoschaalkenmerken, niet alleen op de loutere aanwezigheid van het materiaal. In de studies die in het boek worden aangehaald, veranderden variërende hoogtes, afmetingen en afstanden van topografische structuren de mate van mineralisatie, celoriëntatie, celadhesie en differentiatie.
Dit betekent dat textuur niet louter een versiering of een neveneffect van de verwerking is, maar een actief instrument voor het sturen van biologische reacties. Dit is met name duidelijk bij bot- en tandheelkundige implantaten. Het boek beschrijft hoe een op de juiste wijze ruwe of driedimensionale oppervlaktelaag de vroege stadia van genezing kan versnellen en fibrineafzetting, integrinebinding en micromechanische vergrendeling met bot kan bevorderen. Als gevolg hiervan neemt de afschuifsterkte op het grensvlak tussen implantaat en bot toe en verbetert de belastingsoverdracht. Dit is een goed voorbeeld van hoe texturering geen “blinde verbetering” is, maar een poging om een specifiek grensvlakmechanisme te beheersen. Voorzichtigheid is echter geboden, aangezien dezelfde ruwheid die osseo-integratie bevordert, in een andere toepassing het risico op bacteriële kolonisatie kan vergroten of de oppervlaktecontrole kan belemmeren.

Veelvoorkomende fouten, valkuilen en misleidende aanwijzingen
De meest voorkomende fout is het gelijkstellen van ‘beter materiaal’ aan ‘betere biologische reactie’. Dat is te simplistisch. Sterkte, vermoeidheidsweerstand en chemische stabiliteit verklaren nog niet wat er aan het weefselgrensvlak zal gebeuren. Bij biomaterialen kan men een uitstekend structureel materiaal hebben en een slecht biologisch grensvlak. Het is ook mogelijk om met het tegenovergestelde probleem te maken te krijgen: een zeer biologisch actief oppervlak gemonteerd op een substraat dat niet aan de mechanische eisen voldoet. Dit is precies waarom het uitgangspunt dat het materiaal het implantaat sterkte geeft, terwijl het oppervlak de reactie van het lichaam bepaalt, nuttig is bij het ontwerp.
Het dwingt ons om twee vragen te scheiden die in de klassieke techniek vaak met elkaar worden verward. De tweede valkuil is de overtuiging dat één enkele oppervlakte-eigenschap het hele probleem zal oplossen. In de praktijk bestaat er geen universele “biocompatibiliteitsinstelling”. Het verhogen van de hydrofiliteit kan de adsorptie van bepaalde eiwitten beperken, maar het verbetert niet noodzakelijkerwijs de weefselintegratie. Het vergroten van de ruwheid kan de reactie van osteoblasten bevorderen, maar is mogelijk niet gunstig voor een omgeving met een infectierisico. In het boek zelf wordt opgemerkt dat het nog niet bekend is welke parameter het belangrijkst is voor elke specifieke biologische reactie, dus moeten variabelen onafhankelijk van elkaar worden gemeten en gecorreleerd.
Dit is een zeer belangrijke methodologische richtlijn: in plaats van te zoeken naar één enkel magisch getal, moet men een kaart opstellen van de relaties tussen verschillende eigenschappen van het grensvlak en een specifiek klinisch doel. De derde valkuil betreft de dikte van de modificatie. De auteurs van het hoofdstuk over fysisch-chemische modificaties benadrukken dat modificaties zo dun mogelijk moeten zijn. Idealiter zou het volstaan om slechts de buitenste paar moleculaire lagen – in de orde van enkele nanometers – te wijzigen, hoewel de lagen in de praktijk soms dikker moeten zijn om uniformiteit en duurzaamheid te garanderen. Een te dikke coating kan de mechanische en functionele eigenschappen van het hulpmiddel veranderen en het risico op barsten en delaminatie vergroten. Dit is met name belangrijk wanneer het implantaat wordt blootgesteld aan vermoeidheid of wrijving.
Een laag die er vanuit biologisch oogpunt veelbelovend uitziet, maar na enige tijd mechanisch afbladdert, lost het probleem niet op; het creëert slechts een nieuw probleem. De vierde misvatting is het beschouwen van het oppervlak als een statische toestand. De bron toont aan dat sommige materialen hun oppervlakteorganisatie kunnen omkeren bij de overgang van lucht naar een waterige omgeving. Een oppervlak dat “in droge omstandigheden” is gemeten, is mogelijk niet hetzelfde oppervlak dat eiwitten en cellen in het lichaam aantreffen. Dit heeft directe gevolgen voor onderzoek. Als bij oppervlakteanalyse geen rekening wordt gehouden met de gebruiksomgeving, zou men een parameter kunnen optimaliseren die na implantatie niet langer dezelfde waarde of betekenis heeft.
Wanneer een meer geavanceerde theorie nodig is
Een geavanceerde benadering wordt noodzakelijk wanneer intuïtieve termen als ‘gladder’, ‘hydrofieler’ of ‘ruwer’ niet langer volstaan. Niet-aangroeiende oppervlakken zijn hier een voorbeeld van. Hun functie vloeit niet simpelweg voort uit het feit dat ze glad zijn, maar uit het feit dat ze een stabiele hydratatielaag vormen, waarvan de verwijdering energetisch ongunstig is voor adsorberende eiwitten. Het boek laat zien dat op PEG gebaseerde hydrofiele materialen water binden via waterstofbruggen, terwijl zwitterionische materialen dit nog sterker kunnen doen via elektrostatisch geïnduceerde hydratatie.
Op dit niveau moet men niet alleen rekening houden met functionele chemie, maar ook met de ketenpakkingsdichtheid, de conformationele vrijheid en de stabiliteit van de verankering van de laag. Geavanceerde theorie is ook nodig wanneer het oppervlak niet alleen bedoeld is om niet te interfereren, maar om het celgedrag actief te sturen. In dergelijke gevallen gaat het om geometrie op micro- en nanoschaal, lokale mechanica, de grootte, hoogte en afstand van topografische kenmerken, en soms zelfs de orde of wanorde van het patroon. Dit is precies de reden waarom het onderzoek tegenwoordig gebruikmaakt van topografische matrices en meer systematische oppervlaktescreenings. Dit gaat niet over de academische complexiteit van het onderwerp, maar over het feit dat cellen echt onderscheid maken tussen schalen en patronen van kenmerken, en dat de biologische reactie niet langer een lineaire functie is van één enkele parameter.
Waarom is het oppervlak van een implantaat zo belangrijk? – samenvatting
Bij biomaterialen wordt het succes van een implantaat vaak niet bepaald door het materiaal zelf, maar door het oppervlak dat het aan het lichaam presenteert. Het oppervlak is het eerste contactpunt met eiwitten, cellen en lichaamsvloeistoffen en bepaalt dus grotendeels de biocompatibiliteit. Om deze reden houdt een verstandig implantaatontwerp een scheiding van functies in: het volume is bedoeld om mechanische eigenschappen en duurzaamheid te waarborgen, terwijl het oppervlak bedoeld is om de juiste biologische reactie op te wekken. Dit is de basis voor de gehele logica van het aanpassen van het oppervlak zonder het gehele materiaal te veranderen. Men kan de bestaande buitenlaag hermodelleren, een nieuwe coating aanbrengen of een patroon en topografie ontwerpen die de eiwitadsorptie, het celgedrag, de weefselintegratie of de weerstand tegen aangroei beïnvloeden. Er is één voorwaarde: de modificatie moet echt interfaciaal, dun, duurzaam en afgestemd op een specifiek klinisch doel zijn. Dit is precies de reden waarom het oppervlak bij biomaterialen geen afwerkingsdetail is, maar een van de belangrijkste instrumenten bij het ontwerp van implantaten.