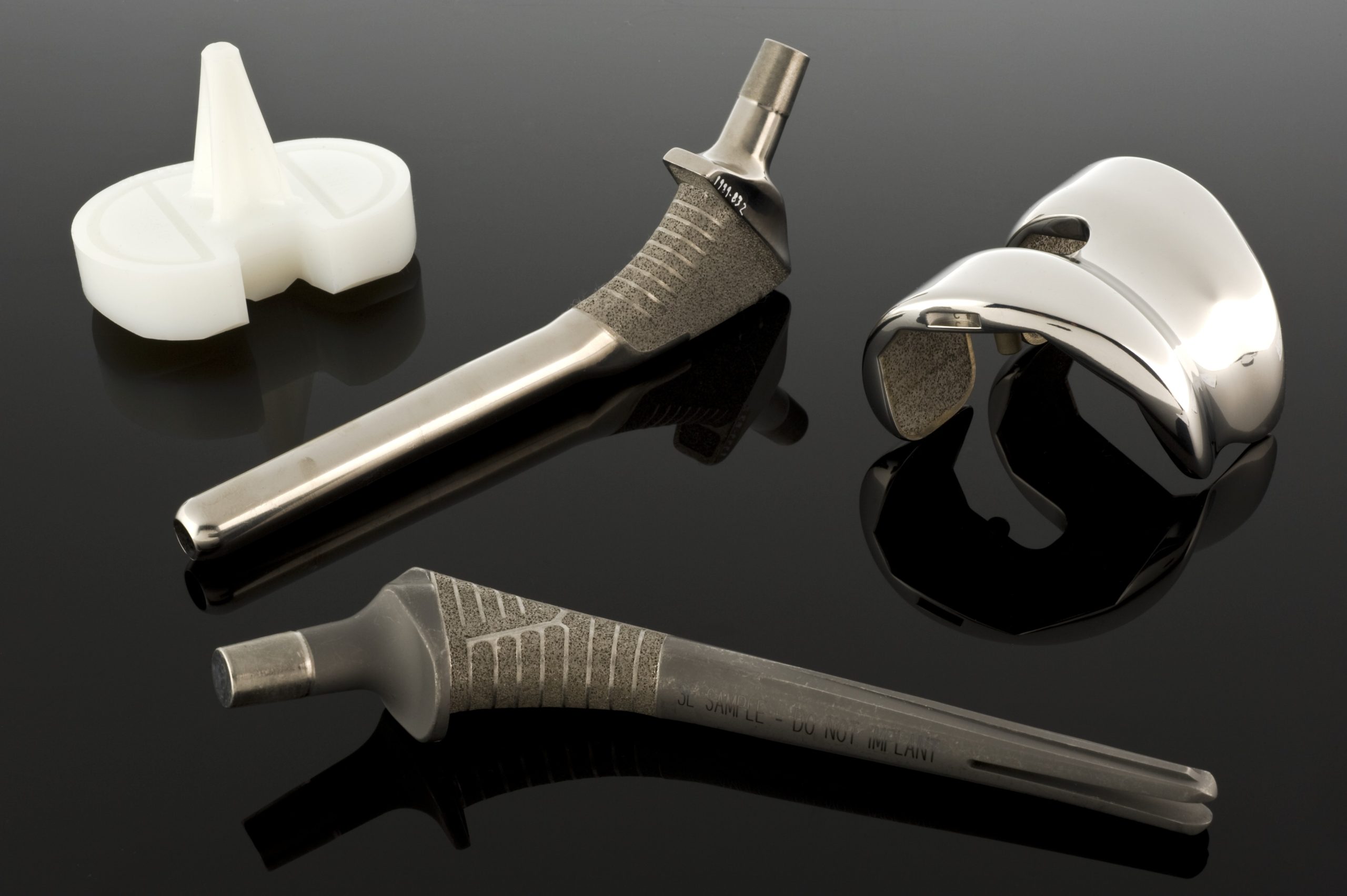
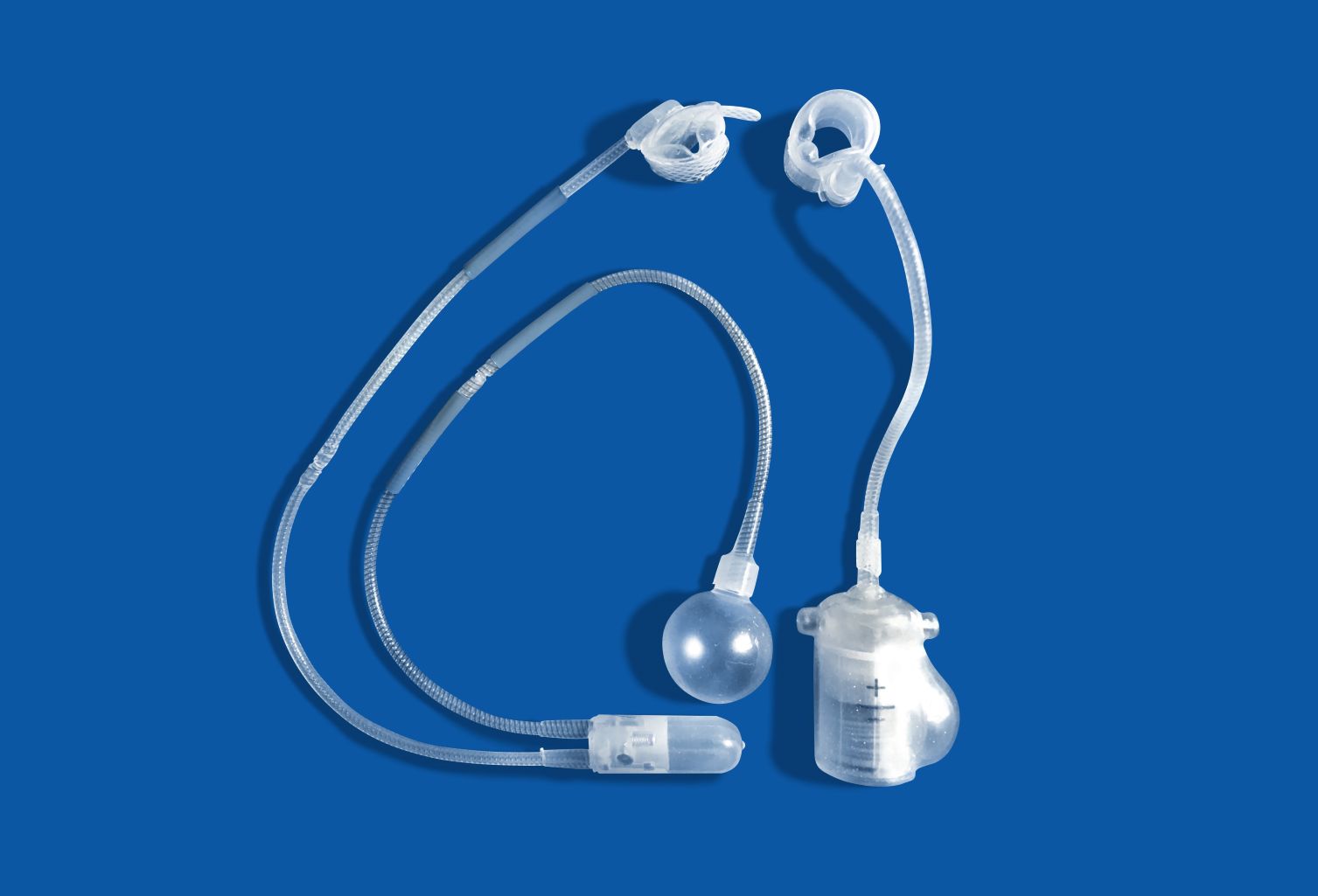
Perché la superficie di un impianto è così importante?
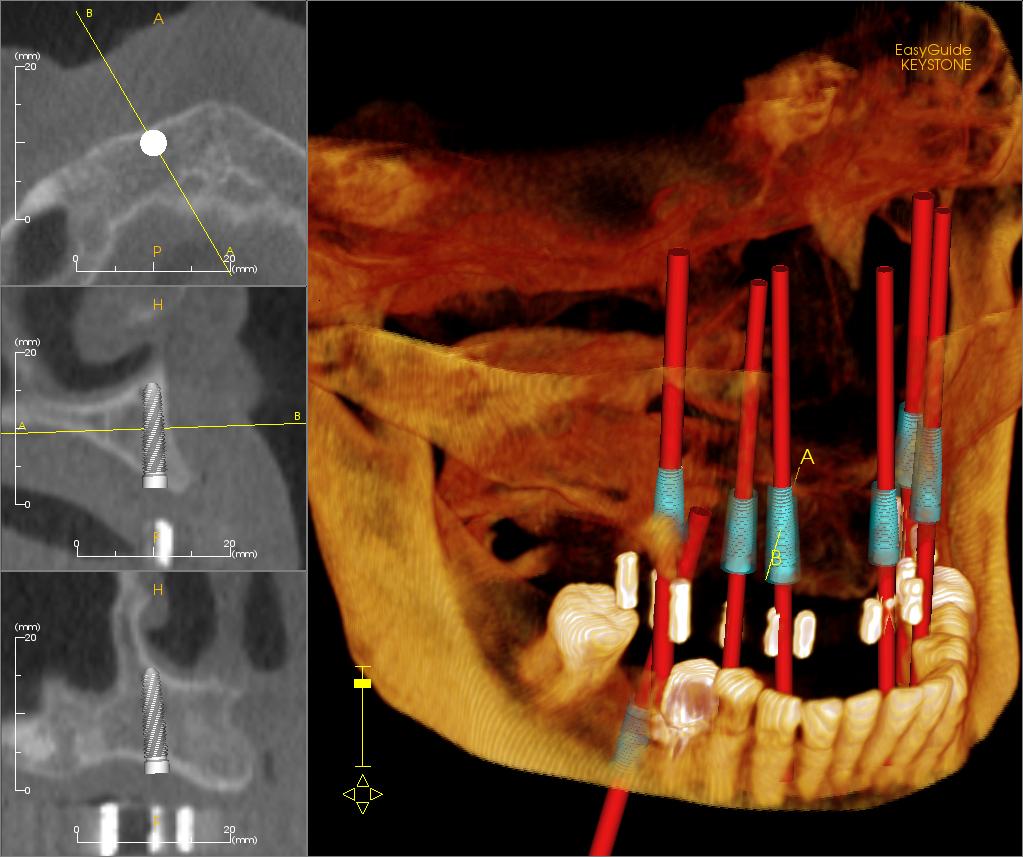
Nell’ingegneria dei biomateriali, è facile affidarsi all’intuizione derivata dalla scienza dei materiali tradizionale: poiché un impianto deve resistere ai carichi, non corrodersi, non usurarsi eccessivamente e funzionare per anni, il suo successo dovrebbe dipendere principalmente dal materiale “all’interno”. Questa è solo una parte della verità. Il materiale di base è infatti responsabile della resistenza, della rigidità, dell’elasticità, della durata e della permeabilità; tuttavia, dal punto di vista del corpo, il primo e più importante contatto non avviene con l’intero blocco di materiale, ma con il suo strato esterno. È questo strato che entra in contatto con sangue, proteine, cellule e fluidi corporei. In pratica, ciò significa che un impianto può essere meccanicamente ottimo ma biologicamente problematico se la sua superficie invia il “segnale sbagliato” ai tessuti.
Questa osservazione cambia il modo in cui concepiamo la progettazione degli impianti. Anziché chiederci solo “di cosa dovrebbe essere fatto l’impianto?”, dobbiamo considerare come dovrebbe essere la superficie dello stesso. Nei biomateriali, la risposta biologica non è un semplice riflesso della composizione chimica dell’intero componente. È piuttosto una risposta a ciò che accade all’interfaccia materiale-tessuto: la chimica superficiale, la bagnabilità, la carica, la rugosità, l’organizzazione e la reattività. Ecco perché il successo di un impianto è spesso determinato non dal volume del materiale, ma proprio dal confine di fase.
Questo articolo si basa su Biomaterials Science: An Introduction to Materials in Medicine, a cura di William R. Wagner et al., 4a ed., 2020. Il contenuto che segue è solo una panoramica generale dell’argomento. A chi fosse interessato all’argomento, consigliamo di approfondire la letteratura.
Come reagisce il corpo alla superficie di un materiale?
Il punto di partenza più importante è semplice: il corpo non “vede” l’intero impianto tutto in volta. Per prima cosa, “legge” la sua superficie. Gli autori di Biomaterials Science affermano esplicitamente che, per i materiali che non rilasciano sostanze indesiderate, il trasferimento di informazioni dal materiale alle proteine, alle cellule e all’intero corpo avviene attraverso la struttura superficiale. Il corpo, quindi, risponde alla chimica e all’organizzazione specifiche dello strato esterno, piuttosto che alle proprietà medie dell’intero materiale. Questo cambiamento di enfasi, apparentemente minore, ha un enorme significato pratico, poiché sposta la questione della biocompatibilità dal livello di “che tipo di lega o polimero abbiamo” al livello di “come appare e si comporta la sua interfaccia”.
È importante ricordare che la superficie non è semplicemente un sottile strato del materiale che si comporta allo stesso modo del suo interno. Il libro sottolinea che la superficie è una zona di particolare reattività e differisce quasi inevitabilmente dalla massa. Per un vero materiale metallico, lo strato esterno può includere non solo ossido metallico, ma anche acqua adsorbita, composti organici polari e contaminanti idrocarburici. Per i polimeri, la zona superficiale specifica può variare da circa 10 a 100 nm. Questo è importante perché significa che, anche se il materiale di massa è omogeneo, la sua porzione biologicamente attiva può essere chimicamente e strutturalmente complessa.
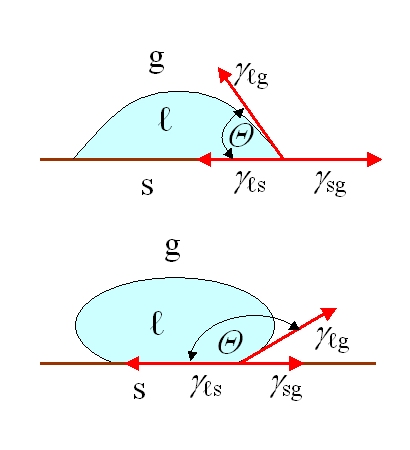
Da un punto di vista biologico, la superficie non è semplicemente una questione di composizione chimica. Gli autori elencano molte caratteristiche che possono influenzare le risposte biologiche: rugosità, modelli e topografia, bagnabilità, mobilità superficiale, composizione chimica, carica elettrica, cristallinità, modulo elastico ed eterogeneità. Allo stesso tempo, osservano onestamente che non è ancora possibile determinare un’unica caratteristica universale che sia la più importante per ogni risposta biologica. In pratica, questa è una lezione fortemente orientata all’ingegneria; non si deve basare un progetto su un unico slogan parametrico come “aumentiamo la rugosità” o “rendiamo la superficie più idrofila”, poiché la risposta dell’organismo è il risultato dell’interazione di diverse caratteristiche contemporaneamente.
Questo approccio spiega perché due impianti realizzati con lo stesso materiale di base possano comportarsi biologicamente in modo diverso. Un cambiamento nella lavorazione, nella sterilizzazione, nella conservazione o nel confezionamento è sufficiente a modificare le condizioni della superficie. Il libro mette in evidenza anche questioni banali come le impronte digitali, gli additivi che migrano dall’imballaggio o i contaminanti provenienti dalla carta o dalla pellicola. In laboratorio, questo è un dettaglio, ma nella realtà sono proprio questi particolari che possono portarci a testare una superficie che non è quella effettivamente presente sull’impianto utilizzato clinicamente.

Come la superficie si traduce in biocompatibilità
Se la superficie è il linguaggio primario di comunicazione tra l’impianto e il corpo, dobbiamo chiederci come si presenta questo dialogo. Uno dei meccanismi chiave è l’adsorbimento delle proteine. La fonte sottolinea che dopo l’impianto di un biomateriale sintetico, le proteine adesive si adsorbono sulla sua superficie molto rapidamente, nel giro di pochi secondi. In questo modo, un materiale che di per sé è privo di motivi di riconoscimento biologico diventa “leggibile” per il corpo. In altre parole, le cellule spesso non reagiscono direttamente al materiale puro, ma allo strato di proteine che si forma sulla sua superficie poco dopo il contatto con il corpo.
Ciò pone un’implicazione fondamentale per la comprensione della biocompatibilità. La biocompatibilità non significa semplicemente l’assenza di tossicità acuta. Significa che il materiale può suscitare una risposta appropriata dell’ospite in una specifica applicazione. Questa “risposta appropriata” può avere un significato differente nel caso di uno stent, un altro per un impianto ortopedico e un altro ancora per un catetere. In ciascuno di questi casi, la superficie controlla gli eventi biologici iniziali: quali proteine si adsorberanno, in quale configurazione, quali recettori cellulari saranno stimolati e se il segnale procederà verso l’integrazione tissutale, l’attivazione piastrinica, la formazione di biofilm o una reazione da corpo estraneo.
Un buon esempio è il confronto tra proteine di adesione e proteine di passivazione. Il libro descrive come il pre-rivestimento di una superficie con fibronectina aumenti l’adesione di molte cellule, mentre l’albumina può limitarla. Non si tratta solo di una curiosità della coltura cellulare, ma di un modello di ciò che accade sugli impianti. La superficie non è uno sfondo neutro. Essa stabilisce le condizioni iniziali per la successiva risposta cellulare. In pratica, ciò significa che due superfici con resistenza meccanica simile possono portare a traiettorie di guarigione completamente diverse semplicemente perché stabiliscono in modo diverso il primo strato di proteine adsorbite.
Altrettanto importanti sono le interazioni tra la superficie e i microrganismi. Nel capitolo sui biofilm, gli autori osservano che la bagnabilità, la carica, la rugosità e la topografia influenzano l’adesione batterica. La tendenza generale è che una maggiore rugosità spesso favorisce l’adesione batterica, mentre le superfici idrofobiche facilitano più frequentemente l’attaccamento dei batteri. Allo stesso tempo, questa non è una regola senza eccezioni, poiché sistemi estremamente superidrofili o superidrofobici possono agire come inibitori del biofilm attraverso un meccanismo diverso. In pratica, ciò serve da avvertenza: una soluzione benefica per l’integrazione tissutale non sarà sempre altrettanto benefica per il controllo della colonizzazione batterica.
Di seguito è riportato un video in lingua inglese intitolato BIOE 5820 Biomaterials Protein Adsorption, che è una lezione sull’adsorbimento delle proteine sulle superfici dei biomateriali.
Perché modificare la superficie piuttosto che l’intero materiale
Questa è la logica principale alla base della modifica superficiale. Se il materiale di massa è responsabile della capacità di carico, della durata e della funzione meccanica, mentre la superficie è responsabile della biointerazione, ha più senso preservare ciò che funziona bene nella massa e modificare solo ciò che entra in contatto con il tessuto. È esattamente così che lo descrivono gli autori del capitolo sulle modifiche fisico-chimiche delle superfici: l’obiettivo è preservare le proprietà fisiche chiave del biomateriale alterando solo lo strato esterno per migliorare o modulare la risposta biologica all’interfaccia tessuto-dispositivo.
Questo approccio presenta diversi vantaggi molto pratici. In primo luogo, non è necessario abbandonare un materiale ben compreso dal punto di vista meccanico e tecnologico. Il titanio, l’acciaio, i polimeri tecnici o gli elastomeri possono continuare a svolgere il loro ruolo strutturale o funzionale. In secondo luogo, la risposta biologica può essere adattata in modo più preciso a una determinata applicazione. Vogliamo una superficie diversa per un impianto osseo, una diversa per un componente a contatto con il sangue e ancora un’altra per un catetere, dove la priorità potrebbe essere quella di limitare l’adsorbimento delle proteine e l’adesione di cellule o batteri. In terzo luogo, la modifica della superficie consente di migliorare un dispositivo senza dover riprogettare completamente l’intera struttura. Il libro sottolinea addirittura che, per i dispositivi già consolidati nella pratica clinica, questo è un modo per alterare le biointerazioni senza riprogettare il prodotto, riorganizzare la produzione o riqualificare il personale medico all’uso della nuova soluzione.
C’è, tuttavia, una condizione da considerare: occorre distinguere tra una vera e propria modifica dell’interfaccia e un cambiamento puramente estetico nella descrizione. La semplice afffermazione secondo la quale un materiale è “bioattivo” o “antivegetativo” ha poco significato se non si conosce l’aspetto effettivo della superficie nella sua forma finale dopo la lavorazione e la sterilizzazione. La fonte osserva che il campione analizzato dovrebbe corrispondere il più possibile al materiale o al dispositivo nella forma utilizzata per i test biologici o l’impianto. Ciò è importante perché la superficie esposta all’aria potrebbe non essere la stessa che il materiale presenta nell’ambiente acquoso del corpo.
Tre metodi principali di modifica superficiale
Il primo metodo consiste nell’alterare la superficie esistente senza aggiungere un nuovo strato separato. Gli atomi, le molecole e i legami già presenti nello strato esterno del materiale possono essere trasformati chimicamente o fisicamente. Questo gruppo comprende, tra l’altro, l’incisione, l’attivazione chimica, l’irruvidimento meccanico, l’impianto ionico e alcuni trattamenti laser. Il punto è che non si “attacca” un nuovo strato all’impianto, ma piuttosto si rimodella la sua stessa superficie. Ciò è vantaggioso laddove è importante una forte integrazione della modifica con il substrato, oltre a ridurre il rischio di delaminazione e a modificare proprietà quali reattività, bagnabilità, resistenza alla corrosione, durezza o bioattività. La fonte mostra, ad esempio, che l’impianto ionico può migliorare la resistenza all’usura o alla corrosione, e che la lavorazione laser può alterare in modo controllato la rugosità superficiale, la cristallinità e la composizione chimica.
Il secondo approccio prevede l’applicazione di un nuovo strato o rivestimento. In questo caso, un materiale con composizione o proprietà diverse viene posto sulla superficie esistente. Può trattarsi di un film sottile, di uno strato innestato, di un rivestimento polimerico o di un sistema progettato come superficie antivegetativa. Questa strategia è particolarmente utile quando il substrato ha proprietà meccaniche ideali ma è troppo “grezzo” dal punto di vista biologico. Un buon esempio è costituito dalle superfici resistenti all’adsorbimento proteico non specifico. Il loro meccanismo si basa solitamente su un forte strato di idratazione, che funge da barriera energetica e fisica alle proteine. Nel capitolo sulle superfici antivegetative, gli autori descrivono due strategie principali per l’applicazione di tali sistemi: “graft-to-surface”, in cui il materiale si adsorbe o si lega dalla soluzione, e “graft-from-surface”, in cui le spazzole polimeriche crescono dalla superficie. Il primo approccio è tecnologicamente più semplice; il secondo consente di ottenere più facilmente un’elevata densità di impaccamento, ma di solito richiede una chimica e una preparazione del substrato più complesse.
In pratica, questa differenza ha un significato ingegneristico. Se vogliamo semplicemente limitare rapidamente la deposizione di proteine su un substrato relativamente semplice, la soluzione più semplice può essere sufficiente; tuttavia, se abbiamo bisogno di uno strato anti-adsorbimento durevole, impermeabile e densamente impaccato, il semplice “attaccare” le molecole alla superficie potrebbe non essere sufficiente. Il libro sottolinea chiaramente che la scelta del metodo determina la densità di impacchettamento, il numero di difetti e la durata della superficie finale. Ciò significa che i rivestimenti non vengono valutati esclusivamente in base alla loro composizione chimica dichiarata, ma in base al fatto che formino effettivamente un’interfaccia omogenea e stabile nelle condizioni operative.
Il terzo approccio prevede la creazione di motivi, trame e topografie. In questo caso, l’attenzione principale non è rivolta alla modifica della composizione chimica, ma all’alterazione della geometria di ciò che la cellula o la proteina “vede”. La fonte sottolinea che la topografia superficiale influenza l’adesione, la proliferazione, la migrazione, la differenziazione e l’espressione genica delle cellule. Le cellule rispondono sia alle caratteristiche su scala micro che su scala nanometrica, non solo alla mera presenza del materiale. Negli studi citati nel libro, l’alterazione di altezze, dimensioni e spaziature delle strutture topografiche ha modificato il grado di mineralizzazione, l’orientamento cellulare, l’adesione cellulare e la differenziazione. Ciò significa che la texture non è un semplice ornamento o un effetto collaterale della lavorazione, ma uno strumento attivo per il controllo delle risposte biologiche.
Ciò è particolarmente evidente negli impianti ossei e dentali. Il libro descrive come uno strato superficiale opportunamente ruvido o tridimensionale possa accelerare le prime fasi di guarigione, favorire la deposizione di fibrina, il legame delle integrine e l’interconnessione micromeccanica con l’osso. Di conseguenza, la resistenza al taglio all’interfaccia impianto-osso aumenta e il trasferimento del carico migliora. Questo è un buon esempio di come la testurizzazione non sia un “miglioramento cieco”, ma un tentativo di controllare uno specifico meccanismo interfacciale; tuttavia, è necessaria cautela, poiché la stessa rugosità che favorisce l’osteointegrazione può, in un’altra applicazione, aumentare il rischio di colonizzazione batterica o ostacolare il controllo della superficie.

Errori comuni, insidie e false piste
L’errore più comune è equiparare “materiale migliore” a “migliore risposta biologica”. È troppo semplicistico. Resistenza, resistenza alla fatica e stabilità chimica non spiegano ancora cosa accadrà all’interfaccia tissutale. Nei biomateriali, è possibile avere un materiale strutturale eccellente e un’interfaccia biologica scadente. Si può anche affrontare il problema opposto: una superficie altamente biologicamente attiva montata su un substrato che non soddisfa i requisiti meccanici. Questo è precisamente il motivo per cui la premessa secondo cui il materiale fornisce all’impianto la resistenza, mentre la superficie determina la risposta del corpo, è utile nella progettazione. Ci costringe a separare due questioni che nell’ingegneria classica vengono spesso accorpate.
La seconda insidia è la convinzione che una singola proprietà della superficie risolva l’intero problema. In pratica, non esiste un’impostazione universale di “biocompatibilità”. Aumentare l’idrofilia può limitare l’adsorbimento di alcune proteine, ma non migliora necessariamente l’integrazione tissutale. Aumentare la rugosità può favorire la risposta degli osteoblasti, ma potrebbe non essere vantaggioso in un ambiente a rischio di infezione. Il libro stesso osserva che non è ancora noto quale parametro sia più importante per ciascuna specifica risposta biologica, quindi le variabili devono essere misurate e correlate in modo indipendente. Si tratta di una linea guida metodologica molto importante: invece di cercare un unico numero magico, occorre costruire una mappa delle relazioni tra diverse proprietà dell’interfaccia e uno specifico obiettivo clinico.
La terza insidia riguarda lo spessore della modifica. Gli autori del capitolo sulle modifiche fisico-chimiche sottolineano che le modifiche dovrebbero essere il più sottili possibile. Idealmente, sarebbe sufficiente alterare solo i pochi strati molecolari più esterni (dell’ordine di pochi nanometri) anche se in pratica gli strati a volte devono essere più spessi per garantire uniformità e durata. Un rivestimento troppo spesso può alterare le proprietà meccaniche e funzionali del dispositivo, oltre ad aumentare il rischio di crepe e delaminazione. Ciò è particolarmente importante quando l’impianto è soggetto a fatica o attrito. Uno strato che sembra promettente dal punto di vista biologico ma che si stacca meccanicamente dopo un certo tempo non risolve il problema; ne crea semplicemente uno nuovo.
Il quarto malinteso consiste nel considerare la superficie come uno stato statico. La fonte dimostra che alcuni materiali possono invertire la loro organizzazione superficiale al passaggio dall’aria a un ambiente acquoso. Una superficie misurata “in condizioni di asciutto” potrebbe non essere la stessa superficie che proteine e cellule incontrano nel corpo. Ciò ha implicazioni dirette per la ricerca. Se l’analisi superficiale non tiene conto dell’ambiente operativo, si potrebbe ottimizzare un parametro che smette di avere lo stesso valore o significato dopo l’impianto.
Quando è necessaria una teoria più avanzata
Un approccio avanzato diventa necessario quando termini intuitivi come “più liscio”, “più idrofilo” o “più ruvido” non sono più sufficienti. Le superfici anti-incrostazione ne sono un esempio. La loro funzione non deriva semplicemente dal fatto che sono scivolose, ma dal fatto che formano uno strato di idratazione stabile, la cui rimozione è energeticamente sfavorevole per le proteine adsorbenti. Il libro dimostra che i materiali idrofili a base di PEG legano l’acqua attraverso legami idrogeno, mentre i materiali zwitterionici possono farlo in modo ancora più forte attraverso l’idratazione indotta elettrostaticamente. A questo livello, si deve considerare non solo la chimica funzionale, ma anche la densità di impacchettamento della catena, la libertà conformazionale e la stabilità dell’ancoraggio dello strato.
È necessaria una teoria avanzata anche quando la superficie non deve solo essere non interferente, ma guidare attivamente il comportamento cellulare. In tali casi, ciò che conta è la geometria su scala micro e nanometrica, la meccanica locale, le dimensioni, l’altezza e la spaziatura delle caratteristiche topografiche e, talvolta, persino l’ordine o il disordine del pattern. Questo è precisamente il motivo per cui la ricerca odierna impiega matrici topografiche e screening superficiali più sistematici. Non si tratta della complessità accademica dell’argomento, ma del fatto che le cellule distinguono realmente tra scale e modelli di caratteristiche, e la risposta biologica cessa di essere una funzione lineare di un singolo parametro.
Perché la superficie di un impianto è così importante? – sintesi
Nei biomateriali, il successo di un impianto è spesso determinato non dal materiale di massa in sé, ma dalla superficie che presenta al corpo. È la superficie il primo punto di contatto con proteine, cellule e fluidi corporei, e quindi controlla in larga misura la biocompatibilità. Per questo motivo, una progettazione sensata dell’impianto comporta la separazione delle funzioni: il volume è destinato a garantire proprietà meccaniche e durata, mentre la superficie è destinata a suscitare la risposta biologica appropriata. Questa è la base dell’intera logica di modificare la superficie senza cambiare l’intero materiale. È possibile rimodellare lo strato esterno esistente, applicare un nuovo rivestimento o progettare un motivo e una topografia che influenzino l’adsorbimento delle proteine, il comportamento cellulare, l’integrazione tissutale o la resistenza alle incrostazioni. C’è una condizione: la modifica deve essere veramente interfacciale, sottile, durevole e adattata a uno specifico obiettivo clinico. Questo è precisamente il motivo per cui, nei biomateriali, la superficie non è un dettaglio di finitura, ma uno degli strumenti principali nella progettazione degli impianti.