Polymeeriset biomateriaalit
Sisällysluettelo
Synteettiset polymeerit ovat nykyään yksi tärkeimmistä biomateriaaliryhmistä metallien ja keraamien ohella. Lääketieteessä niitä käytetään kertakäyttötuotteissa, proteeseissa, hammaslääketieteellisissä materiaaleissa, implanteissa, sidoksissa, ekstrakorporaalisissa laitteissa, lääkeannostelujärjestelmissä ja kudostekniikassa.
Niiden asema johtuu useista keskeisistä eduista. Polymeerit ovat suhteellisen helppoja käsitellä ja niitä voidaan käyttää lateksin, kalvojen, kuitujen, putkien, huokoisten tukirakenteiden sekä monimutkaisten muotojen valmistukseen hyvin kehittyneillä muovinjalostustekniikoilla. Niille on ominaista laaja valikoima mekaanisia ja fysikaalisia ominaisuuksia, kovista ja jäykistä rakenneaineista pehmeisiin elastomeereihin ja hydrogeeleihin. Lisäksi ne ovat usein halvempia ja kevyempiä kuin metallit ja helpompia muokata kemiallisesti ja pinnallisesti.
Polymeeristen biomateriaalien vaatimukset eivät poikkea merkittävästi muiden implanttimateriaalien vaatimuksista. Ennen kaikkea niiden odotetaan olevan biologisesti yhteensopivia (myrkyttömiä, syöpää aiheuttamattomia, pyrogeenisiä ja allergeenisia), steriloitavissa tavanomaisilla menetelmillä (autoklaavi, etyleenioksidi, säteily) sekä omaavan tuotteen toimintaan sopivat mekaaniset ja fysikaaliset ominaisuudet ja hyvän prosessoitavuuden (muovattavuus, suulakepuristettavuus, ruiskupuristettavuus, kuitujen muodostettavuus).

Polymerisaation ja polymeerin rakenteen perusteet
Polymeerit muodostuvat yhdistämällä pieniä molekyylejä, eli monomeereja, pitkiksi ketjuiksi. Tämä prosessi voi tapahtua kondensaatio-polymerisaation (vaiheittain) tai additiopolymerisaation (ketju, esim. vapaat radikaalit) kautta.
Kondensaatio-polymerisaatiossa (vaiheittainen reaktio) jokainen ketjun kasvuvaiheeseen liittyy pienen molekyylin, useimmiten veden tai alkoholin, vapautuminen. Tyypillinen esimerkki on polyamidien (nylonien) muodostuminen aminoryhmän ja karboksyyliryhmän reagoidessa amidisidoksen muodostamiseksi ja veden vapautuessa. Näin muodostuvat polyesterit, polyamidit, polyuretaanit, polysiloksaanit sekä luonnolliset proteiinit ja polysakkaridit, joita myös tuotetaan kondensaatiolla vesimolekyylien vapautuessa.
Monien lääketieteellisten muovien tyypillisen polymeroinnin lisäksi monomeeri sisältää yleensä kaksoissidoksen, joka katkeaa initiaattorin vaikutuksesta – yleensä vapaiden radikaalien, joita syntyy esimerkiksi peroksideista (bentsoyyliperoksidi) lämmön tai UV-säteilyn vaikutuksesta. Näin muodostuu useita suosittuja polymeerejä, kuten polyeteeni, polypropeeni, polyvinyylikloridi, polystyreeni ja poly(metyylimetakrylaatti).
Polymeerimakromolekyylin rakenne määrää sen ominaisuudet. Ketjut voivat olla lineaarisia, haarautuneita tai silloitettuja. Lineaariset polymeerit (esim. klassiset polyesterit tai polyamidit) voivat kiteytyä merkittävässä määrin muodostaen puolikiteisen järjestelmän, jossa järjestäytyneet alueet esiintyvät yhdessä amorfisten alueiden kanssa. Ristisidokset, kuten silikonielastomeerien tai vulkanoinnin jälkeen luonnonkumissa, rajoittavat ketjujen liikkuvuutta, estävät usein kiteytymisen ja johtavat jäykkien kolmiulotteisten verkostojen muodostumiseen.
Polymeerien ominaisuudet riippuvat suuresti polymeroitumisasteesta, eli ketjussa toistuvien yksiköiden lukumäärästä, sekä jäännösryhmien (substituenttien) sijainnista ja jakautumisesta. Mitä suurempi molekyylipaino, sitä pienempi ketjujen liikkuvuus, mikä tarkoittaa suurempaa lujuutta ja lämmön vakautta, mutta myös vaikeampaa muokattavuutta. Materiaali kuvataan yleensä keskimääräisellä Mn:llä (lukukeskimääräinen massa) ja Mw:llä (painokeskimääräinen massa), ja Mw/Mn-suhde määrittää polydispersiteetin, joka on tärkeä sulan viskositeetin ja prosessoinnin kulun kannalta.
Toinen tärkeä tekijä on taktiikka, eli substituenttien järjestys ketjussa. Vinyylipolymeereissä erotetaan toisistaan isotaktiset, syndiotaktiset ja ataktiset konfiguraatiot sivuryhmien järjestyksen perusteella. Iso- ja syndiotaktiset järjestykset suosivat kiteytymistä, vaikka sivuryhmät olisivat suuria, kun taas ataktinen konfiguraatio johtaa yleensä amorfiseen rakenteeseen, kuten tyypillisen polystyreenin tapauksessa.
Polymeereille on ominaista myös siirtymälämpötilat: lasittumislämpötila (Tg) ja sulamislämpötila (Tm). Tg:n alapuolella amorfinen polymeeri käyttäytyy kuin lasi, se on jäykkä ja hauras, ja sen yläpuolella kuin kumimassa tai viskoosi neste. Puolikiteisten polymeerien osalta Tm kuvaa siirtymää kiteisestä faasista nestemäiseen tilaan. Tg:n ja Tm:n sijainti riippuu muun muassa molekyylipainosta, sivuryhmien esiintymisestä, silloitumisasteesta ja kiteisyydestä.
Tärkeimmät biomateriaaleina käytettävät polymeerit
Vaikka satoja polymeerejä voidaan saada suhteellisen helposti, lääketieteellisessä käytännössä käytetään yleisesti noin tusinaa eri polymeeriä, jotka ovat saaneet hyvän maineen biologisen yhteensopivuuden, mekaanisten ominaisuuksien ja steriloitavuuden suhteen.
Polyvinyylikloridi (PVC) on amorfinen, jäykkä polymeeri, jonka ketjussa on suuria kloridiryhmiä. Sen korkea lasittumislämpötila (noin 75–105 °C) tekee siitä puhtaassa muodossaan kovan ja hauraan. Siksi PVC:hen lisätään pehmentimiä, kuten di-2-etyyliheksyyliftalaattia (DEHP), sekä lämpövakauttajia ja prosessointivoiteluaineita. Lisäaineiden koostumus määrittää joustavuuden, vastustuskyvyn veren ja nesteiden komponenttien uuttumiselle sekä stabiilisuuden autoklaavisteriloinnissa. PVC on perusmateriaali veren ja infuusionesteiden säilytyspusseissa, infuusiolaitteissa, dialyysikomponenteissa, letkuissa, katetreissa ja lääketieteellisissä säiliöissä.
Polyeteeniä (PE) on monenlaisia: LDPE, HDPE, LLDPE, VLDPE ja UHMWPE, jonka molekyylipaino on erittäin suuri. Polymerointiedellytyksiä ja katalyyttityyppiä muuttamalla voidaan säätää ketjun haarautumisastetta, kiteisyyttä ja tiheyttä. LDPE on haaroittuneempaa ja pehmeämpää, kun taas HDPE on lineaarista ja erittäin kiteistä. Erityisen tärkeä on UHMWPE (Mw > 2·10⁶ g/mol), joka yhdistää korkean kulutuskestävyyden, hyvät mekaaniset ominaisuudet ja biologisen yhteensopivuuden, minkä ansiosta se sopii käytettäväksi nivelproteeseissa nivelkuppina tai polviproteesien nivelpintana.
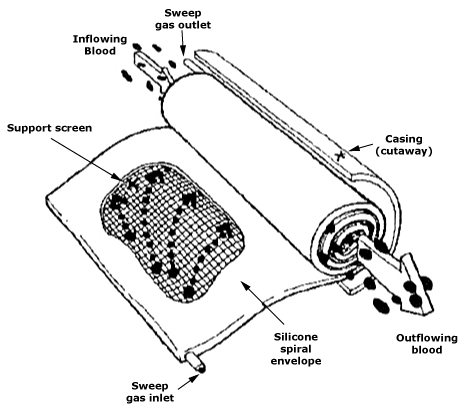
Polypropeeni (PP) on ominaisuuksiltaan samanlainen kuin polyeteeni, mutta metyyliryhmien vuoksi sen jäykkyys on hieman suurempi ja sulamispiste korkeampi. Tässä tärkeä rooli on stereospesifisellä polymeroinnilla Ziegler–Natta-katalyyttien avulla, joka tuottaa isotaktisen polymeerin. PP erottuu erinomaisesta kestävyydestään jännitysmurtumia vastaan ja korkeasta taivutuslujuudestaan, minkä vuoksi sitä käytetään muun muassa kertakäyttöisissä ruiskuissa, hapetuslaitteiden kalvoissa, kirurgisissa ompeleissa, kuitukankaissa ja joissakin verisuoniproteeseissa.
Polymetyylimetakrylaatti (PMMA) on amorfinen polymeeri, jolla on poikkeuksellinen optinen läpinäkyvyys, korkea taitekerroin ja hyvä kestävyys ilmakehän vanhenemiselle. Se on yksi biologisesti yhteensopivimmista muoveista, minkä vuoksi sitä on pitkään käytetty silmälasien ja silmänsisäisten linssien, hammasproteesien, veripumppujen komponenttien, säiliöiden, dialyysikalvojen materiaalina sekä monomeerijauhekomposiittinä nivelproteesien kiinnittämiseen käytettävänä ”luusementtinä”. Ohutristikkäiset johdannaiset, kuten PHEMA tai PAAm, muodostavat hydrogeelejä, joita käytetään muun muassa pehmeissä piilolinsseissä.
Vapaaradikaalipolymerointilla saatu polystyreeni (PS) on yleensä ataktista ja amorfista. GPPS-versiossa se on läpinäkyvää, jäykkää ja sopii hyvin ruiskupuristukseen, kun taas kumimuunnos (HIPS) lisää iskulujuutta ja halkeamiskestävyyttä. Biolääketieteessä PS:ää käytetään pääasiassa soluviljelyastioiden, pyörivien pullojen sekä diagnoosi- ja suodatussarjojen komponenttien materiaalina. Akryylinitriiliä ja butadieenia sisältävä ABS-kopolymeeri tarjoaa paremman kemiallisen kestävyyden ja mittatarkkuuden, ja sitä käytetään esimerkiksi lääkinnällisten laitteiden koteloissa ja dialyysikomponenteissa.
Polyesteriryhmässä polyeteenitereftalaatti (PET) on avainasemassa. Se on erittäin kiteinen polymeeri, jolla on korkea sulamispiste, joka on hydrofobinen ja kestää hydrolyysiä heikosti happamissa ympäristöissä. Kuitujen muodossa oleva PET tunnetaan nimellä Dacron® ja sitä on käytetty vuosia verisuoniproteeseissa, kirurgisissa ompeleissa, kirurgisissa verkoissa ja sydänläppäkomponenteissa.
Polyamidit (nylonit) muodostavat amidiryhmien välisten lukuisien vetysidosten ansiosta kuituja, joilla on erittäin hyvä mekaaninen lujuus ja jotka sopivat erinomaisesti lankojen muodostamiseen. Polyamidit ovat kuitenkin hygroskooppisia – ne imevät vettä, joka toimii pehmentäjänä ja vähentää niiden kimmokerrointa ja lujuutta, ja biologisissa olosuhteissa ne voivat hydrolysoitua proteolyyttisten entsyymien vaikutuksesta. Tästä syystä klassiset nailonit menettävät ominaisuutensa ajan myötä elimistössä ja niiltä käytetään nykyään niitä käytetään useammin ompelumateriaaleina, joiden viipymäaika kehossa on rajoitettu, kuin pysyvinä implantteina.
Fluoripolymeerit, pääasiassa PTFE (Teflon®), erottuvat ainutlaatuisista ominaisuuksistaan: erittäin korkea kiteisyys, alhainen kitkakerroin, alhainen pintaenergia ja erinomainen kemiallinen kestävyys. PTFE:n vetolujuus on suhteellisen alhainen, mutta sitä voidaan käsitellä jauhesintrauksella ja asianmukaisen käsittelyn jälkeen mikrohuokoiseksi, jolloin muodostuu ePTFE-rakenne. Tätä materiaalia käytetään laajalti verisuonimplantteina, katetrimateriaalina ja komponenteissa, jotka vaativat erinomaista liukuvuutta ja kemiallista inerttiyttä.
Kumien ja elastomeerien joukossa erityinen asema on silikonikumilla, joka koostuu metyyliryhmiä sisältävistä polysiloksaaniketjuista. Silloitetussa muodossaan se muodostaa pehmeän, joustavan materiaalin, jolla on erittäin hyvä biologinen yhteensopivuus ja jota käytetään muun muassa rintaimplanteissa, sydämentahdistimien johtimissa, dreeneissä ja erilaisissa pehmeissä proteesikomponenteissa.
Polyuretaanit voidaan suunnitella monenlaisiin muotoihin ja käyttötarkoituksiin, pehmeistä elastomeereistä jäykkään vaahtomuoviin. Lääketieteessä niitä käytetään pinnoitteina, putkina, mekaanisten laitteiden osina ja materiaaleina, joilla on parempi kulutuskestävyys kosketuksessa veren ja pehmytkudosten kanssa. Pehmeiden ja kovien segmenttien sekä kemiallisen muokattavuuden ansiosta polyuretaanit ovat yksi monipuolisimmista polymeereistä biolääketieteellisissä sovelluksissa.
Toinen ryhmä muodostuu kovista polymeereistä: polyasetaaleista (POM, Delrin®), polysulfoneista (Udel®) ja polykarbonaateista (Lexan®). Niillä on jäykät pääketjut, korkea lämmön- ja kemikaalinkestävyys sekä hyvät mekaaniset ominaisuudet. Tästä syystä niitä käytetään lääketieteellisten laitteiden rakenneosissa, pumppujen osissa, venttiileissä ja koteloissa, ja joitakin niistä testataan potentiaalisina implanttimateriaaleina.
Biohajoavat polymeerit ovat yhä tärkeämpiä, erityisesti PLA, PGA, PLGA-kopolymeerit, polydioxanonit, polyalkanolaktonit ja karbonaatit. Nämä ovat pääasiassa α-hydroksihapporyhmän polyestereitä, jotka hajoavat esterisidosten hydrolyysin kautta, jolloin syntyy aineenvaihduntatuotteita, jotka sisällytetään Krebsin sykliin (maitohappo, glykolihappo) ja lopulta erittyvät hiilidioksidina ja vetenä. PLGA:n hajoamisaikaa voidaan säätää kopolymeerin koostumuksella ja prosessiparametreillä, mikä tekee siitä erinomaisen materiaalin kudosteknologian tukirakenteisiin ja lääkeaineiden kantajiin mikropallojen muodossa. PGA toimii hyvin imeytyvänä ompeleena ja kirurgisena verkkomateriaalina, kun taas PLA voi suuremman jäykkyytensä ansiosta toimia väliaikaisena tukielementtinä osteosynteesissä.
Polymeeristen biomateriaalien sterilointi
Toisin kuin metallit ja monet keraamiset materiaalit, polymeerit ovat lämpö- ja kemikaalinkestävyydeltään rajallisia, minkä vuoksi sterilointimenetelmän valinta on ratkaiseva vaihe lääkinnällisen laitteen suunnittelussa.
Kuivalla ilmalla tapahtuva sterilointi, joka suoritetaan 160–190 °C:n lämpötiloissa, sopii vain polymeereille, joilla on erittäin korkea lämpövakaus, kuten PTFE tai silikoni. Useimmille muoveille, mukaan lukien polyeteeni ja PMMA, nämä lämpötilat ylittävät niiden pehmenemis- ja sulamispisteet, mikä johtaa muodonmuutoksiin ja hajoamiseen.
Autoklaavaus eli höyrysterilointi noin 125–130 °C:n lämpötilassa paineistettuna on lämpötilan suhteen hellävaraisempi menetelmä, mutta sillä on muita vaatimuksia: materiaalin on oltava kuuman veden ja höyryn kestävä. Hydrolyysille alttiit polymeerit, kuten tietyt polyamidit, PVC tai POM, voivat hajoaa tai halkeilla rasituksen vaikutuksesta, eivätkä ne sovellu toistuvaan höyrysterilointiin.
Etyleenioksidikaasua käytetään hyvin usein, koska sen avulla tuotteet voidaan steriloida alhaisissa lämpötiloissa. Vaikka tämä menetelmä on suhteellisen hellävarainen materiaalille, se edellyttää kaasujäämien hallintaa ja riittävän pitkää tuuletusta. Jotkut polymeerit voivat kuitenkin hajota tai värjäytyä asteittain jopa tällaisissa olosuhteissa.
Co-60-lähteitä käyttävä säteilysterilointi on erittäin tehokas, mutta ionisoiva säteily voi aiheuttaa ketjun katkeamista tai ylimääräistä verkkosidosta polymeerin rakenteesta riippuen. Polyeteenissä suuri annos johtaa kovaan, hauraaseen materiaaliin, samanaikaisen ketjun katkeamisen ja verkkosidoksen seurauksena. Polypropeeni puolestaan on altis värimuutoksille ja hauraudelle säteilyn jälkeen, ja sen ominaisuuksien heikkeneminen jatkuu vielä pitkään sterilointiin jälkeen. Siksi joissakin sovelluksissa säteilylle herkkiä lisäaineita vältetään ja koostumus valitaan haitallisten vaikutusten minimoimiseksi.

Pinnan muutokset
Koska suurin osa biologisista vuorovaikutuksista tapahtuu pinnan ensimmäisten nanometrien alueella, polymeeritekniikan keskeinen työkalu on pintakerroksen muokkaaminen, usein ilman merkittävää muutosta massan ominaisuuksiin.
Veren kanssa kosketuksiin joutuvissa laitteissa, kuten dialyysilaitteissa, verisuoniproteeseissa, keinotekoisissa venttiileissä, ekstrakorporaalisissa verenkiertojärjestelmissä, tärkein ongelma on tromboosi ja verihiutaleiden tarttuminen. Perinteinen lähestymistapa on kiinnittää hepariini ja sen analogit polymeeripintaan. Hepariini, happaman glykosaminoglykaani, estää hyytymiskaskadin, mutta sen pysyvä sitoutuminen pintaan on vaikeaa, ja hidas vapautuminen voi olla toivottavaa, mutta myös ongelmallista, koska liian nopea pinnan ”kasvaminen” plasmaproteiinikerroksella voi vähentää hepariinin saatavuutta veressä.
Toinen strategia on luoda pintoja, jotka sitovat ensisijaisesti albumiinia, joka on havaittu vähentävän verihiutaleiden tarttumista. Fibronektiinipinnoitteita käytetään, kun tavoitteena on kolonisoida pinta endoteelisoluilla, esimerkiksi yrityksissä luoda ”biologisia” verisuonipintoja synteettisille siirteille. Algiinaattipinnoitteita on testattu kerroksina, jotka parantavat verisuoniproteesien yhteensopivuutta, koska ne ovat biologisesti yhteensopivia ja niiden hajoaminen on hallittavissa.
Suuri ryhmä koostuu fysikaalis-kemiallisista muutoksista, jotka muuttavat kostuvuutta, pintaenergiaa, varausta ja topografiaa. Näitä ovat plasmakäsittelyt (happi-, typpi- ja fluoriplasma), ohuiden piin ja fluoripolymeeripinnoitteiden höyrypinnoitus, hydrogeelisiirto ja ioni-istutus. Tavoitteena voi olla kulutuksen ja korroosion kestävyyden lisääminen (esim. timanttipinnoitteet, anodisointi) tai proteiinien adsorptiota ja solujen tarttumista säätelevät ominaisuudet.
Esimerkiksi polyeteenioksidipinnoitteet (PEO) vähentävät merkittävästi proteiinien adsorptiota ja solujen adheesiota, mikä tekee niistä lupaavia ehdokkaita veren ja solujen ”antiadheesio”pinnoitteiksi. Hydrofiiliset pinnoitteet, joissa on valittu suhde polaarisia ja dispersiivisia vuorovaikutuksia, voivat puolestaan edistää ”passiivisten” proteiinien adsorptiota ja vähentää verihiutaleiden aktivaatiota.
Toinen mielenkiintoinen konsepti on suolaliuoksen perfuusio huokoisten putkien seinämien läpi. Suolaliuoksen virtaus mikrohuokosten läpi luo ohuen nestekerroksen, joka erottaa veren materiaalista, mikä voi vähentää merkittävästi solujen tarttumista ja hyytymien muodostumista. Tätä menetelmää on testattu muun muassa PE:stä, ePTFE:stä, polysulfonista ja oksidikeramiikasta valmistetuilla huokoisilla putkilla, ja tulokset ovat olleet lupaavia testeissä ja elävässä kudoksessa.
Kemogradienttipinnat
Perinteiset tutkimukset pinnan ominaisuuksien vaikutuksesta solujen tai proteiinien käyttäytymiseen edellyttävät monien eri muunnoksilla varustettujen näytteiden valmistamista, mikä on aikaa vievää ja herkkää biologiselle vaihtelulle. Ratkaisu tähän ongelmaan ovat kemogradienttipinnat, eli substraatit, joiden ominaisuudet muuttuvat asteittain yhdellä akselilla.
Polymeerien osalta on kehitetty menetelmiä, joilla polyeteenialustoille voidaan luoda kostuvuusgradientteja RF-plasman tai koronapurkauksen avulla. Polymeerilevy siirretään elektrodin alle siten, että plasman altistumisaika muuttuu asteittain. Mitä pidempi altistumisaika on, sitä suurempi on hapettuneiden polaaristen ryhmien pitoisuus pinnalla ja sitä pienempi veden kostumiskulma, mikä vastaa suurempaa hydrofiilisyyttä. Tällä tavalla on mahdollista saada pinta, jolla kostumiskulma pienenee tasaisesti, esimerkiksi 95°:sta 45°:een useiden senttimetrien pituudella.
Tämän tyyppistä substraattia käytettiin erilaisten solutyyppien, kuten kiinalaisen hamsterin munasarjasolujen (CHO-solujen), fibroblastien ja endoteelisolujen, adheesion ja proliferaation tutkimiseen. Todettiin, että suurin adheesio, leviäminen ja kasvu tapahtui keskivertoisen hydrofiilisyyden alueella, joka vastasi noin 50–55°:n kosketuskulmaa. Sekä erittäin hydrofobiset että erittäin hydrofiiliset pintapalat osoittivat heikompaa solujen kolonisaatiota.
Samanlainen kehitys havaittiin seerumin proteiinien adsorptiossa. Proteiinien, mukaan lukien fibronektiini ja vitronektiini, suurin määrä adsorboitui myös keskitason kostuvuuden alueella, mikä korreloi optimaalisen solujen adheesion ja kasvun kanssa. Näin ollen pintatekniikan näkökulmasta on olemassa kostuvuuden ”ikkuna”, jossa edistetään samanaikaisesti tarttuvien proteiinien suotuisaa adsorptiota ja solujen säilymistä.
Kemogradienttitekniikka laajennettiin funktionaalisten ryhmien gradientteihin, esimerkiksi –COOH, –CH₂OH, –CONH₂ tai –CH₂NH₂, jotka saatiin yhdistämällä koronakäsittely, vinyylimonomeerin varttaminen ja substituutioreaktiot. Tämä mahdollisti pintavarauksen, ionisoituvan ryhmän tiheyden tai polariteetin vaikutuksen tutkimisen solujen käyttäytymiseen, verihiutaleiden adheesioon ja proteiinien adsorptioon edelleen yhdellä ainoalla kokeella.
Tällä tavalla valmistetut kemiallisesti gradienttipinnat ovat tehokas työkalu pinnan ominaisuuksien ja biologisen vasteen välisen suhteen nopeaan kartoittamiseen, mikä vähentää näytteiden määrää ja pienentää solulinjojen tai viljelyolosuhteiden eroista johtuvia tulosten vaihteluita. Tulevaisuudessa vastaavia konsepteja voidaan soveltaa erotuslaitteissa, biosensoreissa ja pinnan ”kirjastoissa” biomateriaalien suurikapasiteettiseen seulontaan.
Yhteenveto – Polymeeriset biomateriaalit
Polymeeriset biomateriaalit ovat erittäin monipuolinen materiaaliryhmä, johon kuuluvat kovat, rakenteelliset kestomuovit (PE, PP, PET, POM, polysulfonit, polykarbonaatit), pehmeät elastomeerit (silikonit, polyuretaanit), hydrogeelit (PHEMA, PAAm), fluoripolymeerit (PTFE) ja yhä tärkeämmäksi tulevat biohajoavat polymeerit (PLA, PGA, PLGA, polydioxanone). Ketjurakenteen, molekyylipainon, silloitumisasteen ja kiteisyyden tarkan muokkaamisen ansiosta on mahdollista suunnitella materiaaleja, jotka sopivat täydellisesti tiettyjen sovellusten vaatimuksiin, kertakäyttöisistä infuusiosarjoista pitkäaikaisiin implantteihin ja kontrolloituihin lääkeannostelujärjestelmiin.
Sterilointi ja pinnan vuorovaikutuksen hallinta veren ja kudosten kanssa ovat edelleen keskeisiä haasteita. Tämä edellyttää paitsi sopivan polymeerin valintaa myös sterilointimenetelmän huolellista valintaa ja, mikä tärkeintä, pinnan modifiointia halutun biologisen yhteensopivuusprofiilin saavuttamiseksi. Nykyaikaiset tekniikat, kuten plasmakäsittely, hydrofiiliset ja hydrofobiset pinnoitteet, biomolekyylien immobilisointi, hydrogeelisiirteet ja kemiallisesti gradienttinen pinnan suunnittelu, avaavat tien biologisten reaktioiden tarkemmalle hallinnalle.
Tämän seurauksena polymeerit eivät ole enää vain ”muovia lääketieteessä”, vaan korkeasti kehitettyjä työkaluja, joiden koostumus, rakenne ja pinta voidaan räätälöidä tietyn kliinisen tehtävän vaatimusten mukaisesti. Tämän joustavuuden ja solujen ja materiaalien vuorovaikutuksesta kertyvän tiedon yhdistelmä tarkoittaa, että polymeeriset biomateriaalit tulevat todennäköisesti näyttelemään entistä suurempaa roolia implantologian, kudostekniikan ja lääketieteellisen teknologian tulevaisuudessa.