Biolääketieteellinen tekniikka materiaalitieteen kontekstissa
Sisällysluettelo
Biolääketieteellinen tekniikka on nykyään laaja tietämyksen ekosysteemi, jossa materiaalitiede, nestemekaniikka ja kuljetusilmiöt, mittaustekniikat ja järjestelmätekniikka kohtaavat fysiologian ja kliinisen käytännön. J.D. Bronzinon toimittaman The Biomedical Engineering Handbook -kirjan toinen painos yhdistää nämä teemat ja osoittaa, kuinka materiaalin valinta ja sen pinnan kunto vaikuttavat anturien suunnitteluun ja massavirtausominaisuuksiin, mikä puolestaan vaikuttaa keinotekoisten elinten suunnitteluun ja niiden tarkkaan valmistukseen. Tämä artikkeli auttaa meitä ymmärtämään tätä näkökulmaa biomateriaalien, biolääketieteellisen anturitekniikan, kudostekniikan ja keinotekoisten elinten alojen esimerkkien avulla, korostaen niiden merkitystä valmistustekniikalle ja laadunvalvonnalle.
Biolääketieteellisessä tekniikassa ei ole erillisiä päätöksiä – materiaaliluokan, pinnan topografian ja kemian, virtaus- ja massansiirto-olosuhteiden, laitteen arkkitehtuurin ja valmistusprosessin valinta muodostavat systeemisen kokonaisuuden, joka on suunniteltava tiettyä kliinistä käyttöaihetta ja biologista kuormitusta varten.
Materiaalitieteen paikka biolääketieteellisessä tekniikassa
Ensyklopedisesti sanottuna biomateriaali on materiaali, joka on tarkoitettu suoraan kosketukseen kudoksen kanssa lääketieteellisessä laitteessa ja suunniteltu korvaamaan turvallisesti ja tehokkaasti kehon rakenne tai toiminta. Laaja katsaus luokkiin ja suunnittelukysymyksiin on esitetty osiossa ”Biomateriaalit”, joka kattaa metallit, keraamit, polymeerit, komposiitit, biohajoavat polymeerit ja biologista alkuperää olevat materiaalit sekä endoproteesien ylläpitoon ja kiinnitykseen liittyvät kysymykset. Pelkästään lukujen rakenne johtaa perusmateriaaliluokkien valinnasta kovan ja pehmeän kudoksen integrointikysymyksiin, mikä heijastaa hyvin alan systeemistä luonnetta.
Metalleissa (Cr–Ni–Mo-teräkset, Co–Cr-seokset, titaaniseokset) korroosio- ja väsymiskestävyys sekä kyky muotoilla mikrorakenne tarkasti ovat avainasemassa. Käytännön näkökulmasta kirjassa korostetaan, että jalostuksen historia – sulatus, muovinen muodonmuutos, lämpökäsittely, puhdistus ja jopa lopullinen mikrokoneistus – korreloi vastustuskyvyn kanssa rako- ja jännityskorroosiota sekä väsymismurtumia vastaan. Tarkkuustuotannon kannalta on tärkeää, että metalleja käsittelevä luku kattaa myös ”implanttien valmistuksen”, mikä vahvistaa materiaalin suunnittelun ja valmistustekniikan erottamattomuuden lääketieteessä.
Keraamit (alumiinioksidi, zirkoniumoksidi, hiili, lasikeraamit, kalsiumfosfaattijärjestelmät) tarjoavat kovuutta, kemiallista kestävyyttä ja – bioaktiivisten lasikeraamien tapauksessa – kyvyn muodostaa kemiallisesti välittyviä sidoksia kudoksen kanssa. Samalla monografia muistuttaa meitä keramiikan hauraudesta ja hajoamisprosesseista ja kuvaa biokeraamisten valmistustekniikoita kovien kudosten korvaamisen ja kudosten integroinnin kannalta. Tässä yhteydessä geometrian, huokoisuuden ja pinnan laadun suunnittelu yhdistyy murtumiskestävyyden kannalta kriittisten virheiden tiukkaan valvontaan.
Polymeerit ovat biolääketieteen sveitsiläiset linkkuveitset, jotka vaihtelevat PVC:stä ja PE:stä PMMA:han ja PU:hun ja sisältävät biohajoavat polyesterijärjestelmät, joilla kaikilla on runsas valikoima pintamodifikaatioita biokompatibiliteetin parantamiseksi. Erityisen tärkeää on se, että tämä luokka mahdollistaa ominaisuuksien hallinnan molekyylipainon ja -jakauman, kemiallisen rakenteen ja ristisidosten avulla sekä mekaanisen estefunktion yhdistämisen bioaktiivisiin kemiallisiin motiiveihin. Sterilointi ja sen vaikutus ominaisuuksiin sekä proteiini-pinta-rajapinnan kemiallisen gradientin muokkaamiseksi käsitellään myös, koska ne vaikuttavat suoraan hemokompatibiliteettiin ja solujen kiinnittymiseen.
Komposiiteissa niiden rakenteen (hiukkaset, kuidut, huokoisuus) ansiosta on mahdollista yhdistää ristiriitaiset vaatimukset: moduloida anisotropiaa, sovittaa moduuli luuhun, parantaa tärinänvaimennusta ja saavuttaa asteittaisia ominaisuuksien muutoksia. Monografiassa järjestellään nämä kysymykset ja käsitellään ominaisuuksien rajoja, huokoisuutta ja biologista yhteensopivuutta. Tuotannon näkökulmasta faasijakauman ja virheiden hallinta matriisin ja vahvistuksen rajapinnalla on yhtä tärkeää kuin materiaali itsessään.
Biomateriaalin valintaa ja kelpoisuutta ei voida erottaa sen käsittelyyn käytetystä tekniikasta ja aiotusta kuormitusmenetelmästä. Sama materiaali, jolla on erilainen mikrorakenne, topografia ja pinnan puhtaus, osoittaa erilaisen profiilin korroosion, kulumisen, proteiinin adsorptiossa ja kudoksen integraatiossa. Siksi suunnitteluprosessissa on tarpeen hallita samanaikaisesti tilavuuden mikrorakennetta ja biofysikaalis-kemiallista rajapintaa.
Biolääketieteelliset anturit ja materiaalibiologset rajapinnat
Biolääketieteelliset anturit toimivat biologisen järjestelmän ja elektronisen järjestelmän välisenä rajapintana, muuntaen geometriset, mekaaniset, termiset, hydrauliset tai kemialliset suureet sähköisiksi signaaleiksi. Kokoelmassa korostetaan kaksijakoista luokitusta: fysikaaliset anturit, jotka mittaavat muun muassa lihasten siirtymää, verenpainetta ja nesteiden virtausta, ja kemialliset anturit, jotka tunnistavat yhdisteitä, pitoisuuksia ja aktiivisuuksia – sähkökemiallisista ja fotometrisistä monimutkaisiin analyyttisiin järjestelmiin. Optiset anturit korostetaan erittäin monipuolisena työkaluna sekä havaitsemiseen että tiedonsiirtoon kuituoptiikan ansiosta.
Biopotentiaali-elektrodit ovat olennaisia diagnostisessa ja terapeuttisessa käytössä, ja niillä on erityinen asema. Niiden toiminta riippuu paitsi elektronisesta järjestelmästä ja geometriasta, ennen kaikkea siitä, miten ne ovat vuorovaikutuksessa biologisen ympäristön kanssa. Eri sovellukset – pintakäsitellyistä Ag/AgCl-elektrodeista EMG-neuloihin ja ohutkalvomikroelektrodeihin sydämen sisäisen ja keskushermoston rekisteröintiin – vaativat erilaisia materiaalien, pinnoitteiden ja mekaanisen rakenteen kokoonpanoja sekä erilaisia kelpoisuusmenettelyjä. Hylkimisreaktiot ja vierasesineiden aiheuttamat reaktiot heikentävät signaalin vakautta ja rajapinnan kestävyyttä, joten kyse ei ole vain elektroniikasta, vaan myös kemiasta, pinnan topografiasta ja prosessin puhtaudesta.
Kirjassa esitellään myös menetelmiä anturien kiinnittämiseksi potilaisiin, aina kosketuksettomista menetelmistä ihokosketukseen, minimaalisesti invasiivisiin kehon sisäisiin antureihin ja implantoitaviin antureihin. Jokaisella näistä menetelmistä on erilaiset vaatimukset biologisen yhteensopivuuden, signaalin vakauden ja desinfiointi-/sterilointistrategioiden suhteen, mikä vaikuttaa suoraan materiaalin valintaan ja valmistustekniikkaan.
Biolääketieteellisen anturin suunnittelu on verrattavissa rajapinnan suunnitteluun, jossa sähköiset ja mekaaniset parametrit ovat yhtä tärkeitä kuin kontaktimateriaalin valinta, sen pinnoitteet, pinnan esikäsittely ja kiinnitysmenetelmä, jotka yhdessä määräävät bioreaktion ja signaalin muutoksen ajan kuluessa.
Kuljetusilmiöt ja mekaaniset rajoitukset
Kudostekniikka ja keinotekoisten elinten suunnittelu perustuvat ymmärrykseen, että massan, energian ja liikemäärän kuljetus mikrometreistä senttimetreihin säätelee kudosten ja laitteiden toimintaa. ”Kudostekniikka”-osion toimittajat korostavat kahta tekniikan teemaa: materiaalien ominaisuudet ja kehitys kahdella pituusasteikolla (molekyyli- ja solutasolla) sekä nopeusprosessien analysointi. Pintatasolla tämä koskee biomolekyylitekniikkaa (adheesio-ligandien immobilisaatio, motiivitiheyden säätö) sekä proteiiniadsorptioilmiöitä, jotka muokkaavat solujen vastausta. Mesoskaalatasolla avainasemassa ovat tarkasti määriteltyjen huokoskokoisten, läpäisevyyksien ja hajoamisten tukirakenteet ja regenerointimallit.
Lisäksi mukaan luetaan tangentiaaliset jännitteet virtauksessa sekä ravinteiden, hapen ja metaboliittien diffuusio- ja konvektioasteet. Luvut, jotka käsittelevät leikkausjännitysten vaikutusta soluihin ja massansiirron roolia kudosten toiminnassa, osoittavat, että mekaaninen ympäristö ja pitoisuusgradientit vaikuttavat morfologiaan, sytoskeletaaliseen uudelleenjärjestäytymiseen, signaalinsiirtoon, metaboliittien eritykseen ja geenien säätelyyn endoteelisoluissa – ja siten uusien kudosten kehitykseen, vakauteen ja toimintaan. Johtopäätös on yksinkertainen: ilman virtauksen ja massanvaihdon hallintaa edes parhaiten valittu materiaali ei toimi odotetulla tavalla.
Kudos- ja keinotekoisten elinten suunnittelussa virtaus- ja diffuusioparametrit ovat yhtä tärkeitä suunnittelumateriaaleja kuin polymeerit tai keraamit. Bioreaktorit, huokosrakenne ja tuotteen virtausominaisuudet on sovitettava suunnittelumuuttujiksi.
Kudostekniikka
Kudostekniikka määritellään tieteellisten periaatteiden soveltamiseksi elävien kudosten suunnitteluun, rakentamiseen, muokkaamiseen, kasvatukseen ja ylläpitoon. Bronzino et al. mukaan tämän mahdollistamiseksi on valittava solulinjan ja solulähteen valintaa, matriisin ja solujen välisen rajapinnan suunnittelua sekä kudosrakenteen hallintaa ja metabolisen ravinnon varmistamista. Tässä materiaalit kohtaavat biologian: immobilisoidut adheesioligandit, proteiiniadsorption hallinta ja tukirakenteen mikroarkkitehtuuri määräävät adheesion, proliferaation ja erilaistumisen.
Käytännössä ydin koostuu tukirakenteista, joiden ominaiskoko on 10–100 µm ja jotka määräävät kuljetuksen, solujen kolonisaation ja kudoksen kasvusuunnan. Tästä näkökulmasta biologisesti hajoavat polymeerit ovat ratkaisevan tärkeitä: biologisesti hajoavia polymeerejä käsittelevässä luvussa kuvataan sekä glykolidi- ja laktiidipohjaisia alifaattisia polyestereitä että vaihtoehtoisia polymeeriryhmiä sekä niiden hajoamisen mallintamista. Kirjoittaja korostaa kahta etua: kroonisen vierasesineiden reaktion häviäminen resorption edetessä ja kyky toimia väliaikaisina tukirakenteina kudosten uudistumiselle.
Kollageenimateriaalit, jotka ovat kudospohjaisia järjestelmiä, tarjoavat biologisesti tutun solunulkoisen matriisin arkkitehtuurin. Kollageenia käsittelevässä osassa kuvataan sekä kemiallinen rakenne että fysikaalis-kemialliset ominaisuudet sekä membraanien, huokoisten vaahtojen, geelien ja komposiittien valmistustekniikat. Lisäksi esitetään resorboituvien kollageeni-implanttien suunnittelukriteerit, mukaan lukien huokoisuus, näennäistiheys, hydrofiilisys, läpäisevyys ja in vivo -stabiilisuus. Nämä parametrit, jotka ovat myös valmistusprosessin parametreja, kuten kuivausnopeus, pakastekuivausolosuhteet, silloitusaineet ja reagenssien puhtaus, vaikuttavat suoraan biologisiin tuloksiin.
Laitteet ja bioreaktorit syntyvät materiaalien ja virtausmekaniikan vuorovaikutuksen tuloksena. Kapillaarikuitu- ja mikrokantajajärjestelmät mahdollistavat aineenvaihdunnan ylläpitämisen kudosten rekonstruointiin tarvittavalla solutiheydellä, edellyttäen että leikkausjännitykset ja pitoisuusgradientit ovat hallinnassa. Sama logiikka pätee kliinisessä mittakaavassa, kun tukirakenne kolonisoituu in situ: perfuusio, diffuusio ja isännän mekaaniset rajoitukset määräävät implantin kohtalon.
Keinotekoiset elimet ja korvauslääketiede
Osa ”Proteesit ja keinotekoiset elimet” osoittaa, että elinten toiminnan korvaaminen voi olla väliaikaista (esim. ekstrakorporaalinen verenkierto), ajoittaista ja toistettavaa (hemodialyysi, CAPD) tai pitkäaikaista implantoinnin avulla. Samalla kirjoittajat tuovat rehellisesti esiin rajoitukset: kuten mikä tahansa kone, myös keinotekoisella elimellä on rajoitettu käyttöikä, joka johtuu kitkasta, kulumisesta ja materiaalin ikääntymisestä kehon lämpimässä, kosteassa ja syövyttävässä ympäristössä. Hyötyjen tasapaino riippuu siis laitteen odotetusta käyttöiästä, sen huolto-/vaihtomenetelmästä ja potilaan tilan ennusteesta. Tämä tekninen realismi on ristiriidassa demografisen tosiasian kanssa: miljoonat potilaat ovat elossa sydämentahdistimien, venttiilien, dialyysin tai dreenijärjestelmien ansiosta.
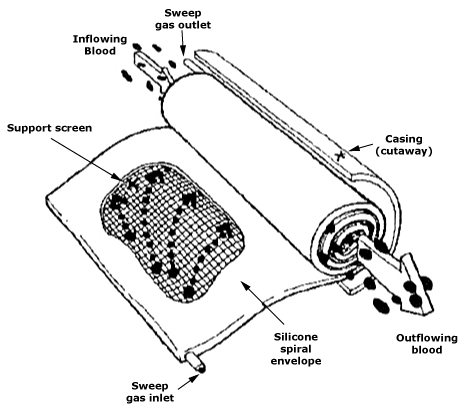
Keinotekoisen munuaisen esimerkki on erityisen opettavainen: se on laite, joka ilmentää massansiirtoa. Dialyysissä kliinisen vaikutuksen määräävät kalvot, läpäisevyyskertoimet, puhdistuma ja virtausolosuhteet sekä farmakokinetiikka ja toimenpiteen riittävyys. Jokainen näistä muuttujista liittyy materiaalitieteeseen (kemia ja kalvoarkkitehtuuri), fluidimekaniikkaan (laminaarinen/turbulentti virtaus, seinäilmiöt) ja toimintavarmuuteen. Siksi hemodiafiltraatiota, pinnan modifiointia ja uusia kalvopolymeerejä on kehitetty intensiivisesti.
Sydän- ja verisuonijärjestelmässä on ristiriita hemokompatibiliteetin ja mekaanisen kestävyyden vaatimusten välillä. Venttiilin suunnittelu edellyttää sekä hemodynamiikan arviointia (painehäviöt, energiahäviöt, takavirtaukset ja pysähtyneet alueet) että trombin kertymisen ja syklisen kestävyyden kysymysten huomioon ottamista. Verisuonisiirteissä tromboosia ja neointimaalisia hyperplasioita torjutaan muuttamalla materiaaleja ja geometriaa, jotka vaikuttavat leikkausjännityksen jakautumiseen ja virtausominaisuuksiin. Materiaalin tai pinnan topografian muutokset eivät ole pelkästään kosmeettisia, vaan ne vaikuttavat tromboosin syntyyn ja haavan paranemiseen.
Biohybridielimet puolestaan ovat laitteita, jotka sisältävät eläviä elementtejä ja yhdistävät siirtoleikkaustekniikat synteettisiin rakenteisiin, mikä lupaa luonnonmukaisempia toimintoja mutta asettaa materiaali- ja prosessivaatimuksia. Tämä on ala, jolla kudostekniikka ja massan korvaavat laitteet vetävät köyttä samaan suuntaan: kohti yhä toiminnallisempia ja kestävämpiä rajapintoja.
Tarkkuusvalmistus ja laadunvalvonta
Tuotteen valmistustapa ja materiaalit määräävät sen lopullisen tilan. Metallien osalta käsittelymenetelmät – kuten valssaus, taonta, lämpökäsittely, leikkaus sekä puhdistus ja passivointi – määräävät tekstuurin, raekoon, jäännösjännitykset ja pintakerroksen koostumuksen, jotka vaikuttavat väsymiseen, korroosioon ja solujen tarttuvuuteen. Teräksen, Co–Cr- ja Ti-seosten osalta monografiassa käsitellään paitsi ominaisuuksia myös implanttien valmistuksen erityispiirteitä, mikä siltaa materiaali- ja teknologian välisen kuilun. Tämä siirtyminen tietolomakkeesta prosessilomakkeeseen on lääketieteessä ehdottoman tärkeää.
Keraamisten materiaalien osalta synteesi- ja sintrausmenetelmien valinta, faasijakaumien ja virheidenn hallinta sekä pintakäsittely vaikuttavat murtumiskestävyyteen ja bioaktiivisiin ominaisuuksiin. Erityisesti lasikeraamisissa biokeraamissa ja hydroksiapatiiteissa koostumuksen, kiteisyyden ja huokoisuuden tarkka hallinta on suoraan yhteydessä kudosten integroitumiseen ja puristuslujuuteen. Nämä ovat alueita, joilla huokoisuuden, topografian ja virheiden mittaaminen on osa kliinistä turvallisuutta.
Polymeereissä prosessi määrää materiaalin ominaisuudet, mukaan lukien sen lämpömekaaninen historia, hehkutusympäristö, sterilointimenetelmän valinta ja stabiloivat lisäaineet, jotka kaikki vaikuttavat materiaalin hajoamiseen ja ikääntymiseen. Monografiassa kiinnitetään huomiota kahteen alueeseen: pinnan muokkaus (fysikaalinen ja kemiallinen) biokompatibiliteetin ja proteiini-/solujen adheesion parantamisen välineenä sekä kemiallisesti gradienttisten pintojen luominen, joka mahdollistaa biologisen käyttäytymisen tutkimisen ja manipuloinnin. Valmistuksen kannalta tämä tarkoittaa, että pinnan esikäsittely – kuten plasma, silanointi ja siirretyt kerrokset – tulisi olla validoitu, toistettava prosessi, ei taidetta.
Kudostekniikassa ja biohybridielinten valmistuksessa teknologia kattaa tukirakenteiden mikroarkkitehtuurien rakentamisen, menetelmät niiden sterilointiin biologista toimintaa vaarantamatta sekä bioreaktorin parametrien ja solujen kolonisaatiomenettelyjen hallinnan. Suunnitellessa immunoprotektiivisia kapseleita tai avoimia arkkitehtuureja on tarpeen hallita samanaikaisesti diffuusiota, läpäisevyyttä ja seinämän mekaniikkaa.
Materiaaliluokat
Kun edellä mainittuja periaatteita sovelletaan ortopedian kliinisiin indikaatioihin, endoproteesien laakeriparien ja kiinnitysstrategian valinta edellyttää kompromissia kulumisen, mekaanisen vakauden ja väsymisvakauden sekä biologisen integraation välillä luussa. Siksi kirjallisuudessa on kehitetty intensiivisesti huokoisia, bioaktiivisia pinnoitteita ja ultra-korkeamolekyylipainoisten polymeerien pintamodifikaatioita. Hammaslääketieteessä samanlaista logiikkaa sovelletaan implantteihin ja restaurointeihin, joissa bioinertit ja bioaktiiviset keraamit sekä titaani/zirkonium yhdistetään tarpeeseen mikro- ja nanotekstuurien suhteen, jotka edistävät osseointegraatiota ja limakalvon siirtymän biologista tiiviyttä. Sydän- ja verisuonijärjestelmässä venttiilien ja siirteiden muotoilu on suora seuraus hemodynaamisuudesta ja paikallisen geometrian ja karheuden prokoaguloivista vaikutuksista.
Munuaisalueella kalvolaitteet osoittavat, kuinka puhdistuma-, läpäisevyys- ja kokonaiskuljetusteoria muuttuu todellisessa maailmassa hoitomuodoksi, lääkeaineen farmakokinetiikaksi ja dialyysin riittävyyden arvioinniksi – ja kuinka pienet erot kalvoissa, virtauksissa ja hydrauliikassa johtavat kliinisesti merkittävään eroon. Siirtyminen kliiniseen käyttöön edellyttää fysiologisten vaatimusten kartoittamista materiaali-, geometria-, kuljetus- ja valmistusparametreihin; tiettyyn sovellukseen ja kuormitukseen sopivaa parasta materiaalia ei ole olemassa.
Monografian toimittajat osoittavat kehityksen suunnan: laitteet, jotka integroivat elävät komponentit synteettisiin rakenteisiin, kuten biohybridielimet ja informaatioproteesit, jotka tarjoavat keholle korvaavia tai moduloituja signaaleja lääketieteellisen tilan korjaamiseksi. Kyse ei ole vain ohjausalgoritmeista, vaan myös materiaaleista ja pintarajapinnoista, joiden on toimittava ennustettavasti vuosien ajan. Pehmeiden robotiikkalaitteiden ja anturien kehittäminen, joilla on korkea biologinen spesifisyys (entsyymi-substraatti, antigeeni-vasta-aine, ligandi-reseptori), edellyttää suunnittelijoilta mikro- ja nanovalmistustekniikoiden hallintaa sekä aktiivisten kerrosten stabilointia.
Biolääketieteellinen tekniikka materiaalitieteen kontekstissa – yhteenveto
The Biomedical Engineering Handbook -kirjan toinen painos tarjoaa kattavan suunnitelman biolääketieteellisestä tekniikasta, ja siinä käsitellään muun muassa biomateriaaleja, antureita ja mittauksia, kudostekniikkaa ja keinotekoisia elimiä. Kolme teemaa toistuu koko katsauksessa. Ensimmäinen on järjestelmällisyys: materiaali, pinta, kuljetus, fluidimekaniikka, elektroniikka ja valmistusprosessi ovat erottamattomia ja yhdessä määrittävät turvallisuuden ja tehokkuuden. Toinen on skaalautuvuus: molekyyleistä ja adheesiivisista ligandeista 10–100 µm:n arkkitehtuureihin ja koko laitteisiin, yhden mittakaavan parametrien on oltava yhdenmukaisia muiden vaatimusten kanssa. Kolmas on valmistettavuus: sterilointi, puhtaus, huokoisuuden ja karheuden hallinta, passivointi ja pinnan muokkaus eivät ole lisäominaisuuksia, vaan osa suunnittelua.
Tämän seurauksena biolääketieteen suunnittelija toimii kapellimestarina, joka koordinoi materiaaleja, virtauksia, signaaleja ja prosesseja halutun biologisen vasteen aikaansaamiseksi ja toiminnallisen vakauden saavuttamiseksi kokonaisuutena. Tämä monografiassa johdonmukaisesti kehitetty näkökulma on edelleen nykyinen perusta biolääketieteen, hammaslääketieteen ja tarkkuustuotannon ammattilaisille.
Kirjallisuus
Bronzino, J.D. (toim.). The Biomedical Engineering Handbook. Toinen painos. CRC Press, Boca Raton, 2000.