¿Por qué es tan importante la superficie de un implante?
En la ingeniería de biomateriales, es fácil recurrir a la intuición que deriva de la ciencia de los materiales tradicional: dado que un implante debe soportar cargas, no debe corroerse ni desgastarse en exceso y debe funcionar durante años, su éxito debería depender principalmente del material «interior». Pero esto es solo una parte de la verdad. El material a granel es, efectivamente, el responsable de la solidez, la rigidez, la elasticidad, la durabilidad y la permeabilidad. Sin embargo, desde la perspectiva del cuerpo, el primer contacto, y el más importante, no se produce con todo el bloque de material, sino con su capa exterior. Esta es la capa que entra en contacto con la sangre, las proteínas, las células y los fluidos corporales. En la práctica, esto significa que un implante puede ser mecánicamente muy bueno, pero biológicamente problemático si su superficie envía la «señal equivocada» a los tejidos.
Esta observación cambia nuestra forma de pensar sobre el diseño de implantes. En lugar de preguntarnos únicamente «¿de qué debe estar hecho el implante?», debemos considerar cómo debe ser la superficie del implante. En los biomateriales, la respuesta biológica no es un simple reflejo de la composición química de todo el componente. Más bien, es una respuesta a lo que ocurre en la interfaz entre el material y el tejido: la química de la superficie, la humectabilidad, la carga, la rugosidad, la organización y la reactividad. Por eso, el éxito de un implante no suele estar determinado por el volumen del material, sino precisamente por el límite de fase.
Este artículo se basa en Biomaterials Science: An Introduction to Materials in Medicine, ed. William R. Wagner et al., 4.ª ed., 2020. El siguiente contenido es solo una visión general del tema. A quienes les interese saber más, les recomendamos profundizar en la bibliografía.
¿Cómo reacciona el cuerpo ante la superficie de un material?
El punto de partida más importante es sencillo: el cuerpo no «ve» todo el implante de una vez. Primero, «lee» su superficie. Los autores de Biomaterials Science afirman explícitamente que, en el caso de los materiales que no liberan sustancias no deseadas, la transferencia de información del material a las proteínas, a las células y a todo el cuerpo se produce a través de la estructura superficial. El cuerpo, por lo tanto, responde a la química y organización específicas de la capa externa, más que a las propiedades promedias de todo el material. Este cambio de énfasis, aparentemente menor, tiene una enorme importancia práctica, ya que traslada la cuestión de la biocompatibilidad del nivel de «qué tipo de aleación o polímero tenemos» al nivel de «cómo se ve y se comporta su interfaz».
Es importante recordar que la superficie no es simplemente una capa delgada del material que se comporta igual que su interior. El libro destaca que la superficie es una zona de especial reactividad y difiere, casi inevitablemente, del volumen. En el caso de un material metálico real, la capa exterior puede incluir no solo óxido metálico, sino también agua adsorbida, compuestos orgánicos polares y contaminantes de hidrocarburos. En el caso de los polímeros, esta zona superficial única puede oscilar entre unos 10 y 100 nm. Esto es importante porque significa que, incluso si el material del volumen es homogéneo, su porción biológicamente activa puede ser química y estructuralmente compleja.
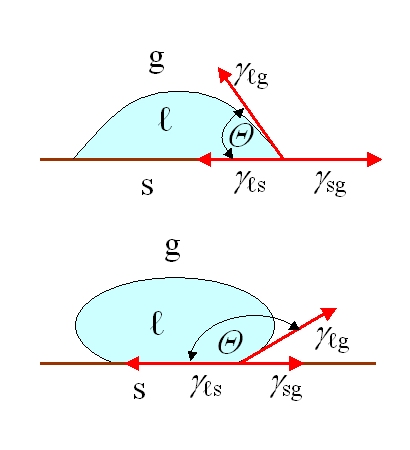
Desde una perspectiva biológica, la superficie no es meramente una cuestión de composición química. Los autores enumeran muchas características que pueden influir en las respuestas biológicas: rugosidad, patrones y topografía, humectabilidad, movilidad superficial, composición química, carga eléctrica, cristalinidad, módulo de elasticidad y heterogeneidad. Al mismo tiempo, señalan con honestidad que aún no es posible identificar una única característica universal que sea la más importante para todas las respuestas biológicas. En la práctica, se trata de una lección muy orientada a la ingeniería; no se debe basar un diseño en un único eslogan paramétrico como «aumentemos la rugosidad» o «hagamos que la superficie sea más hidrofílica», ya que la respuesta del organismo es el resultado de la interacción de varias características a la vez.
Este enfoque explica por qué dos implantes fabricados con el mismo material a granel pueden comportarse de forma biológicamente diferente. Un cambio en el procesamiento, la esterilización, el almacenamiento o el envasado basta para alterar el estado de la superficie. El libro destaca incluso cuestiones tan triviales como las huellas dactilares, los aditivos que migran del envase o los contaminantes del papel o el film. En el laboratorio, esto es un detalle pero, en la realidad, son precisamente esos detalles los que pueden llevarnos a analizar una superficie que no es la que realmente está presente en el implante utilizado clínicamente.

Cómo la superficie se traduce en biocompatibilidad
Si la superficie es el principal lenguaje de comunicación entre el implante y el cuerpo, debemos preguntarnos cómo es este diálogo. Uno de los mecanismos clave es la adsorción de proteínas. La fuente destaca que, tras la implantación de un biomaterial sintético, las proteínas adhesivas se adsorben en su superficie muy rápidamente, en cuestión de segundos. De este modo, un material que, en sí mismo, carece de motivos de reconocimiento biológico se vuelve «legible» para el cuerpo. En otras palabras, las células, a menudo, no reaccionan directamente con el material puro, sino con la capa de proteínas que se forma en su superficie poco después del contacto con el cuerpo.
Esto tiene una implicación fundamental para comprender la biocompatibilidad. La biocompatibilidad no implica simplemente la ausencia de toxicidad aguda. Implica la capacidad del material para provocar una respuesta adecuada del huésped en una aplicación específica. Esta «respuesta adecuada» puede significar una cosa para un stent, otra para un implante ortopédico y otra muy distinta para un catéter. En cada uno de estos casos, la superficie controla los eventos biológicos iniciales: qué proteínas se adsorberán, en qué configuración, qué receptores celulares se estimularán y si la señal avanzará hacia la integración tisular, la activación plaquetaria, la formación de biopelículas o una reacción a cuerpos extraños.
Un buen ejemplo es la comparación entre las proteínas de adhesión y las proteínas de pasivación. El libro describe cómo el recubrimiento previo de una superficie con fibronectina aumenta la adhesión de muchas células, mientras que la albúmina puede limitarla. Esto no es solo una curiosidad sobre el cultivo celular, sino un modelo de lo que ocurre en los implantes. La superficie no es un fondo neutro; establece las condiciones iniciales para la respuesta celular posterior. En la práctica, esto significa que dos superficies con una resistencia mecánica similar pueden dar lugar a trayectorias de cicatrización completamente diferentes, simplemente, porque establecen la primera capa de proteínas adsorbidas de manera diferente.
Las interacciones entre la superficie y los microorganismos son igualmente importantes. En el capítulo sobre las biopelículas, los autores señalan que la humectabilidad, la carga, la rugosidad y la topografía influyen en la adhesión bacteriana. La tendencia general es que una mayor rugosidad suele favorecer la adhesión bacteriana, y que las superficies hidrofóbicas facilitan la fijación bacteriana con mayor frecuencia. Al mismo tiempo, no se trata de una regla sin excepciones, ya que los sistemas extremadamente superhidrófilos o superhidrofóbicos pueden actuar como inhibidores de biopelículas a través de un mecanismo diferente. En la práctica, esto sirve como advertencia: una solución beneficiosa para la integración tisular no siempre será igualmente beneficiosa para controlar la colonización bacteriana.
A continuación, se muestra un vídeo en inglés titulado BIOE 5820 Biomaterials Protein Adsorption, que es una clase sobre la adsorción de proteínas en superficies de biomateriales.
¿Por qué modificar la superficie en lugar de todo el material?
Esta es la razón principal que justifica la modificación de la superficie. Si el material en su conjunto es el responsable de la capacidad de carga, la durabilidad y la función mecánica, mientras que la superficie es la responsable de la biointeracción, lo más lógico es conservar lo que funciona bien en el conjunto y modificar solo lo que entra en contacto con el tejido. Así es precisamente como lo expresan los autores del capítulo sobre modificaciones fisicoquímicas de la superficie: el objetivo es preservar las propiedades físicas clave del biomaterial mientras se altera solamente la capa exterior para mejorar o modular la respuesta biológica en la interfaz tejido‑dispositivo.
Este enfoque tiene varias ventajas muy prácticas. En primer lugar, no hay necesidad de abandonar un material que se conoce bien desde el punto de vista mecánico y tecnológico. El titanio, el acero, los polímeros de ingeniería o los elastómeros pueden seguir desempeñando su función estructural o funcional. En segundo lugar, la respuesta biológica puede adaptarse con mayor precisión a una aplicación determinada. Queremos una superficie diferente para un implante óseo, otra diferente para un componente que esté en contacto con la sangre y otra más para un catéter, donde la prioridad puede ser limitar la adsorción de proteínas y la adhesión de células o bacterias. En tercer lugar, la modificación de la superficie permite mejorar un dispositivo sin tener que rediseñar por completo toda la estructura. El libro incluso destaca que, para los dispositivos ya bien establecidos en la práctica clínica, esta es una forma de alterar las biointeracciones sin rediseñar el producto, reestructurar la producción ni volver a formar al personal médico para que utilice la nueva solución.
Sin embargo, hay una condición: hay que distinguir entre una modificación real de la interfaz y un cambio cosmético en la descripción. La mera declaración de que un material es «bioactivo» o «antiincrustante» tiene poco sentido si se desconoce cómo es realmente la superficie en su forma final tras el procesamiento y la esterilización. La fuente señala que la muestra analizada debe corresponderse lo más fielmente posible con el material o dispositivo en la forma utilizada para las pruebas biológicas o la implantación. Esto es importante porque la superficie expuesta al aire puede no ser la misma que el material presenta en el entorno acuoso del cuerpo.
Los tres métodos principales de modificación de superficies
El primer método consiste en alterar la superficie existente sin añadir una nueva capa separada. Los átomos, moléculas y enlaces ya presentes en la capa exterior del material pueden transformarse química o físicamente. Este grupo incluye, entre otros, el grabado, la activación química, el texturizado mecánico, la implantación de iones y ciertos tratamientos con láser. La idea es que no «adherimos» una nueva capa al implante, sino que remodelamos su propia superficie. Esto resulta ventajoso cuando es importante que haya una fuerte integración de la modificación con el sustrato, además de reducir el riesgo de delaminación y alterar propiedades como la reactividad, la humectabilidad, la resistencia a la corrosión, la dureza o la bioactividad. La fuente muestra, por ejemplo, que la implantación de iones puede mejorar la resistencia al desgaste o a la corrosión, y que el procesamiento con láser puede alterar de forma controlada la rugosidad, la cristalinidad y la química de la superficie.
El segundo enfoque consiste en aplicar una nueva capa o recubrimiento. En este caso, se coloca un material con una composición o propiedades diferentes sobre la superficie existente. Puede tratarse de una película delgada, una capa injertada, un recubrimiento polimérico o un sistema diseñado como superficie antiincrustante. Esta estrategia resulta especialmente valiosa cuando el sustrato tiene propiedades mecánicas ideales, pero es demasiado «bruto» desde el punto de vista biológico. Un buen ejemplo son las superficies resistentes a la adsorción no específica de proteínas. Su mecanismo suele basarse en contar con una fuerte capa de hidratación que actúa como barrera energética y física frente a las proteínas. En el capítulo sobre «superficies antiadherentes», los autores describen dos estrategias principales para aplicar dichos sistemas: «injerto a la superficie», donde el material se adsorbe o se une a partir de la solución, e «injerto desde la superficie», donde los cepillos poliméricos crecen desde la superficie. El primer enfoque es tecnológicamente más sencillo; el segundo alcanza más fácilmente una alta densidad de empaquetamiento, pero suele requerir una química y una preparación del sustrato más complejas.
En la práctica, esta diferencia tiene importancia desde el punto de vista de la ingeniería. Si simplemente queremos limitar de manera rápida la deposición de proteínas sobre un sustrato relativamente sencillo, la solución más simple puede ser suficiente. Sin embargo, si necesitamos una capa antiadsorción duradera, impermeable y densamente empaquetada, el simple hecho de «pegar» moléculas a la superficie puede no ser suficiente. El libro destaca claramente que la elección del método determina la densidad de empaquetamiento, el número de defectos y la durabilidad de la superficie final. Esto significa que los recubrimientos no se evalúan únicamente en función de su composición química declarada, sino de si realmente forman una interfaz homogénea y estable en condiciones de funcionamiento.
El tercer enfoque consiste en crear patrones, texturas y topografías. En este caso, el objetivo principal no es cambiar la composición química, sino alterar la geometría de lo que la célula o la proteína «ve». La fuente destaca que la topografía de la superficie influye en la adhesión, la proliferación, la migración, la diferenciación y la expresión génica de las células. Además, las células responden tanto a características a escala micro como a escala nano, y no solo a la mera presencia del material. En los estudios citados en el libro, la variación de las alturas, los tamaños y los espaciamientos de las estructuras topográficas alteró el grado de mineralización, la orientación celular, la adhesión celular y la diferenciación. Esto significa que la textura no es un mero adorno o un efecto secundario del procesamiento, sino una herramienta activa para controlar las respuestas biológicas.
Esto es particularmente evidente en los implantes óseos y dentales. El libro describe cómo una capa superficial adecuadamente rugosa o tridimensional puede acelerar las primeras etapas de la cicatrización, fomentar el depósito de fibrina, la unión de integrinas y el entrelazamiento micromecánico con el hueso. Como resultado, aumenta la resistencia al cizallamiento en la interfaz implante‑hueso y mejora la transferencia de carga. Este es un buen ejemplo de cómo la texturización no es una «mejora a ciegas», sino un intento de controlar un mecanismo interfacial específico. Sin embargo, hay que actuar con cautela, ya que la misma rugosidad que favorece la osteointegración puede, en otras aplicaciones, aumentar el riesgo de colonización bacteriana o dificultar el control de la superficie.

Errores comunes, dificultades y pistas falsas
El error más común es equiparar «mejor material» con «mejor respuesta biológica», ya que es demasiado simplista. La resistencia mecánica, la resistencia a la fatiga y la estabilidad química aún no explican lo que sucederá en la interfaz tisular. En biomateriales, se puede tener un material estructural excelente y una interfaz biológica deficiente. También se puede enfrentar al problema opuesto: una superficie con una elevada actividad biológica montada sobre un sustrato que no cumple los requisitos mecánicos. Precisamente por eso, la premisa de que el material proporciona solidez al implante, mientras que la superficie determina la respuesta del cuerpo, resulta útil en el diseño. Nos obliga a separar dos cuestiones que, a menudo, se agrupan en la ingeniería clásica.
El segundo obstáculo es la creencia de que una sola propiedad de la superficie resolverá todo el problema. En la práctica, no existe un «ajuste de biocompatibilidad» universal. Aumentar la hidrofilia puede limitar la adsorción de ciertas proteínas, pero no mejora necesariamente la integración tisular. Aumentar la rugosidad puede favorecer la respuesta de los osteoblastos, pero puede no ser beneficioso para un entorno con riesgo de infección. El propio libro señala que aún no se sabe qué parámetro es el más importante para cada respuesta biológica específica, por lo que las variables deben medirse y correlacionarse de forma independiente. Esta es una directriz metodológica muy importante: en lugar de buscar una única solución mágica, hay que construir un mapa de relaciones entre varias propiedades de la interfaz y un objetivo clínico específico.
La tercera dificultad se refiere al espesor de la modificación. Los autores del capítulo sobre modificaciones fisicoquímicas hacen hincapié en que las modificaciones deben ser lo más finas posible. Lo ideal sería alterar solo las capas moleculares más externas, del orden de unos pocos nanómetros, aunque en la práctica las capas, a veces, deben ser más gruesas para garantizar la uniformidad y la durabilidad. Un recubrimiento demasiado grueso puede alterar las propiedades mecánicas y funcionales del dispositivo, además de aumentar el riesgo de agrietamiento y delaminación. Esto es especialmente importante cuando el implante está sometido a fatiga o fricción. Una capa que parece prometedora desde el punto de vista biológico pero que se desprende mecánicamente al cabo de un tiempo no resuelve el problema; simplemente crea uno nuevo.
El cuarto error es considerar la superficie como un estado estático. La fuente demuestra que algunos materiales pueden invertir su organización superficial al pasar del aire a un entorno acuoso. Así pues, una superficie medida «en condiciones secas» puede no ser la misma superficie con la que se encuentran las proteínas y las células en el cuerpo. Esto tiene implicaciones directas para la investigación. Si el análisis de la superficie no tiene en cuenta el entorno operativo, se podría optimizar un parámetro que deja de tener el mismo valor o significado tras la implantación.
Cuando se necesita una teoría más avanzada
Un enfoque avanzado se hace necesario cuando términos intuitivos como «más lisa», «más hidrofílica» o «más rugosa» ya no son suficientes. Las superficies antiadherentes son un excelente ejemplo. Su función no se debe simplemente al hecho de que sean resbaladizas, sino a que forman una capa de hidratación estable cuya eliminación resulta energéticamente desfavorable para las proteínas adsorbentes. El libro demuestra que los materiales hidrofílicos basados en PEG (polietilenglicol) se unen al agua a través de enlaces de hidrógeno, mientras que los materiales zwitteriónicos pueden hacerlo aún con mayor fuerza a través de la hidratación inducida electrostáticamente. A este nivel, no solo hay que tener en cuenta la química funcional, sino también la densidad de empaquetamiento de la cadena, la libertad conformacional y la estabilidad del anclaje de la capa.
También se necesita una teoría avanzada cuando la superficie no solo debe ser no interferente, sino que también debe guiar activamente el comportamiento celular. En tales casos, lo que importa es la geometría a escala micro y nanométrica, la mecánica local, el tamaño, la altura y el espaciado de las características topográficas. Y, a veces, incluso el orden o el desorden del patrón. Precisamente por eso la investigación actual emplea matrices topográficas y cribados de superficies más sistemáticos. No se trata de la complejidad académica del tema, sino del hecho de que las células distinguen realmente entre escalas y patrones de características, y la respuesta biológica deja de ser una función lineal de un único parámetro.
¿Por qué es tan importante la superficie de un implante? – Resumen
En los biomateriales, el éxito de un implante, a menudo, no está determinado por el material en sí, sino por la superficie que presenta al cuerpo. La superficie es el primer punto de contacto con las proteínas, las células y los fluidos corporales y, por lo tanto, controla en gran medida la biocompatibilidad. Por esta razón, un diseño sensato del implante implica separar funciones: el volumen está destinado a garantizar las propiedades mecánicas y la durabilidad, mientras que la superficie está destinada a provocar la respuesta biológica adecuada. Esta es la base de toda la lógica de modificar la superficie sin cambiar todo el material. Se puede remodelar la capa exterior existente, aplicar un nuevo recubrimiento o diseñar un patrón y una topografía que influyan en la adsorción de proteínas, el comportamiento celular, la integración tisular o la resistencia a las incrustaciones. No obstante, hay una condición: la modificación debe ser verdaderamente interfacial, fina, duradera y adaptada a un objetivo clínico específico. Precisamente por eso, en los biomateriales, la superficie no es un detalle de acabado, sino una de las principales herramientas en el diseño de implantes.




