Sistemi di equilibrio di fase delle leghe
Indice
Nei metalli puri, il processo di trasformazione è solitamente facile da comprendere: la fusione e la solidificazione avvengono a una temperatura unica e ben definita, così come alcune trasformazioni strutturali allo stato solido. Le curve di raffreddamento mostrano quindi delle pause caratteristiche, poiché l’energia viene assorbita o rilasciata per la trasformazione stessa, piuttosto che per il cambiamento di temperatura. Nel caso delle leghe, la situazione non è più così “puntiforme”. Accade spesso che una lega inizi a solidificarsi a una temperatura ma finisca a un’altra, e durante il processo coesistono fasi con composizioni variabili.
Questo è il motivo per cui nella scienza dei materiali vengono utilizzati i diagrammi di equilibrio di fase, noti anche come diagrammi di fase. Tali diagrammi possono essere considerati come una mappa: mostrano quali fasi sono stabili in funzione della temperatura e della composizione e in quale ordine avvengono le trasformazioni durante il riscaldamento e il raffreddamento. Ciò consente di prevedere sia il corso della cristallizzazione e delle successive trasformazioni allo stato solido, sia, di conseguenza, la struttura e le proprietà della lega finita.
Concetti chiave: sistema, fase e componenti
Per leggere correttamente i diagrammi di equilibrio, è necessario comprendere il linguaggio che “parlano”. In termini termodinamici, un sistema è un frammento separato della realtà analizzato in determinate condizioni, ad esempio un campione di lega che stiamo raffreddando. Una fase indica una parte omogenea di un sistema con proprietà identiche e una composizione chimica costante, separata dalle altre fasi da un confine di fase. Una fase può essere un liquido, una soluzione solida o una fase intermetallica specifica, se ne viene formata una.
Anche i componenti, ovvero le sostanze (solitamente elementi) che costituiscono la lega e dalle quali possono formarsi le fasi, sono importanti. Nel contesto dei diagrammi binari, ci riferiamo solitamente a un sistema composto da due costituenti le cui proporzioni variano nella lega. In pratica, ciò significa che il diagramma non descrive un singolo “materiale”, ma piuttosto un’intera famiglia di leghe con composizioni diverse, e ogni cambiamento nella composizione ci sposta in un punto diverso sulla mappa delle fasi.
Regola delle fasi di Gibbs
Uno dei motivi per cui il comportamento delle leghe differisce da quello dei metalli puri è il numero di variabili che “controllano” il sistema. La regola delle fasi di Gibbs organizza la relazione tra il numero di componenti, il numero di fasi e il numero di gradi di libertà. Nella pratica metallurgica, spesso si ipotizza una pressione costante perché il suo effetto sulle transizioni di fase dei metalli è solitamente minimo rispetto all’effetto della temperatura e della composizione.
Il senso pratico è questo: se il sistema ha poco “spazio di manovra”, la transizione deve avvenire a una temperatura (da qui le interruzioni caratteristiche). Tuttavia, quando vi è variabilità nella composizione e la possibilità che coesistano più fasi, il sistema può attraversare aree in cui due fasi si verificano simultaneamente e le loro composizioni cambiano con la temperatura. Quindi, la solidificazione o le trasformazioni allo stato solido si estendono su un certo intervallo di temperatura e la struttura si forma in più fasi.
Come si crea un diagramma di equilibrio binario?
Un diagramma binario tipico mostra la relazione tra temperatura e composizione chimica. L’asse orizzontale rappresenta la composizione della lega (ad esempio, la percentuale di un componente), mentre l’asse verticale rappresenta la temperatura. Per costruire un diagramma di questo tipo, viene eseguita una serie di esperimenti su molte leghe con proporzioni diverse dei componenti e vengono registrate le temperature alle quali avvengono le trasformazioni, il più delle volte mediante metodi di analisi termica basati su curve di raffreddamento e riscaldamento.
I confini delle aree di fase sono particolarmente importanti nel grafico. Una linea chiamata liquidus separa l’area completamente liquida dall’area in cui il liquido coesiste con la fase solida. La linea solidus segna il confine al di sotto del quale la lega è completamente solida. Tra il liquidus e il solidus, di solito c’è un’area di miscela (ad esempio, fase liquida + fase solida), il che in pratica significa che durante il raffreddamento, la lega attraversa una fase in cui parte del materiale è già solido e parte rimane liquido.
È importante anche il modo in cui viene letta la composizione delle fasi a una data temperatura. Ciò avviene tracciando una linea orizzontale (isoterma) attraverso il grafico: l’intersezione con il liquidus mostra la composizione del liquido, mentre l’intersezione con il solidus mostra la composizione della fase solida in equilibrio a quella temperatura. Questo è il fondamento per dedurre cosa sta realmente accadendo nella lega durante il raffreddamento.
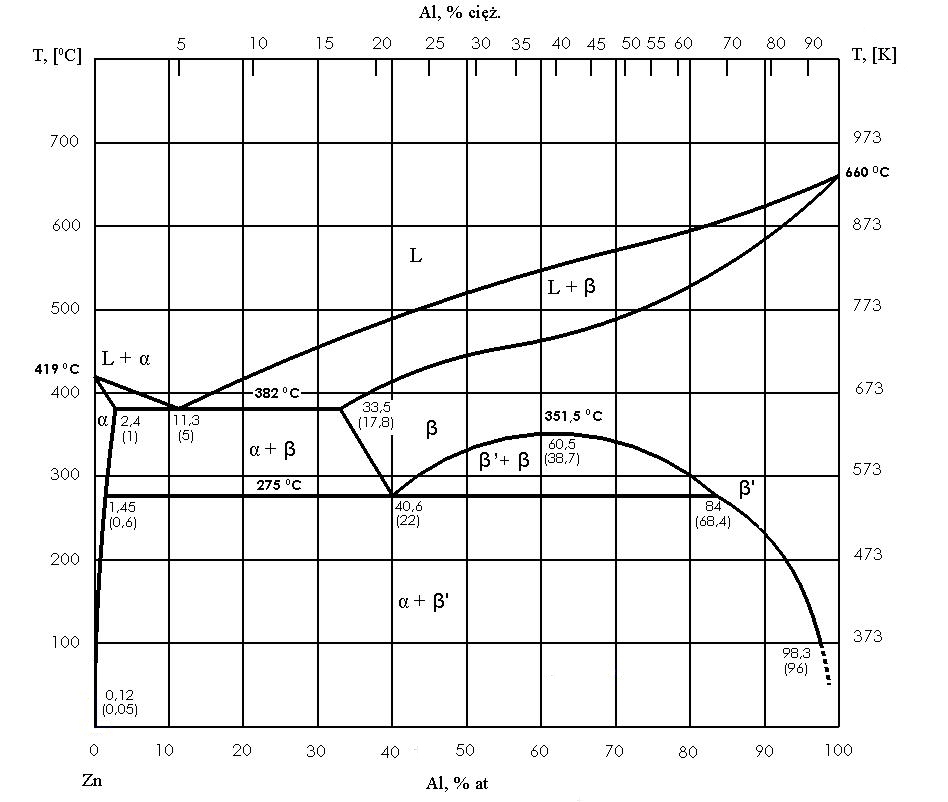
I tipi più importanti di sistemi di equilibrio
Soluzione solida continua
In alcuni sistemi, i componenti si mescolano liberamente tra loro sia allo stato liquido che allo stato solido. In questo caso, al di sotto del solidus, c’è una sola fase: una soluzione solida con una composizione che dipende dalla posizione sull’asse della composizione. Durante il raffreddamento, la lega inizia a solidificarsi al liquidus quando compaiono i primi cristalli della soluzione solida e termina al solidus quando scompare l’ultima parte di liquido. Questo è un classico esempio di solidificazione in un intervallo di temperatura, senza una singola interruzione.
È bene ricordare che nell’area “soluzione liquida + solida”, le composizioni di entrambe le fasi sono diverse e cambiano con la temperatura. La lettura dell’isoterma ci permette di determinare quale parte della lega è già allo stato solido in un dato momento e quale parte è ancora liquida.
Eutettico
Un sistema eutettico è molto caratteristico quando i componenti si mescolano in uno stato liquido ma si dissolvono male, o per nulla, in uno stato solido. In questo caso, esiste una composizione eutettica e una temperatura alla quale un liquido omogeneo si trasforma in due fasi solide contemporaneamente. Tale trasformazione è isotermica, quindi si verifica una chiara pausa sulla curva di raffreddamento, come nel caso del metallo puro, ma il meccanismo è diverso: invece di una singola fase solida, si forma una miscela fine di due fasi, solitamente con una morfologia specifica e regolare.
Le leghe con una composizione diversa da quella eutettica formano una struttura mista. Se la lega è ipereutettica, i cristalli primari di una fase vengono prima separati e solo successivamente il resto del liquido si solidifica come eutettico. Se la lega è ipereutettica, compaiono prima i cristalli primari della seconda fase, seguiti da quelli eutettici. Di conseguenza, la microstruttura dipende dalla composizione: l’eutettico può dominare, i cristalli primari possono dominare, oppure entrambi i componenti possono avere proporzioni simili.
Eutettico con solubilità limitata allo stato solido
In pratica, spesso si verifica una situazione intermedia: i componenti si mescolano bene allo stato liquido, ma allo stato solido formano soluzioni solide solo in misura limitata. Quindi, invece di fasi “pure”, si formano soluzioni solide di confine, comunemente indicate come α e β, e l’eutettico diventa una miscela di queste due soluzioni con composizioni sature alla temperatura eutettica.
Questo è molto importante perché, con l’ulteriore raffreddamento, la solubilità allo stato solido spesso diminuisce, quindi le soluzioni α e β possono diventare supersature. Di conseguenza, dopo il completamento della solidificazione possono verificarsi separazioni secondarie e un’ulteriore “maturazione” della struttura. Il diagramma non è quindi solo una descrizione della cristallizzazione, ma anche una guida ai cambiamenti nello stato solido che influenzano le proprietà del materiale.
Peritectica
Nei sistemi peritectici avviene una trasformazione in cui il liquido reagisce con la fase solida esistente per formare una nuova fase solida. Ciò avviene a una temperatura specifica perché al momento della reazione coesistono tre fasi. Il meccanismo peritectico è di importanza pratica perché la nuova fase spesso cresce sui cristalli della fase originale, formando uno strato che ostacola l’ulteriore diffusione dei componenti. Ciò può causare una deviazione del corso effettivo della trasformazione dall’equilibrio ideale, specialmente con un raffreddamento più rapido.
Da un punto di vista tecnologico, la peritectica può essere fonte di eterogeneità e strutture che dipendono non solo dal diagramma di equilibrio stesso, ma anche dalla cinetica, ovvero dalla velocità dei processi di diffusione; pertanto, nell’interpretare i diagrammi, è importante ricordare che il diagramma descrive l’equilibrio e non sempre lo stato effettivo “al volo”, senza il tempo necessario affinché la composizione si equalizzi.
Solubilità limitata nei liquidi
A volte, anche allo stato liquido, il sistema non è completamente omogeneo. Può accadere che, entro un certo intervallo di temperatura, il liquido si separi in due liquidi con composizioni diverse, favorendo la segregazione e la formazione di aree con proprietà diverse. In un sistema di questo tipo è possibile una trasformazione monotettica, in cui un liquido si trasforma in un altro liquido e in una fase solida.
Dal punto di vista della tecnologia di fusione, questo è importante perché la separazione dei liquidi può portare a un’eterogeneità indesiderata della lega. In pratica, questo fenomeno viene spesso contrastato mediante un adeguato controllo del processo, compresa la selezione della velocità di raffreddamento o del metodo di miscelazione del metallo liquido, al fine di limitare il tempo necessario allo sviluppo della segregazione.
Composti chimici e fasi intermetalliche
In molti sistemi si formano composti chimici e fasi intermetalliche. Se un composto ha una composizione stechiometrica costante, esso appare sul diagramma come una posizione caratteristica corrispondente a questa proporzione di componenti. Tale composto può fondere in modo “simile al metallo puro” quando si trasforma in un liquido della stessa composizione, oppure può formarsi e scomparire in trasformazioni peritectiche quando il processo procede attraverso la reazione con il liquido.
Le fasi intermetalliche sono spesso dure e fragili e la loro presenza può alterare in modo significativo le proprietà della lega. Per questo motivo, i diagrammi di fase sono particolarmente importanti nella progettazione delle leghe, poiché consentono di prevedere se, entro un determinato intervallo di composizione e temperatura, apparirà una fase che comprometterà la plasticità o, al contrario, rafforzerà la lega attraverso precipitati fini.
Trasformazioni allo stato solido: eutettoide e perittetoide
I diagrammi di equilibrio non terminano con la solidificazione. In molte leghe, le trasformazioni che avvengono dopo la transizione allo stato solido sono importanti, specialmente quando la solubilità nelle soluzioni solide cambia con la temperatura o quando uno dei componenti presenta polimorfismo. Di particolare importanza è la trasformazione eutettoide, che è equivalente all’eutettica ma avviene interamente allo stato solido: una soluzione solida si scompone in due fasi solide a temperatura costante. Questa trasformazione porta spesso a una struttura fine e regolare e può alterare in modo significativo le proprietà meccaniche.
Esiste anche una trasformazione peritectica, analoga alla peritectica, ma senza il coinvolgimento di liquidi: due fasi solide reagiscono per formare una terza fase solida. In pratica, le trasformazioni allo stato solido possono essere cruciali, poiché possono determinare la durezza, la resistenza all’urto o la resistenza allo scorrimento, anche se il processo di solidificazione è avvenuto correttamente.
Significato pratico
La conclusione più importante che si può trarre dall’analisi dei diagrammi è che le proprietà delle leghe derivano principalmente dalla loro struttura e non solo dagli elementi che contengono. Le leghe monofasiche sono solitamente più omogenee e le loro proprietà cambiano spesso in modo più graduale con la composizione. Nelle leghe multifase, la situazione è più complessa perché il comportamento del materiale è determinato dal tipo di fasi, dalla loro proporzione, distribuzione, dimensione dei grani e morfologia (ad esempio, la forma degli eutettici o la natura dei precipitati).
Pertanto, un diagramma di fase è uno strumento che aiuta a collegare le condizioni di processo al risultato. Se si conoscono le temperature e le composizioni alle quali si verificano determinate fasi, è possibile selezionare consapevolmente la composizione della lega e le condizioni di raffreddamento e trattamento termico. In pratica, ciò significa che è possibile prevedere se la lega tenderà a segregarsi, se appariranno fasi intermetalliche fragili, se i precipitati potranno essere utilizzati per il rinforzo o se la struttura sarà stabile nelle condizioni operative.
Sistemi di equilibrio di fase delle leghe – sintesi
I sistemi di equilibrio di fase sono uno strumento che organizza il comportamento delle leghe in modo sistematico e prevedibile. Possono essere utilizzati per determinare quali fasi saranno stabili, quando inizierà e finirà la solidificazione, se si verificheranno fenomeni eutettici o peritetici e quali trasformazioni potranno avvenire allo stato solido. In pratica, ciò significa la capacità di controllare la microstruttura e quindi le proprietà meccaniche e fisiche del materiale. La capacità di leggere i diagrammi di fase è quindi una delle competenze più importanti nella scienza dei materiali e nella metallurgia, poiché consente di tradurre la teoria delle trasformazioni di fase in decisioni ingegneristiche concrete.