Porque é tão importante a superfície de um implante?
Na engenharia de biomateriais, é fácil recorrer à intuição derivada da ciência dos materiais tradicional: uma vez que um implante deve suportar cargas, não sofrer corrosão, não desgastar-se excessivamente e funcionar durante anos, o seu sucesso deveria depender principalmente do “interior” do material. Isto é apenas parte da verdade. O material em si é, de facto, responsável pela resistência, rigidez, elasticidade, durabilidade e permeabilidade. No entanto, do ponto de vista do corpo, o primeiro e mais importante contacto não ocorre com o bloco inteiro de material, mas com a sua camada exterior. É esta camada que entra em contacto com o sangue, as proteínas, as células e os fluidos corporais. Na prática, isto significa que um implante pode ser mecanicamente muito bom, mas biologicamente problemático, se a sua superfície enviar o “sinal errado” aos tecidos.
Esta observação altera a forma como pensamos sobre o design de implantes. Em vez de perguntarmos apenas “de que deve ser feito o implante?”, devemos considerar como deve ser a superfície do implante. Nos biomateriais, a resposta biológica não é um simples reflexo da composição química de todo o componente. É, antes, uma resposta ao que acontece na interface material-tecido: a química da superfície, a molhabilidade, a carga, a rugosidade, a organização e a reatividade. É por isso que o sucesso de um implante é tantas vezes determinado não pelo volume do material, mas precisamente na fronteira de fases.
Este artigo baseia-se no livro Biomaterials Science: An Introduction to Materials in Medicine, ed. William R. Wagner et al., 4.ª ed., 2020. O conteúdo que se segue é apenas uma visão geral do tema. Para quem estiver interessado no assunto, recomendamos a consulta da literatura especializada.
Como reage o corpo à superfície de um material?
O ponto de partida mais importante é simples: o corpo não “vê” o implante na sua totalidade de uma só vez. Primeiro, “lê” a sua superfície. Os autores de Biomaterials Science afirmam explicitamente que, no caso de materiais que não libertam substâncias indesejáveis, a transferência de informação do material para as proteínas, as células e todo o corpo ocorre através da estrutura da superfície. O corpo, portanto, responde à química e à organização específicas da camada externa, em vez de responder às propriedades médias de todo o material. Esta mudança de ênfase, aparentemente menor, tem um enorme significado prático, pois desloca a questão da biocompatibilidade do nível de “que tipo de liga ou polímero temos” para o nível de “como a sua interface se apresenta e se comporta”.
É importante lembrar que a superfície não é simplesmente uma camada fina do material que se comporta da mesma forma que o seu interior. O livro salienta que a superfície é uma zona de reatividade particular e difere quase inevitavelmente da massa. No caso de um material metálico real, a camada exterior pode incluir não só óxido metálico, mas também água adsorvida, compostos orgânicos polares e contaminantes de hidrocarbonetos. No caso dos polímeros, a zona superficial específica pode variar entre cerca de 10 nm e 100 nm. Este aspeto é importante porque significa que, mesmo que o material no seu conjunto seja homogéneo, a sua porção biologicamente ativa pode ser química e estruturalmente complexa.
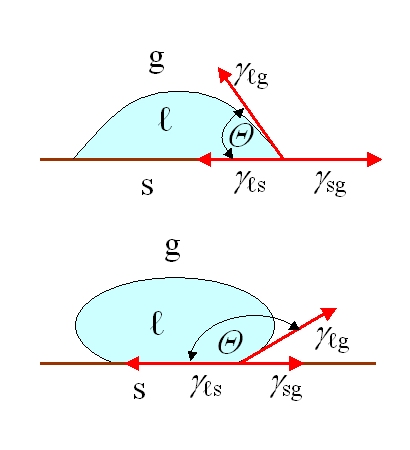
De uma perspetiva biológica, a superfície não é meramente uma questão de composição química. Os autores enumeram muitas características que podem influenciar as respostas biológicas: rugosidade, padrões e topografia, molhabilidade, mobilidade superficial, composição química, carga elétrica, cristalinidade, módulo de elasticidade e heterogeneidade. Ao mesmo tempo, observam honestamente que ainda não é possível identificar uma única característica universal que seja a mais importante para todas as respostas biológicas. Na prática, esta é uma lição muito orientada para a engenharia; não se deve basear um projeto num único lema paramétrico, como “vamos aumentar a rugosidade” ou “vamos tornar a superfície mais hidrofílica”, porque a resposta do corpo é o resultado da interação de várias características ao mesmo tempo.
Esta abordagem explica por que razão dois implantes feitos do mesmo material em massa podem comportar-se biologicamente de forma diferente. Uma alteração no processamento, esterilização, armazenamento ou embalagem é suficiente para alterar o estado da superfície. O livro destaca até mesmo questões tão banais como impressões digitais, aditivos que migram da embalagem ou contaminantes provenientes de papel ou película. Em laboratório, isto é um pormenor, mas, na realidade, são precisamente esses pormenores que podem levar-nos a testar uma superfície que não é a que está realmente presente no implante utilizado clinicamente.

Como a superfície se traduz em biocompatibilidade
Se a superfície é a principal forma de comunicação entre o implante e o corpo, temos de nos perguntar como é feito esse diálogo. Um dos mecanismos-chave é a adsorção de proteínas. A fonte salienta que, após a implantação de um biomaterial sintético, proteínas adesivas adsorvem na sua superfície muito rapidamente, em segundos. Desta forma, um material que, por si só, carece de motivos de reconhecimento biológico torna-se “legível” para o corpo. Por outras palavras, as células muitas vezes não reagem diretamente ao material puro, mas à camada de proteínas que se forma na sua superfície pouco depois do contacto com o corpo.
Isto tem uma implicação fundamental para a compreensão da biocompatibilidade. A biocompatibilidade não significa apenas a ausência de toxicidade aguda. Significa a capacidade do material de provocar uma resposta adequada do hospedeiro numa aplicação específica. Esta “resposta adequada” pode significar uma coisa para um stent, outra para um implante ortopédico e ainda outra para um cateter. Em cada um destes casos, a superfície controla os eventos biológicos iniciais: quais as proteínas que se irão adsorver, em que configuração, quais os recetores celulares que serão estimulados e se o sinal irá prosseguir para a integração tecidular, ativação plaquetária, formação de biofilme ou uma reação a corpo estranho.
Um bom exemplo é a comparação entre proteínas de adesão e proteínas de passivação. O livro descreve como o pré-revestimento de uma superfície com fibronectina aumenta a adesão de muitas células, enquanto a albumina pode limitá-la. Isto não é apenas uma curiosidade da cultura celular, mas um modelo do que acontece nos implantes. A superfície não é um pano de fundo neutro. Ela define as condições iniciais para a resposta celular subsequente. Na prática, isto significa que duas superfícies com resistência mecânica semelhante podem originar trajetórias de cicatrização completamente diferentes simplesmente porque estabelecem a primeira camada de proteínas adsorvidas de forma diferente.
Igualmente importantes são as interações entre a superfície e os microrganismos. No capítulo sobre biofilmes, os autores observam que a molhabilidade, a carga, a rugosidade e a topografia influenciam a adesão bacteriana. A tendência geral é que uma maior rugosidade promova frequentemente a adesão bacteriana, e que as superfícies hidrofóbicas facilitem com maior frequência a fixação bacteriana. Ao mesmo tempo, esta não é uma regra sem exceções, uma vez que sistemas extremamente super-hidrofílicos ou super-hidrofóbicos podem atuar como inibidores de biofilmes através de um mecanismo diferente. Na prática, isto serve como uma nota de cautela: uma solução benéfica para a integração tecidular nem sempre será igualmente benéfica para controlar a colonização bacteriana.
Segue-se um vídeo em inglês intitulado BIOE 5820 Biomaterials Protein Adsorption (BIOE 5820 Adsorção de proteínas em biomateriais), que é uma palestra sobre a adsorção de proteínas em superfícies de biomateriais.
Porquê modificar a superfície em vez de todo o material
Esta é a principal razão por trás da modificação da superfície. Se o material em massa é responsável pela capacidade de suporte de carga, durabilidade e função mecânica, enquanto a superfície é responsável pela biointeração, faz todo o sentido preservar o que funciona bem no material em massa e modificar apenas o que entra em contacto com o tecido. É precisamente assim que os autores do capítulo sobre modificações físico-químicas da superfície explicam a situação: o objetivo é preservar as propriedades físicas essenciais do biomaterial, alterando apenas a camada exterior para melhorar ou modular a resposta biológica na interface tecido-dispositivo.
Esta abordagem tem várias vantagens muito práticas. Em primeiro lugar, não há necessidade de abandonar um material que é bem compreendido do ponto de vista mecânico e tecnológico. O titânio, o aço, os polímeros de engenharia ou os elastómeros podem continuar a desempenhar o seu papel estrutural ou funcional. Em segundo lugar, a resposta biológica pode ser adaptada com maior precisão a uma determinada aplicação. Queremos uma superfície para um implante ósseo, outra diferente para um componente em contacto com o sangue e ainda outra para um cateter, onde a prioridade pode ser limitar a adsorção de proteínas e a adesão de células ou bactérias. Em terceiro lugar, a modificação da superfície permite melhorar um dispositivo sem ter de redesenhar completamente toda a estrutura. O livro salienta mesmo que, para dispositivos já bem estabelecidos na prática clínica, esta é uma forma de alterar as biointerações sem redesenhar o produto, reequipar a produção ou dar nova formação ao pessoal médico para utilizar a nova solução.
Existe, no entanto, uma condição: é necessário distinguir entre uma modificação real da interface e uma alteração cosmética na descrição. A mera declaração de que um material é “bioativo” ou “antifouling” significa pouco se não se souber como é a superfície real na sua forma final após o processamento e a esterilização. A fonte observa que a amostra analisada deve corresponder o mais fielmente possível ao material ou dispositivo na forma utilizada para testes biológicos ou implantação. Este aspeto é importante porque a superfície exposta ao ar pode não ser a mesma superfície que o material apresenta no ambiente aquoso do corpo.
Três métodos principais de modificação de superfície
O primeiro método envolve alterar a superfície existente sem adicionar uma nova camada separada. Átomos, moléculas e ligações já presentes na camada exterior do material podem ser transformados química ou fisicamente. Este grupo inclui, entre outros, gravação, ativação química, rugosidade mecânica, implantação de iões e certos tratamentos a laser. A questão é que não “fixamos” uma nova camada ao implante, mas sim remodelamos a sua própria superfície. Isto é vantajoso quando é importante uma forte integração da modificação com o substrato, bem como para reduzir o risco de delaminação e alterar propriedades como a reatividade, a molhabilidade, a resistência à corrosão, a dureza ou a bioatividade. A fonte mostra, por exemplo, que a implantação de iões pode melhorar a resistência ao desgaste ou à corrosão, e que o processamento a laser pode alterar de forma controlada a rugosidade, a cristalinidade e a composição química da superfície.
A segunda abordagem envolve a aplicação de uma nova camada ou revestimento. Neste caso, um material com composição ou propriedades diferentes é colocado sobre a superfície existente. Pode tratar-se de uma película fina, uma camada enxertada, um revestimento polimérico ou um sistema concebido como superfície antifouling. Esta estratégia é particularmente valiosa quando o substrato possui propriedades mecânicas ideais, mas é demasiado “bruto” do ponto de vista biológico. Um bom exemplo são as superfícies resistentes à adsorção não específica de proteínas. O seu mecanismo depende geralmente de uma forte camada de hidratação, que atua como uma barreira energética e física às proteínas. No capítulo sobre superfícies antifouling, os autores descrevem duas estratégias principais para a aplicação de tais sistemas: “enxerto na superfície”, em que o material é adsorvido ou se liga a partir da solução, e “enxerto a partir da superfície”, em que escovas poliméricas crescem a partir da superfície. A primeira abordagem é tecnologicamente mais simples; a segunda alcança mais facilmente uma alta densidade de empacotamento, mas geralmente requer química e preparação do substrato mais complexas.
Na prática, esta diferença tem significado em termos de engenharia. Se quisermos apenas limitar rapidamente a deposição de proteínas num substrato relativamente simples, a solução mais simples pode ser suficiente. No entanto, se precisarmos de uma camada anti-adsorção durável, impermeável e densamente empacotada, “colar” simplesmente as moléculas à superfície pode não ser suficiente. O livro enfatiza claramente que a escolha do método determina a densidade de empacotamento, o número de defeitos e a durabilidade da superfície final. Isto significa que os revestimentos não são avaliados apenas com base na sua composição química declarada, mas sim na possibilidade de formar efetivamente uma interface homogénea e estável nas condições de funcionamento.
A terceira abordagem envolve a criação de padrões, texturas e topografias. Aqui, o foco principal não está em alterar a composição química, mas em alterar a geometria daquilo que a célula ou a proteína “vê”. A fonte salienta que a topografia da superfície influencia a adesão, a proliferação, a migração, a diferenciação e a expressão genética das células. As células respondem tanto a características em microescala como em nanoescala, e não apenas à mera presença do material. Nos estudos citados no livro, alturas, tamanhos e espaçamentos variáveis das estruturas topográficas alteraram o grau de mineralização, a orientação celular, a adesão celular e a diferenciação. Isto significa que a textura não é um mero ornamento ou um efeito secundário do processamento, mas uma ferramenta ativa para controlar respostas biológicas.
Isto é particularmente evidente em implantes ósseos e dentários. O livro descreve como uma camada superficial adequadamente rugosa ou tridimensional pode acelerar as fases iniciais da cicatrização, promover a deposição de fibrina, a ligação de integrinas e o entrelaçamento micromecânico com o osso. Como resultado, a resistência ao cisalhamento na interface implante-osso aumenta e a transferência de carga melhora. Este é um bom exemplo de como a texturização não é uma “melhoria cega”, mas uma tentativa de controlar um mecanismo interfacial específico. No entanto, é necessário ter cuidado, pois a mesma rugosidade que auxilia a osseointegração pode, noutra aplicação, aumentar o risco de colonização bacteriana ou dificultar o controlo da superfície.

Erros comuns, armadilhas e pistas falsas
O erro mais comum é equiparar “melhor material” a “melhor resposta biológica”. É demasiado simplista. A resistência, a resistência à fadiga e a estabilidade química ainda não explicam o que irá acontecer na interface tecidular. Nos biomateriais, é possível ter um excelente material estrutural e uma interface biológica deficiente. Também se pode enfrentar o problema oposto: uma superfície altamente ativa do ponto de vista biológico montada num substrato que não cumpre os requisitos mecânicos. É precisamente por isso que a premissa de que o material confere resistência ao implante, enquanto a superfície determina a resposta do corpo, é útil no design. Obriga-nos a separar duas questões que são frequentemente agrupadas na engenharia clássica.
A segunda armadilha é a convicção de que uma única propriedade da superfície resolverá todo o problema. Na prática, não existe uma “configuração de biocompatibilidade” universal. Aumentar a hidrofilicidade pode limitar a adsorção de certas proteínas, mas não melhora necessariamente a integração tecidual. Aumentar a rugosidade pode promover a resposta dos osteoblastos, mas pode não ser benéfico para um ambiente em risco de infeção. O próprio livro observa que ainda não se sabe qual o parâmetro mais importante para cada resposta biológica específica, pelo que as variáveis devem ser medidas e correlacionadas de forma independente. Esta é uma orientação metodológica muito importante: em vez de procurar um único número mágico, deve-se construir um mapa de relações entre várias propriedades da interface e um objetivo clínico específico.
A terceira armadilha diz respeito à espessura da modificação. Os autores do capítulo sobre modificações físico-químicas enfatizam que as modificações devem ser tão finas quanto possível. Idealmente, bastaria alterar apenas as poucas camadas moleculares mais externas – da ordem de alguns nanómetros –, embora, na prática, as camadas tenham por vezes de ser mais espessas para garantir uniformidade e durabilidade. Um revestimento demasiado espesso pode alterar as propriedades mecânicas e funcionais do dispositivo, bem como aumentar o risco de fissuras e delaminação. Isto é particularmente importante quando o implante está sujeito a fadiga ou atrito. Uma camada que parece promissora do ponto de vista biológico, mas que se descola mecanicamente após algum tempo, não resolve o problema; apenas cria um novo.
O quarto equívoco é tratar a superfície como um estado estático. A fonte demonstra que alguns materiais podem reverter a sua organização superficial na transição do ar para um ambiente aquoso. Uma superfície medida “em condições secas” pode não ser a mesma superfície que as proteínas e as células encontram no corpo. Isto tem implicações diretas para a investigação. Se a análise da superfície não tiver em conta o ambiente operacional, pode-se otimizar um parâmetro que deixa de ter o mesmo valor ou significado após a implantação.
Quando é necessária uma teoria mais avançada
Uma abordagem avançada torna-se necessária quando termos intuitivos como “mais lisa”, “mais hidrofílica” ou “mais rugosa” já não são suficientes. As superfícies antifouling são um exemplo. A sua função não resulta simplesmente do facto de serem escorregadias, mas sim de formarem uma camada de hidratação estável, cuja remoção é energeticamente desfavorável para a adsorção de proteínas. O livro demonstra que os materiais hidrofílicos à base de PEG ligam a água através de ligações de hidrogénio, enquanto os materiais zwitteriónicos podem fazê-lo de forma ainda mais forte através da hidratação induzida eletrostaticamente. A este nível, é necessário considerar não só a química funcional, mas também a densidade de empacotamento da cadeia, a liberdade conformacional e a estabilidade da fixação da camada.
É também necessária uma teoria avançada quando a superfície não se destina apenas a não interferir, mas a orientar ativamente o comportamento celular. Nestes casos, o que importa é a geometria à escala micro e nano, a mecânica local, o tamanho, a altura e o espaçamento das características topográficas e, por vezes, até a ordem ou desordem do padrão. É precisamente por isso que a investigação atual recorre a matrizes topográficas e a triagens de superfícies mais sistemáticas. Não se trata da complexidade académica do assunto, mas do facto de as células distinguirem verdadeiramente entre escalas e padrões de características, e de a resposta biológica deixar de ser uma função linear de um único parâmetro.
Porque é tão importante a superfície de um implante? – resumo
Nos biomateriais, o sucesso de um implante costuma ser determinado não pelo material em si, mas pela superfície que este apresenta ao corpo. É a superfície que constitui o primeiro ponto de contacto com proteínas, células e fluidos corporais, controlando assim, em grande medida, a biocompatibilidade. Por esta razão, um design sensato do implante envolve a separação de funções: o volume destina-se a garantir propriedades mecânicas e durabilidade, enquanto a superfície se destina a suscitar a resposta biológica adequada. Esta é a base de toda a lógica de modificar a superfície sem alterar todo o material. É possível remodelar a camada exterior existente, aplicar um novo revestimento ou conceber um padrão e uma topografia que influenciem a adsorção de proteínas, o comportamento celular, a integração tecidular ou a resistência ao fouling. Há uma condição: a modificação deve ser verdadeiramente interfacial, fina, duradoura e adaptada a um objetivo clínico específico. É precisamente por isso que, nos biomateriais, a superfície não é um detalhe de acabamento, mas uma das principais ferramentas na conceção de implantes.




