Biomateriais na medicina e na odontologia
Índice
Os biomateriais são a espinha dorsal da medicina e odontologia reconstrutivas modernas. As suas aplicações vão desde válvulas cardíacas e endopróteses articulares até implantes intraósseos, sensores, elétrodos e sistemas de administração de medicamentos. Este artigo tem como objetivo fornecer uma visão geral concisa, mas abrangente, da sua definição, requisitos de biocompatibilidade, classes primárias, mecanismos de interação com o corpo, testes e princípios de degradação, bem como destacar os principais aspetos da engenharia de superfícies e fabricação de precisão que determinam o sucesso clínico de um produto. O artigo baseia-se na monografia clássica «Biomaterials Science: An Introduction to Materials in Medicine», editada por B.D. Ratner et al. (Academic Press).
Os biomateriais devem ser sempre analisados no contexto da sua aplicação clínica, dentro de um ambiente biológico específico e após passarem por processos reais de fabrico e esterilização, pois essas etapas definem as suas propriedades funcionais e segurança.

O que é um biomaterial e o que é biocompatibilidade?
Na terminologia adotada na literatura, um biomaterial é um material inanimado destinado a interagir com um sistema biológico num dispositivo médico. A sua aceitabilidade clínica depende da biocompatibilidade, ou seja, a capacidade de provocar uma resposta adequada e deliberadamente desejada do hospedeiro numa determinada aplicação, ou seja, uma resposta que permita o efeito terapêutico pretendido e não gere riscos inaceitáveis. Essas definições, estabelecidas nos trabalhos de D.F. Williams e nos capítulos introdutórios de monografias, entre outros, tornaram-se a pedra angular do desenvolvimento interdisciplinar do campo.
A biocompatibilidade é uma relação material-dispositivo-paciente-aplicação; o mesmo material pode ser biocompatível num produto e problemático noutro.
Historicamente, os biomateriais incluíram tanto metais usados em próteses (por exemplo, ouro em odontologia) quanto materiais como vidro ou madeira em próteses externas. O entendimento atual da disciplina desenvolveu-se em paralelo com a cristalização da comunidade científica, simpósios e o estabelecimento de sociedades científicas; ao mesmo tempo, a estrutura da literatura profissional e das normas tomou forma.
A sistemática dos materiais utilizados na medicina e na odontologia inclui: metais, polímeros, hidrogéis, materiais biorreabsorvíveis, cerâmicas e vitrocerâmicas, materiais naturais, compósitos, bem como camadas finas, revestimentos e enxertos superficiais, têxteis e materiais funcionais (que respondem ativamente a estímulos). Isso está resumido na Parte I da monografia, e capítulos detalhados discutem as características, propriedades e aplicações de classes individuais.
Na prática clínica, o material raramente ocorre sozinho, mas forma um dispositivo médico com geometria, rugosidade, pureza e histórico de processamento específicos; por exemplo, os capítulos nas partes II e VII descrevem implantes vasculares, elétrodos, sensores, implantes dentários e ortopédicos e sistemas de administração de medicamentos.
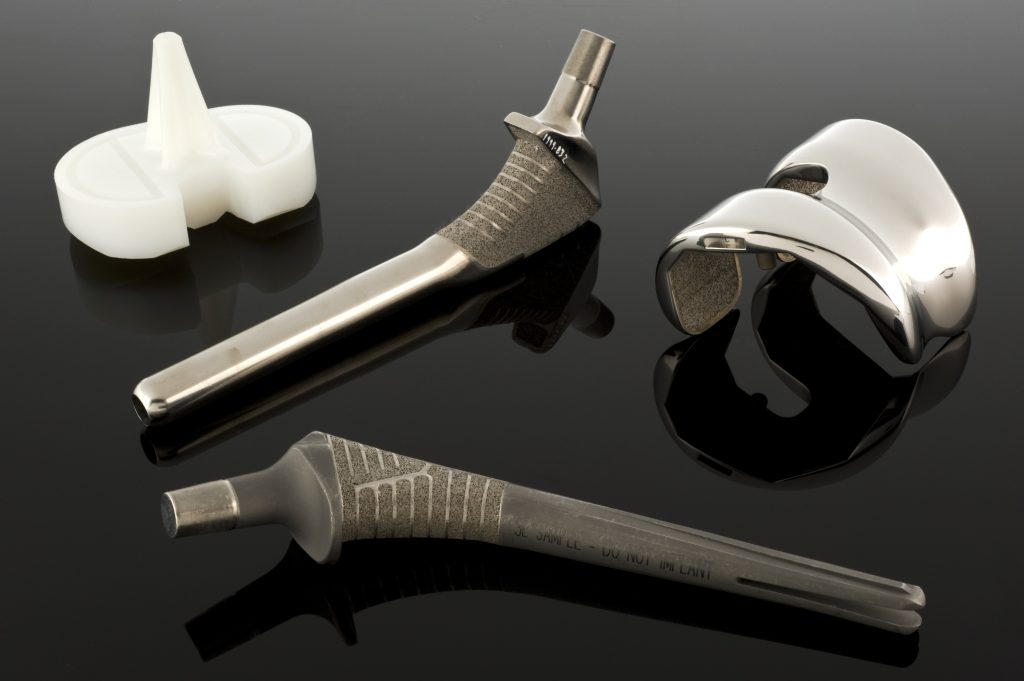
Os metais (por exemplo, aços Cr-Ni-Mo, ligas Co-Cr, ligas de titânio) continuam a ser a base para implantes sujeitos a cargas mecânicas (placas, parafusos, endopróteses, componentes de válvulas). As propriedades mecânicas, a vida útil à fadiga e a resistência à corrosão são fundamentais, e o seu nível depende fortemente do histórico de processamento (desde a fundição, passando pelo trabalho plástico, até ao tratamento térmico) e da microestrutura.
Os polímeros (de termoplásticos a elastómeros e resinas reticuladas) proporcionam flexibilidade, baixa densidade, facilidade de moldagem e a capacidade de modificar a microestrutura e a função (por exemplo, revestimentos hemocompatíveis, géis condutores, membranas). Os capítulos sobre polímeros enfatizam a importância do peso molecular (Mn, Mw), polidispersidade e taticidade para as propriedades mecânicas e de processamento. Do ponto de vista operacional, a transição vítrea (Tg), a fusão cristalina (Tm) e o patamar da borracha, visíveis nos testes DMA, são críticos.
Cerâmicas e vitrocerâmicas, que variam de óxidos (como alumina e zircónia) a vidros bioativos, são fundamentais em aplicações onde alta dureza, estabilidade química e bioatividade são necessárias, por exemplo, em odontologia restauradora e reparação de defeitos ósseos. Estes materiais podem formar uma ligação forte e mediada quimicamente com o tecido (bioatividade), o que é discutido em detalhes na aula “biocerâmicas”.
Os materiais naturais (colagénio, elastina, polissacarídeos) estão a ganhar importância na engenharia de tecidos devido à sua semelhança com a matriz extracelular e ao seu potencial para promover a regeneração (por exemplo, arcabouços de pele ou nervos).
A escolha do material está ligada à localização anatómica e ao regime de tensão: as válvulas cardíacas requerem resistência à fadiga e à coagulação sanguínea; as endopróteses da anca requerem alta resistência e pares de atrito adequados; os implantes dentários requerem biointegração e estanqueidade biológica da passagem dos tecidos moles. O Capítulo VII fornece descrições detalhadas destes requisitos para tipos específicos de produtos.
Propriedades de volume e superfície
Nos biomateriais, distinguimos entre propriedades de volume (resistência, módulo, resistência ao impacto, fluência, fadiga e condutividade) e propriedades de superfície (energia e química da superfície, carga, topografia e camada limite após adsorção de proteínas). Estas últimas determinam o primeiro contacto com o sangue e os tecidos – a cascata de adsorção de proteínas, ativação celular e cascata de coagulação. A monografia inclui capítulos dedicados à adsorção de proteínas e à resposta do sangue ao material, bem como às correlações entre as propriedades da superfície e a resposta biológica.
Nos polímeros, a arquitetura das macromoléculas (lineares, ramificadas ou reticuladas), a cristalinidade, a taticidade e a distribuição do peso molecular determinam as respostas mecânicas e térmicas. Do ponto de vista da engenharia, os parâmetros que controlam o processamento (por exemplo, injeção, extrusão ou moldagem reativa) e o comportamento durante o ciclo de vida do produto são críticos. As distribuições de Mn/Mw, Tg e Tm, bem como os espectros DMA, servem de base para projetar estruturas de membrana, revestimentos e elastómeros implantáveis.
Mesmo diferenças subtis nas propriedades da superfície (química, nanotextura, histórico de esterilização) podem alterar radicalmente o perfil de adsorção de proteínas e, subsequentemente, afetar a trombogenicidade e a cicatrização, razão pela qual o gerenciamento da condição da superfície é tão importante quanto a seleção da composição química do material.
Como o corpo responde ao biomaterial?
Após a implantação, uma cadeia de reações do hospedeiro é desencadeada, incluindo hemostasia, inflamação aguda, proliferação e remodelação tecidual na presença de um corpo estranho. Isto resulta numa reação a corpos estranhos, caracterizada pela ativação crónica de macrófagos, pela formação de células gigantes de corpos estranhos e pelo desenvolvimento de uma cápsula fibrosa. Processos separados e complexos envolvem o contacto com o sangue (ativação plaquetária e cascata de coagulação) e o sistema imunitário (imunologia e sistema complemento). O compêndio dos capítulos 4.1–4.7 fornece uma estrutura conceitual e métodos para avaliar esta resposta.
O padrão de resposta depende do local de implantação, tamanho e rugosidade, bem como da composição do material e condição da superfície; até o mesmo material pode induzir diferentes fenótipos de macrófagos em tecidos moles e tecidos periosteais. Portanto, a avaliação da biocompatibilidade deve ser específica para cada aplicação (in vitro + in vivo).
Os testes de biomateriais abrangem estudos in vitro (células, proteínas e hemocompatibilidade), estudos in vivo (modelos animais e locais de implante), testes sangue-material e o desenho de modelos animais adaptados à indicação clínica. As diretrizes compiladas nas secções 5.1–5.5 estabelecem uma linguagem comum para laboratórios académicos e industriais, bem como para avaliação regulatória. Os resultados de um nível (por exemplo, in vitro) não podem ser extrapolados diretamente para resultados clínicos; a triangulação de dados (análise in vitro–in vivo–explante) é o padrão ouro no desenvolvimento e supervisão de produtos.
Degradação e envelhecimento num ambiente biológico
O corpo não é um ambiente simples para o design de materiais. É rico em proteínas, enzimas e células capazes de gerar espécies reativas de oxigénio e cloro. Neste ambiente, os materiais estão sujeitos a hidrólise, oxidação, corrosão, fadiga, fissuração por tensão e até mineralização patológica. As secções 6.1–6.5 fornecem uma visão geral transversal dos mecanismos de degradação de polímeros, metais e cerâmicas.
Particularmente instrutivo é o mecanismo pelo qual o polímero hospedeiro oxida. Na inflamação aguda, os neutrófilos produzem anião superóxido, peróxido de hidrogénio e (com a participação da mieloperoxidase) ácido hipocloroso (HOCl); os macrófagos, que dominam cronicamente (juntamente com as células gigantes), sustentam a emissão de radicais livres, e a adesão da MPO à superfície do corpo estranho pode fornecer um catalisador no local da implantação. Este ambiente promove a oxidação das ligações éter e uretano, bem como o início de fissuras e rachaduras por tensão em elastómeros de uretano, fenómenos observados, entre outros, em componentes de poliuretano de elétrodos e cabos de marcapassos.
A degradação é sinérgica: cargas alternadas produzem microfissuras e uma superfície nova e reativa; a absorção de água altera o pH local e facilita a difusão de reagentes; os produtos da hidrólise aumentam a hidrofilicidade e a penetração de agentes de degradação. O controlo da composição, a estabilização antioxidante e as condições de tensão residual são críticos para a segurança a longo prazo.
Em metais corrosivos, a degradação inclui corrosão por pite e corrosão em fendas, corrosão sob tensão e desgaste tribológico em pares de atrito, o que pode levar a partículas soltas e reações teciduais. As cerâmicas, embora quimicamente mais estáveis, são frágeis e sensíveis a defeitos que iniciam fissuras; portanto, seu projeto requer um controle rigoroso de defeitos.
Exemplos de aplicações clínicas
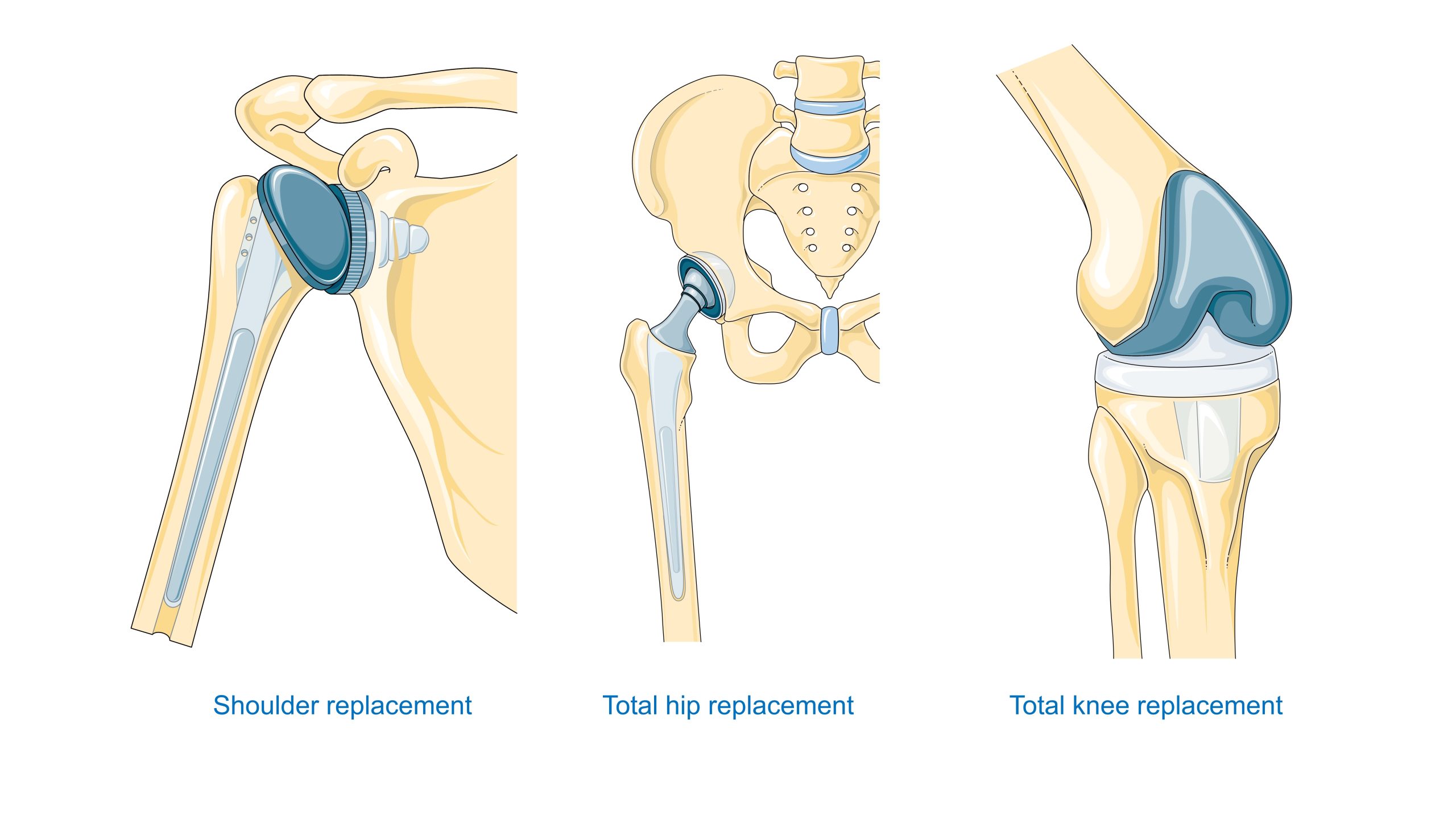
Sistema cardiovascular. Os materiais para válvulas, enxertos, stents, sistemas extracorpóreos e órgãos artificiais devem encontrar um equilíbrio entre hemocompatibilidade e durabilidade mecânica, bem como resistência à deposição de proteínas/células. As estratégias não trombogénicas incluem modificações de superfície (como heparinização e hidrogeles) e controlo da energia de superfície.
Odontologia. Os implantes de titânio e zircónio revolucionaram a reabilitação protética. O sucesso depende da biointegração com o osso (mais precisamente, adesão estreita e retenção mecânica) e da estanqueidade da passagem através da membrana mucosa. Os materiais para restaurações (cerâmicas preciosas, vitrocerâmicas) beneficiam dos avanços em biocerâmicas e usinagem de precisão.
Ortopedia. As endopróteses de anca e joelho exigem um compromisso entre resistência estática e à fadiga, resistência ao desgaste e propriedades tribológicas do par de atrito (metal-polietileno UHMWPE, cerâmica-cerâmica, metal-metal). Além disso, a ligação com o osso é crucial: comparando cimento acrílico com revestimentos porosos para osseointegração.
Fabricação de precisão, microestrutura e engenharia de superfícies
No caso de implantes metálicos, as propriedades resultam de toda a cadeia de processamento, desde a fusão e refinação, passando pela deformação plástica e tratamento térmico, até à maquinagem, soldagem, revestimento e esterilização. A microestrutura (tamanho do grão, fases, textura) e os defeitos induzidos pelo processo influenciam a resistência à fadiga e a resistência à corrosão. A introdução de revestimentos e estruturas porosas (por exemplo, malhas sinterizadas, pulverizações de plasma) é um exemplo de uma tarefa interdisciplinar: a adesão, rigidez, topografia e integridade à fadiga de todo o componente devem ser equilibradas.
Nos polímeros, os parâmetros de processamento (temperatura, tempo e tensões residuais) são igualmente importantes, assim como a seleção de estabilizadores antioxidantes e o controlo de pureza, pois estes fatores determinam a bioestabilidade subsequente. Na prática, houve casos de fissuração por tensão em poliuretanos usados em elétrodos de pacemakers, especificamente na interface entre tensões residuais, o ambiente biológico e a oxidação pelo hospedeiro.
A engenharia de superfícies é um conjunto de ferramentas para modificar propriedades, que vão desde revestimentos físico-químicos até a aplicação de filmes finos e camadas de polímeros enxertados, bem como micro/nanotopografia. As correlações entre os parâmetros da superfície e a resposta biológica são o tema de capítulos práticos dedicados.
Para dispositivos implantados a longo prazo, pequenas decisões de processo (por exemplo, tipo de esterilização, condições de envelhecimento de armazenamento) podem tornar-se as principais causas de diferenças clínicas anos mais tarde; documentar o histórico de processamento e o controlo de qualidade são partes integrantes do projeto de biomateriais.
Ética, regulamentos e normas
Os produtos são colocados no mercado sob rigorosos sistemas de avaliação, incluindo a FDA e a ISO. O custo para demonstrar segurança e eficácia é significativo, mas protege os pacientes e molda a política de qualidade. Ao mesmo tempo, surgem questões éticas: como equilibrar os interesses dos pacientes e as pressões económicas, como projetar estudos com risco mínimo, quando e como retirar soluções obsoletas. Essas questões, juntamente com o papel das normas consensuais e do desenvolvimento tecnológico, são discutidas na seção sobre novos produtos e normas. O progresso clínico requer progresso simultâneo na metodologia de avaliação, nas normas e na ética; caso contrário, a inovação pode ser ilusória ou arriscada.
Perspetivas
No horizonte estão materiais biologicamente funcionais (sensíveis a estímulos) e sistemas avançados de biossensores e órgãos artificiais (implantáveis e extracorpóreos) que tornam a interface biomaterial o centro da informática fisiológica. O seu sucesso dependerá do controlo subtil das interações superficiais, da estabilidade a longo prazo e da proteção contra a degradação. A secção da monografia dedicada a órgãos artificiais e biossensores mostra como os materiais, a eletrónica e a biologia devem trabalhar em estreita colaboração. O futuro dos biomateriais está nos sistemas híbridos, que exigirão um controlo ainda mais meticuloso da microestrutura e da superfície.
Biomateriais na medicina e na odontologia – resumo
Os biomateriais são componentes ativos da terapia que co-criam o microambiente biológico. O sucesso é determinado igualmente pela escolha da classe de material, engenharia de superfície, microestrutura e histórico de processamento, bem como pela compreensão da resposta do hospedeiro e dos mecanismos de degradação ao longo do tempo. Metais, polímeros e cerâmicas trazem diferentes conjuntos de vantagens e riscos; polímeros naturais e sistemas bioativos expandem a paleta com funções regenerativas. De uma perspetiva clínica, cada projeto apresenta um problema de otimização multiobjetiva para uma indicação específica e população de pacientes, que a monografia sistematiza, progredindo de definições e propriedades, passando pela biologia de contato e testes, até os aspectos práticos da implantação e análise de explantes. Por fim, a fabricação de precisão e o controlo de qualidade não são a última etapa, mas parte integrante da ciência dos biomateriais, pois ditam o comportamento a longo prazo do material no corpo.
A competência abrangente no design de biomateriais é a capacidade de combinar a ciência dos materiais com a biologia e a engenharia de produtos, desde a química e a microestrutura, passando pela superfície, até à fabricação e esterilização. Isso resulta em uma solução clínica única e bem documentada, verificada na via clínica in vitro-in vivo.
Bibliografia
Ratner, B.D., Hoffman, A.S., Schoen, F.J., Lemons, J.E. (eds.). Biomaterials Science: An Introduction to Materials in Medicine. Academic Press, San Diego–Londres–Boston–Nova Iorque–Sydney–Tóquio–Toronto, 1996.