Elementos aleantes en aleaciones de hierro y carbono

Índice
El acero al carbono puede alcanzar una amplia gama de propiedades mediante el tratamiento térmico pero, en muchas aplicaciones, esto sigue sin ser suficiente. La introducción de componentes distintos del hierro y el carbono en el acero (o el aumento del contenido de ciertos aditivos, como el manganeso y el silicio) da lugar a un grupo de materiales denominados aceros aleados. Estos elementos añadidos deliberadamente, llamados aditivos de aleación, interactúan simultáneamente con el hierro, el carbono y entre sí, lo que da lugar a un cambio en la estructura y las propiedades. Esto permite conseguir mayores propiedades mecánicas y tecnológicas, una mayor templabilidad, alta dureza y resistencia a la abrasión, así como propiedades especiales (por ejemplo, resistencia a la corrosión, resistencia al calor o resistencia térmica).
Al mismo tiempo, el acero aleado suele ser más caro, por lo que se utiliza cuando el acero al carbono no cumple los requisitos. En la práctica, también es importante que los aceros aleados se utilicen con mayor frecuencia en estado tratado térmicamente, ya que solo así se manifiestan plenamente los efectos de la aleación. Es decir, cambio en la cinética de la transformación de la austenita, diferente tendencia al crecimiento del grano, posibilidad de producir y estabilizar carburos de aleación y obtención de combinaciones favorables de dureza y plasticidad.
¿Cómo se clasifican los aceros aleados y por qué esta clasificación es, a veces, ambigua?
La clasificación de los aceros aleados puede basarse en varios criterios, pero la clasificación más habitual es según el tipo y la cantidad de aditivos aleantes, es decir, según la composición química. De ahí aparecen nombres como aceros al cromo, aceros al manganeso o aceros al cromo‑níquel. Sin embargo, el material señala que, con las composiciones químicas cada vez más complejas de hoy en día, esta clasificación es menos clara, ya que el acero puede contener varios aditivos importantes al mismo tiempo y su comportamiento depende de su combinación, no solo del elemento «principal».
Desde el punto de vista de la tecnología y la selección de materiales, la clasificación según la cantidad de aditivos de aleación en aceros de baja aleación, media aleación y alta aleación es igualmente importante y, con contenidos muy bajos, nos referimos a aceros microaleados. La clasificación según la aplicación también tiene una gran importancia práctica: distinguimos entre aceros estructurales, aceros para herramientas y aceros con propiedades especiales. Hay una lógica simple detrás de esta clasificación: diferentes aplicaciones requieren diferentes «mecanismos» de refuerzo (por ejemplo, precipitación de carburo, mayor templabilidad, estabilización de la estructura a altas temperaturas, etc.) y, por lo tanto, diferentes aditivos.
Marcado de aceros aleados
El material describe un sistema de marcado en el que la marca del acero consta de números y letras, y su significado está estrechamente relacionado con la composición. El primer número suele indicar el contenido medio de carbono en centésimas de porcentaje, mientras que los números que siguen a las letras indican el contenido medio de un elemento de aleación determinado en porcentaje. Si no hay ningún número después de la letra, significa que el contenido del elemento no supera el 1,5 %. Además, los aceros de mayor calidad con un contenido muy bajo de fósforo y azufre se marcan con la letra A al final de la marca.
También es importante señalar que, en el sistema citado, las letras proceden del alfabeto ruso y corresponden a elementos específicos (por ejemplo, la letra que designa al níquel, al cromo o al molibdeno en este sistema es diferente de la que se utiliza en los símbolos químicos modernos). El material también ofrece un ejemplo de cómo interpretar el marcado, ya que muestra cómo leer los rangos de contenido de carbono y aditivos principales a partir de la propia marca y cómo reconocer si el acero es de calidad ordinaria o superior.
En los aceros para herramientas, el sistema de marcado es diferente: al principio, hay letras que indican el grupo funcional (por ejemplo, aceros para trabajo en frío, trabajo en caliente y aceros rápidos) y las siguientes letras y números se utilizan para indicar los principales aditivos de aleación o sus grupos y para distinguir entre grados. El material también proporciona una lista de letras asignadas a los elementos en las marcas de las herramientas (por ejemplo, marcas separadas para tungsteno, vanadio, molibdeno, cromo, cobalto, etc.).
Elementos de aleación y alotropía del hierro
Uno de los efectos más importantes de la aleación es la influencia de los aditivos en el rango de estabilidad de los alótropos del hierro, es decir, en las temperaturas a las que puede existir la austenita (fase γ). El material divide los elementos en dos grupos básicos según cómo desplazan las temperaturas de transición A3 y A4. Los elementos del primer grupo disminuyen A3 y aumentan A4, lo que significa que el rango de existencia de la fase γ se amplía. Con un contenido suficientemente alto, puede darse una situación en la que la fase γ exista desde la temperatura ambiente hasta la temperatura de fusión: se trata de un sistema con un campo de austenita abierto. Este efecto se ha descrito para las aleaciones de hierro con níquel, cobalto y manganeso, que forman soluciones sólidas continuas con el hierro.
Si los elementos que expanden el campo γ no forman soluciones continuas, sino solo soluciones límite, el panorama es más complejo: el campo γ puede expandirse inicialmente, pero más tarde, como resultado de la aparición de rangos bifásicos, puede reducirse gradualmente hasta desaparecer. El material se refiere a este caso como un sistema con un campo de austenita expandido y ofrece ejemplos entre los que se incluyen ciertos sistemas con cobre u oro, así como la influencia de elementos intersticiales como el carbono y el nitrógeno.
El segundo grupo tiene el efecto contrario: estos elementos reducen A4 y aumentan A3, y con suficiente solubilidad en hierro, pueden conducir a la formación de un campo de austenita cerrado, limitado por el área de dos fases α + γ. Fuera de este campo, la ferrita existe desde temperaturas normales hasta el punto de fusión. El material enumera una amplia gama de elementos que presentan este efecto (entre ellos, aluminio, silicio, titanio, vanadio, cromo, molibdeno, tungsteno y otros). Cuando la solubilidad en γ es demasiado baja, en lugar de un campo cerrado, se forma un sistema con un campo de austenita reducido, como se describe, por ejemplo, para las aleaciones con boro, circonio y cesio.

¿En qué forma se presentan los aditivos de aleación en el acero?
El funcionamiento de un aditivo depende, en gran medida, de dónde y en qué forma se encuentra en la microestructura. El material enumera varias posibilidades: los elementos de aleación pueden presentarse en una solución sólida, como los carburos, como inclusiones no metálicas, como compuestos intermetálicos o, en raras ocasiones, en forma libre. Al mismo tiempo, se destaca que, en los aceros aleados utilizados en la práctica, hay dos formas que revisten una importancia fundamental: la solución sólida y los carburos, ya que son los que determinan en mayor medida las propiedades y el comportamiento durante el tratamiento térmico.
Las inclusiones no metálicas suelen aparecer en pequeñas cantidades, y su influencia depende más de su forma, tamaño y distribución que de su composición química. Se pueden formar compuestos intermetálicos, pero normalmente solo con contenidos muy elevados de aditivos, por lo que en los aceros de ingeniería típicos son menos importantes que la solución sólida y los carburos. Esta conclusión orienta el análisis posterior: si queremos comprender por qué el acero aleado es más duro, más templable o más resistente al sobrecalentamiento, normalmente tenemos que fijarnos en el endurecimiento por solución y en el papel de los carburos de aleación.
El efecto de los aditivos en la solución sólida sobre la ferrita
Muchos elementos aleantes se disuelven en ferrita o austenita, pero el grado de esta solubilidad es individual y está relacionado, entre otras cosas, con la correspondencia entre los tamaños de los átomos. El material hace referencia al criterio de la diferencia de diámetro atómico y muestra el rango en el que la formación de soluciones sólidas es especialmente favorable. Además, nos recuerda los elementos intersticiales (como el carbono, el nitrógeno o el boro) que forman soluciones intersticiales en el hierro.
El efecto técnico más importante es el siguiente: los aditivos disueltos en ferrita aumentan la resistencia a la tracción, el límite elástico y la dureza, mientras que disminuyen las propiedades plásticas. El material señala que cuanto mayor es la diferencia entre un elemento dado y el hierro (por ejemplo, en términos de tamaño atómico), mayor es el cambio. También se proporciona información cualitativa sobre qué elementos endurecen más la ferrita. Por ejemplo, el manganeso, el silicio y el níquel, entre otros, provocan un endurecimiento significativo, mientras que el efecto del cromo, el molibdeno y el tungsteno es menos pronunciado. En cuanto a la resistencia al impacto, se indica que la mayoría de estos elementos (con excepción del cromo y el níquel) la reducen y que, de los aditivos considerados, el níquel es el más beneficioso, ya que puede aumentar tanto la dureza como la resistencia al impacto.
También vale la pena tener en cuenta la dependencia de la velocidad de enfriamiento. El material describe que la ferrita que contiene níquel, cromo o manganeso en solución puede formar una estructura similar a una aguja, parecida a la martensita, cuando se enfría rápidamente, lo que da lugar a un aumento de la dureza de 100‑150 HB en comparación con el estado después de un enfriamiento lento. Sin embargo, en el caso de la ferrita con silicio, molibdeno o tungsteno, esta dependencia de la velocidad de enfriamiento es insignificante. Se trata de una observación importante, ya que demuestra que incluso «la misma composición» puede dar lugar a diferentes durezas si se modifica el proceso de enfriamiento.
Carburos de aleación
En los aceros aleados, no solo la solución sólida desempeña un papel fundamental, los carburos también suelen hacerlo. El material explica que la tendencia de los elementos a formar carburos está relacionada con su estructura electrónica, y la conclusión práctica es que los elementos pueden clasificarse según su capacidad creciente para formar carburos estables: Fe, Mn, Cr, Mo, W, V, Ti, Zr y Nb. Cuanto más estable es el carburo, mayor es la temperatura a la que se disuelve en austenita durante el calentamiento y más difícil es separarlo de la martensita durante el templado, lo que afecta directamente a la selección de las temperaturas de austenización y templado en los aceros aleados.
El material también cita la clasificación de Goldschmidt, que organiza los tipos de carburos según la estructura cristalina y las propiedades. Los carburos del grupo I, con una red regular de tipo NaCl y fórmula MC (por ejemplo, TiC, ZrC, VC o NbC), son muy estables, tienen puntos de fusión muy altos y una dureza muy elevada. El grupo II incluye carburos con una red hexagonal compacta, del tipo MC o M2C (por ejemplo, WC, W2C o MoC), con puntos de fusión y dureza ligeramente inferiores. El grupo III está formado por carburos M3C con una estructura de cementita (incluidos Fe3C y Mn3C), con una dureza inferior en comparación con los carburos más estables de los grupos I y II.
Al mismo tiempo, se hizo hincapié en que los carburos de aleación rara vez se presentan «en su forma pura». Por lo general, contienen hierro en solución y, si el acero tiene varios aditivos, los carburos también pueden contener estos elementos. Los carburos con una estructura similar pueden disolverse entre sí (por ejemplo, la cementita y el carburo de manganeso), y los aceros también contienen carburos con patrones más complejos, como M23C6 o M7C3. El material también destaca una importante distinción tecnológica: los carburos simples, como MC y M2C, son muy estables y difíciles de disolver en austenita, incluso a altas temperaturas, mientras que los carburos complejos se disuelven más fácilmente cuando se calientan.
Elementos formadores y no formadores de carburo
El material propone una clasificación conveniente de los elementos de aleación basada en su interacción con el carbono. El grupo no formador de carburos incluye, entre otros, Ni, Si, Co, Al, Cu y N. En los aceros, estos elementos suelen presentarse en una solución sólida en hierro, con importantes excepciones: el cobre con un contenido superior al 0,5 % aproximadamente puede formar una fase separada (una solución sólida en una matriz de cobre), y el nitrógeno puede formar compuestos en forma de nitruros.
Los elementos formadores de carburo son más «duales»: pueden aparecer tanto en solución sólida como en forma de carburos, y la forma que predomina depende del contenido de carbono y de qué otros elementos formadores de carburo estén presentes. El material proporciona una lógica práctica en este caso: con un mayor contenido de carbono y una pequeña cantidad de aditivos formadores de carburo, estos elementos se encontrarán principalmente en carburos, mientras que, con un bajo contenido de carbono y un alto contenido de aditivos formadores de carburo, el carbono se unirá en carburos y los aditivos «excedentes» permanecerán en la solución sólida. Los elementos que se unirán primero en los carburos vienen determinados por su afinidad por el carbono.
En este punto, el material destaca claramente que el efecto de los carburos sobre las propiedades es, en general, mucho más fuerte que el endurecimiento de la ferrita por los aditivos disueltos en la solución. Además, el «poder» de los carburos en la práctica viene determinado, principalmente, por su dispersión y morfología: las partículas de carburo grandes tienen un efecto endurecedor menor, los precipitados en forma de placa perjudican más la plasticidad que los esferoidales con la misma dureza, y los carburos en los límites de grano pueden provocar fragilidad.
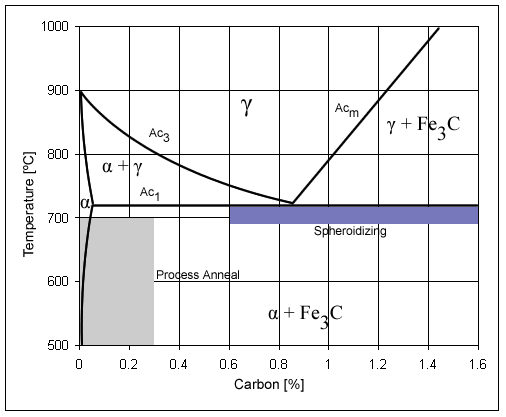
¿Cómo cambian los aditivos de aleación el sistema Fe‑Fe₃C?
La introducción de aditivos de aleación cambia la posición de las temperaturas y los puntos característicos en el sistema hierro-cementita. El material indica que los elementos que amplían el rango de la fase γ reducen la temperatura de transformación Ac3, mientras que los elementos que reducen el campo γ aumentan Ac3, lo que es especialmente evidente con un bajo contenido de carbono. Un efecto similar (hasta cierto punto) se aplica a la temperatura de transformación eutectoide, ya que también se produce una transformación alotrópica «en segundo plano».
El efecto sobre la concentración de carbono en el punto eutectoide también es muy importante. El material indica que todos los elementos de aleación desplazan el punto S de perlita hacia la izquierda, es decir, hacia los contenidos de carbono más bajos, lo que reduce el contenido de carbono en la perlita de la aleación. Del mismo modo, la mayoría de los aditivos desplazan el punto E, que determina el límite de solubilidad del carbono en la austenita, hacia la izquierda. Los que ejercen un efecto más fuerte (en orden ascendente de efecto) son W, Si, Cr, Mo, V y Ti. El desplazamiento del punto E puede ser tan grande que, incluso con un contenido de carbono inferior al 2 % en los aceros aleados, puede aparecer una estructura ledeburítica, lo que es una clara señal de que un simple diagrama Fe‑Fe₃C ya no es suficiente para predecir la estructura de los aceros aleados.
El material extrae una conclusión metodológica inequívoca de esto: cuantos más aditivos haya y mayor sea su contenido, más cambian las temperaturas de transformación y la posición de los puntos característicos, por lo que en el caso de los aceros aleados no se debe utilizar «mecánicamente» solo el sistema hierro‑cementita, sino tener en cuenta la naturaleza multicomponente del equilibrio.
La influencia de los aditivos en los gráficos CTPi
Lo más «práctico» para el tratamiento térmico es cómo los aditivos de aleación cambian las transformaciones de la austenita sobreenfriada visibles en los gráficos CTPi. El material explica que los elementos que no forman carburos (por ejemplo, Ni, Cu, Si, Al o Co) normalmente no cambian la forma de las curvas del comienzo y el final de la transformación de austenita, sino que las desplazan hacia la derecha, lo que implica un aumento de la estabilidad de la austenita sobreenfriada y una ralentización de sus transformaciones. Al mismo tiempo, se indica una excepción: el cobalto puede actuar de manera diferente y acelerar la transformación.
En el caso de los elementos formadores de carburo, el panorama es más complejo, especialmente con contenidos de carbono más elevados. El material indica que estos aditivos provocan, en particular, un retraso en la transformación perlítica, a menudo también un aumento de la temperatura máxima de transformación perlítica (con la excepción del manganeso), una reducción del límite superior de las temperaturas de transformación bainítica y un retraso en la transformación bainítica, pero normalmente menor que en la transformación perlítica. El resultado es una «extensión» de los rangos de transformación perlítica y bainítica que pueden solaparse en los aceros no aleados. Al aumentar el contenido de aditivos de aleación, pueden aparecer dos máximos distintos de velocidad de transformación, separados por un rango de alta estabilidad de austenita.
Sin embargo, es muy importante señalar que el efecto de los aditivos formadores de carburo sobre la estabilidad de la austenita depende de la cantidad que realmente esté presente en la austenita, es decir, de si han tenido tiempo de disolverse durante la austenización. El material destaca que los elementos formadores de carburos aumentan la estabilidad de la austenita sobreenfriada solo si se han disuelto completamente en ella durante el calentamiento. Si, por el contrario, permanecen como carburos sin disolver, el efecto puede ser el contrario: la austenita se empobrece en aditivos y carbono, y los propios carburos pueden actuar como núcleos y favorecer una transformación acelerada. Esto explica por qué la temperatura y el tiempo de austenización adecuados son tan importantes en los aceros aleados.
Elementos aleantes en aleaciones de hierro y carbono: resumen
Desde una perspectiva de ingeniería, los elementos de aleación en los aceros Fe‑C pueden entenderse como una herramienta que opera en tres niveles relacionados. En primer lugar, modifican el equilibrio de fases al desplazar las temperaturas de transformación y la estabilidad de la austenita, a veces hasta el punto de formar sistemas con un campo γ abierto, cerrado o reducido. En segundo lugar, influyen en la cinética de las transformaciones al desplazar los diagramas CTPi, aumentar la estabilidad de la austenita, cambiar la relación perlita‑bainita y configurar la templabilidad al reducir la velocidad crítica de enfriamiento. En tercer lugar, desarrollan propiedades a través de la microestructura: endurecen la ferrita en solución pero, sobre todo, a través de los carburos de aleación, permiten un fuerte endurecimiento, el control del crecimiento del grano y efectos especiales durante el templado, incluida la dureza secundaria.
En la práctica, esto significa que los aditivos de aleación no son «bonificaciones a la composición», sino elementos de un sistema de control de la estructura: su efecto real depende de si se disuelven en austenita o se presentan como carburos, cuál es su dispersión y cómo se desarrollan la austenización, el enfriamiento y el templado. Solo una visión coherente de estas relaciones permite aprovechar todo el potencial de los aceros aleados.


