Biomaterialen in de geneeskunde en tandheelkunde
Inhoudsopgave
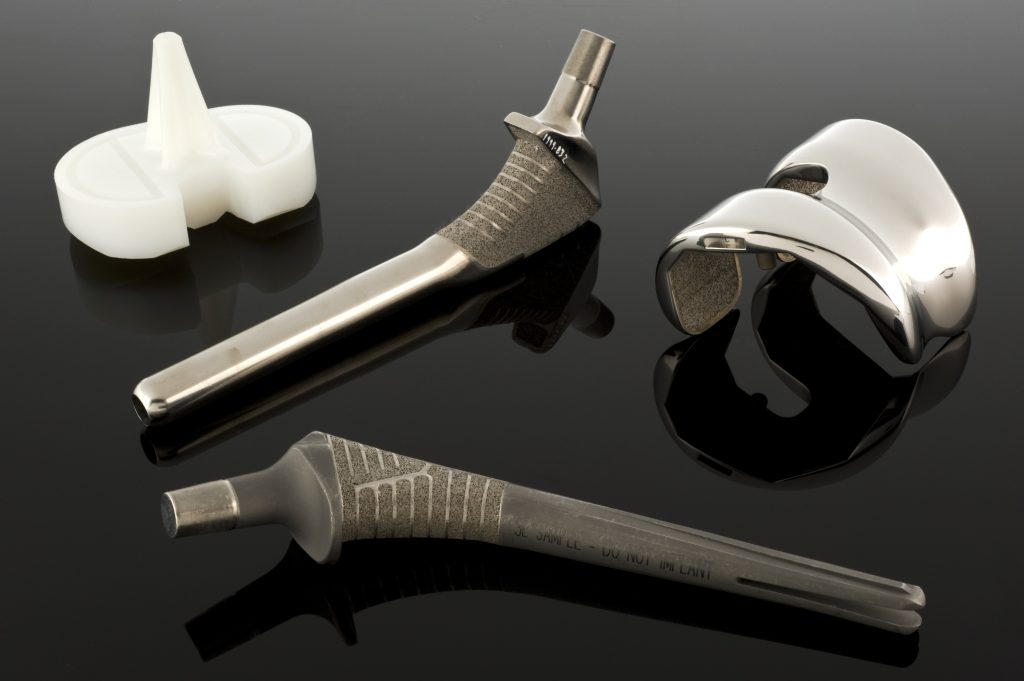
Biomaterialen vormen de ruggengraat van de moderne reconstructieve geneeskunde en tandheelkunde. Hun toepassingen variëren van hartkleppen en gewrichtsendoprothesen tot intraossale implantaten, sensoren, elektroden en systemen voor medicijnafgifte. Dit artikel heeft tot doel een beknopt maar volledig overzicht te geven van hun definitie, biocompatibiliteitseisen, primaire klassen, interactiemechanismen met het lichaam, testmethoden en afbraakprincipes, en de belangrijkste aspecten van oppervlakte-engineering en precisieproductie te belichten die bepalend zijn voor het klinische succes van een product. Het artikel is gebaseerd op de klassieke monografie “Biomaterials Science: An Introduction to Materials in Medicine”, onder redactie van B.D. Ratner et al. (Academic Press).
Biomaterialen moeten altijd worden geanalyseerd in de context van hun klinische toepassing, binnen een specifieke biologische omgeving en na het ondergaan van daadwerkelijke productie- en sterilisatieprocessen, aangezien deze stadia hun functionele eigenschappen en veiligheid bepalen.

Wat is een biomateriaal en wat is biocompatibiliteit?
In de terminologie die in de literatuur wordt gebruikt, is een biomateriaal een levenloos materiaal dat bedoeld is om in een medisch hulpmiddel in wisselwerking te treden met een biologisch systeem. De klinische aanvaardbaarheid ervan hangt af van de biocompatibiliteit, d.w.z. het vermogen om in een bepaalde toepassing een passende, bewust gewenste reactie van de gastheer op te wekken, d.w.z. een reactie die het beoogde therapeutische effect mogelijk maakt en geen onaanvaardbaar risico met zich meebrengt. Deze definities, die onder meer zijn vastgelegd in de werken van D.F. Williams en in de inleidende hoofdstukken van monografieën, zijn de hoeksteen geworden van de interdisciplinaire ontwikkeling van het vakgebied.
Biocompatibiliteit is een relatie tussen materiaal, hulpmiddel, patiënt en toepassing; hetzelfde materiaal kan in het ene product biocompatibel zijn en in het andere product problematisch.
Historisch gezien omvatten biomaterialen zowel metalen die worden gebruikt in prothesen (bijvoorbeeld goud in de tandheelkunde) als materialen zoals glas of hout in externe prothesen. Het huidige begrip van de discipline heeft zich ontwikkeld samen met de kristallisatie van de wetenschappelijke gemeenschap, symposia en de oprichting van wetenschappelijke verenigingen; tegelijkertijd heeft de structuur van de vakliteratuur en normen vorm gekregen.
De systematiek van materialen die in de geneeskunde en tandheelkunde worden gebruikt, omvat: metalen, polymeren, hydrogels, bioresorbeerbare materialen, keramiek en glaskeramiek, natuurlijke materialen, composieten, evenals dunne lagen, coatings en oppervlaktetransplantaten, textiel en functionele materialen (die actief reageren op prikkels). Dit wordt samengevat in deel I van de monografie, en in gedetailleerde hoofdstukken worden de kenmerken, eigenschappen en toepassingen van afzonderlijke klassen besproken.
In de klinische praktijk komt het materiaal zelden op zichzelf voor, maar vormt het een medisch hulpmiddel met een specifieke geometrie, ruwheid, zuiverheid en verwerkingsgeschiedenis; in de hoofdstukken in deel II en VII worden bijvoorbeeld vasculaire implantaten, elektroden, sensoren, tandheelkundige en orthopedische implantaten en systemen voor de toediening van geneesmiddelen beschreven.
Metalen (bijv. Cr-Ni-Mo-staal, Co-Cr-legeringen, titaniumlegeringen) blijven de basis voor mechanisch belaste implantaten (platen, schroeven, endoprothesen, klepcomponenten). Mechanische eigenschappen, vermoeiingslevensduur en corrosiebestendigheid zijn van het grootste belang, en het niveau daarvan hangt sterk af van de verwerkingsgeschiedenis (van smelten via plastische bewerking tot warmtebehandeling) en de microstructuur.
Polymeren (van thermoplasten tot elastomeren en verknoopte harsen) bieden flexibiliteit, een lage dichtheid, vormbaarheid en de mogelijkheid om de microstructuur en functie te wijzigen (bijv. hemocompatibele coatings, geleidende gels, membranen). In de hoofdstukken over polymeren wordt het belang benadrukt van molecuulgewicht (Mn, Mw), polydispersiteit en tacticiteit voor mechanische en verwerkingseigenschappen. Vanuit operationeel oogpunt zijn de glasovergang (Tg), kristallijne smelting (Tm) en het rubberplateau, zichtbaar in DMA-tests, van cruciaal belang.
Keramiek en glaskeramiek, variërend van oxiden (zoals aluminiumoxide en zirkoniumoxide) tot bioactief glas, zijn cruciaal in toepassingen waar een hoge hardheid, chemische stabiliteit en bioactiviteit vereist zijn, bijvoorbeeld in de restauratieve tandheelkunde en bij het herstel van botdefecten. Deze materialen kunnen een sterke, chemisch gemedieerde binding met weefsel vormen (bioactiviteit), wat in detail wordt besproken in het hoofdstuk “biokeramiek”.
Natuurlijke materialen (collageen, elastine, polysacchariden) winnen aan belang in weefselengineering vanwege hun gelijkenis met de extracellulaire matrix en hun potentieel om regeneratie te bevorderen (bijvoorbeeld huid- of zenuwscaffolds).
De keuze van het materiaal hangt samen met de anatomische locatie en het spanningsregime: hartkleppen moeten bestand zijn tegen vermoeidheid en bloedstolling; heupendoprothesen moeten een hoge sterkte en geschikte wrijvingsparen hebben; tandheelkundige implantaten moeten zich biologisch integreren en biologisch goed afsluiten in het zachte weefsel. Hoofdstuk VII geeft een gedetailleerde beschrijving van deze vereisten voor specifieke soorten producten.
Volume- en oppervlakte-eigenschappen
Bij biomaterialen maken we onderscheid tussen volume-eigenschappen (sterkte, modulus, slagvastheid, kruip, vermoeidheid en geleidbaarheid) en oppervlakte-eigenschappen (oppervlakte-energie en chemie, lading, topografie en de grenslaag na eiwitadsorptie). Deze laatste bepaalt het eerste contact met bloed en weefsels — de cascade van eiwitadsorptie, celactivering en de coagulatiecascade. De monografie bevat hoofdstukken gewijd aan eiwitadsorptie en de reactie van het bloed op het materiaal, evenals correlaties tussen oppervlakte-eigenschappen en biologische reactie.
In polymeren bepalen de architectuur van macromoleculen (lineair, vertakt of verknoopt), kristalliniteit, tacticiteit en molecuulgewichtverdeling de mechanische en thermische reacties. Vanuit technisch oogpunt zijn de parameters die de verwerking (bijv. injectie, extrusie of reactief gieten) en het gedrag tijdens de levenscyclus van het product bepalen, van cruciaal belang. Mn-/Mw-, Tg- en Tm-verdelingen, evenals DMA-spectra, dienen als basis voor het ontwerpen van membraanstructuren, coatings en implanteerbare elastomeren.
Zelfs subtiele verschillen in oppervlakte-eigenschappen (chemie, nanotextuur, sterilisatiegeschiedenis) kunnen het eiwitadsorptieprofiel radicaal veranderen en vervolgens de trombogeniciteit en genezing beïnvloeden. Daarom is het beheer van de oppervlaktetoestand net zo belangrijk als de keuze van de chemische samenstelling van het materiaal.
Hoe reageert het lichaam op biomateriaal?
Na implantatie wordt een reeks reacties van het gastheerorganisme in gang gezet, waaronder hemostase, acute ontsteking, proliferatie en weefselhermodellering in aanwezigheid van een vreemd lichaam. Dit resulteert in een vreemd-lichaamsreactie, gekenmerkt door de chronische activering van macrofagen, de vorming van vreemd-lichaamsreuzencellen en de ontwikkeling van een fibreuze capsule. Afzonderlijke, complexe processen hebben betrekking op contact met bloed (bloedplaatjesactivering en de stollingscascade) en het immuunsysteem (immunologie en het complementsysteem). Het compendium van de hoofdstukken 4.1–4.7 biedt een conceptueel kader en methoden voor het evalueren van deze reactie.
Het responspatroon is afhankelijk van de implantatieplaats, de grootte en de ruwheid, evenals de materiaalsamenstelling en de toestand van het oppervlak; zelfs hetzelfde materiaal kan verschillende macrofaagfenotypes induceren in zacht weefsel en periostweefsel. Daarom moet de beoordeling van de biocompatibiliteit toepassingsspecifiek zijn (in vitro + in vivo).
Het testen van biomateriaal omvat in vitro-onderzoeken (cellen, eiwitten en hemocompatibiliteit), in vivo-onderzoeken (diermodellen en implantatieplaatsen), bloed-materiaal-tests en het ontwerpen van diermodellen die zijn afgestemd op de klinische indicatie. De richtlijnen die zijn samengevat in de paragrafen 5.1-5.5 vormen een gemeenschappelijke taal voor academische en industriële laboratoria, evenals voor regelgevende beoordelingen. Resultaten van één niveau (bijvoorbeeld in vitro) kunnen niet rechtstreeks worden geëxtrapoleerd naar klinische resultaten; triangulatie van gegevens (in vitro-in vivo-explantanalyse) is de gouden standaard bij productontwikkeling en -toezicht.
Afbraak en veroudering in een biologische omgeving
Het lichaam is geen eenvoudige omgeving voor materiaalontwerp. Het is rijk aan eiwitten, enzymen en cellen die reactieve zuurstof- en chloorspecies kunnen genereren. In deze omgeving zijn materialen onderhevig aan hydrolyse, oxidatie, corrosie, vermoeidheid, spanningsscheuren en zelfs pathologische mineralisatie. De paragrafen 6.1–6.5 geven een dwarsdoorsnedeoverzicht van de afbraakmechanismen van polymeren, metalen en keramiek.
Bijzonder leerzaam is het mechanisme waarbij het gastheerpolymeer oxideert. Bij acute ontstekingen produceren neutrofielen superoxide-anion, waterstofperoxide en (met medewerking van myeloperoxidase) hypochloorzuur (HOCl); macrofagen, die chronisch domineren (samen met reuzencellen), zorgen voor de afgifte van vrije radicalen, en MPO-adhesie aan het oppervlak van het vreemde lichaam kan een katalysator vormen op de implantatieplaats. Deze omgeving bevordert de oxidatie van ether- en urethaanbindingen, evenals het ontstaan van scheuren en spanningsscheuren in urethaanelastomeren, verschijnselen die onder andere worden waargenomen in polyurethaancomponenten van elektroden en pacemakerleidingen.
De degradatie is synergetisch: afwisselende belastingen veroorzaken microscheurtjes en een nieuw, reactief oppervlak; waterabsorptie verandert de lokale pH en vergemakkelijkt de diffusie van reagentia; hydrolyseproducten versterken de hydrofiliteit en de penetratie van degradatiemiddelen. Het beheersen van de samenstelling, de stabilisatie van antioxidanten en de restspanningsomstandigheden is van cruciaal belang voor de veiligheid op lange termijn.
Bij corrosieve metalen omvat degradatie putcorrosie en spleetcorrosie, spanningscorrosie en tribologische slijtage in wrijvingsparen, wat kan leiden tot losse deeltjes en weefselreacties. Keramiek is weliswaar chemisch stabieler, maar broos en gevoelig voor defecten die scheurtjes veroorzaken; daarom vereist het ontwerp ervan een strenge controle op defecten.
Voorbeelden van klinische toepassingen
Cardiovasculair systeem. Materialen voor kleppen, transplantaten, stents, extracorporale systemen en kunstmatige organen moeten een evenwicht vinden tussen hemocompatibiliteit en mechanische duurzaamheid, evenals weerstand tegen eiwit-/celafzetting. Niet-trombogene strategieën omvatten oppervlakteaanpassingen (zoals heparinisatie en hydrogels) en controle van de oppervlakte-energie.
Tandheelkunde – Implantaten van titanium en zirkonium hebben een revolutie teweeggebracht in prothetische rehabilitatie. Het succes hangt af van de bio-integratie met het bot (meer bepaald, nauwe hechting en mechanische retentie) en de dichtheid van de doorgang door het slijmvlies. Materialen voor restauraties (edelkeramiek, glaskeramiek) profiteren van de vooruitgang op het gebied van biokeramiek en precisiebewerking.
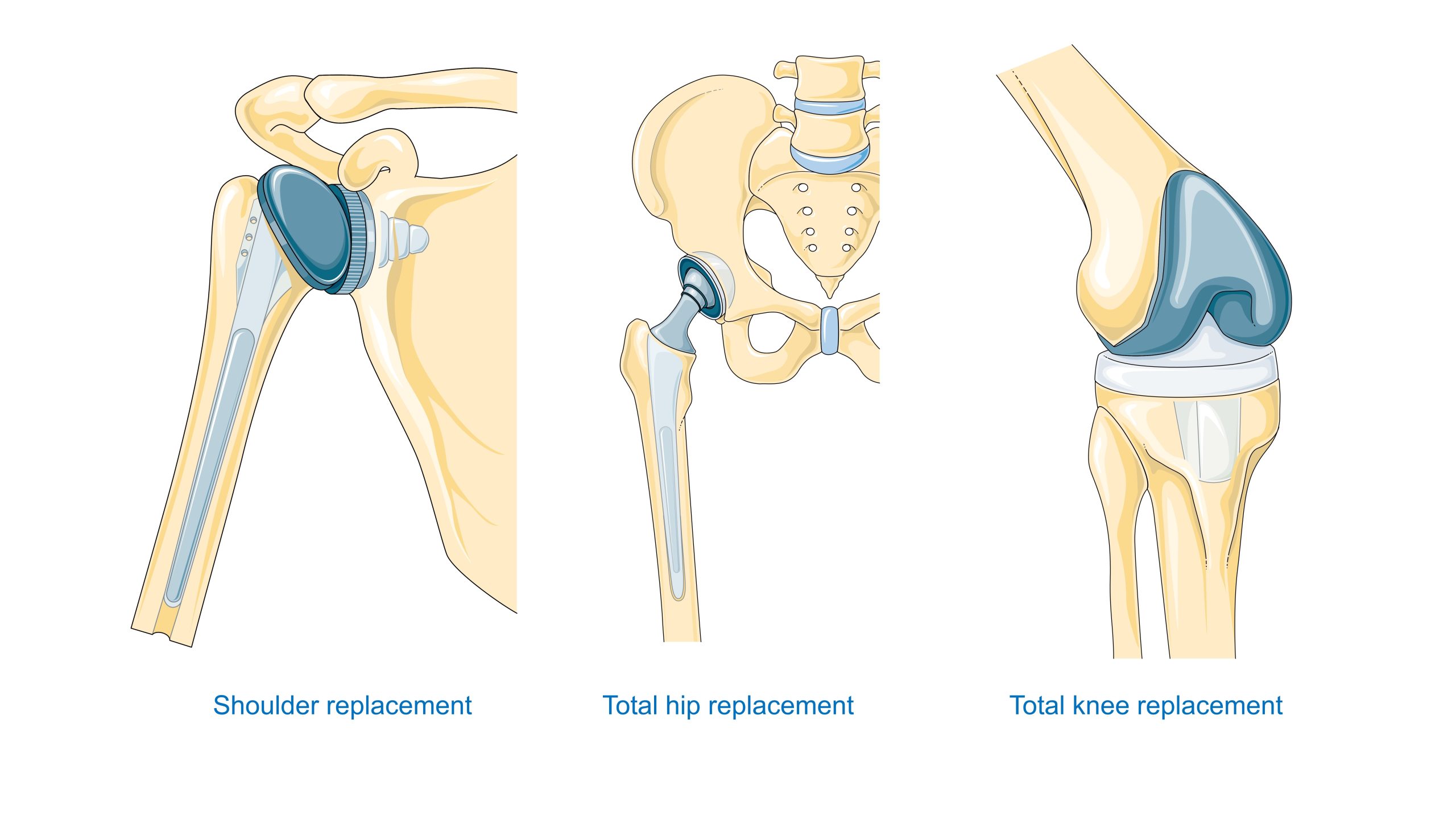
Orthopedie – Heup- en knie-endoprothesen vereisen een compromis tussen statische en vermoeiingssterkte, slijtvastheid en de tribologische eigenschappen van het wrijvingspaar (metaal-UHMWPE-polyethyleen, keramiek-keramiek, metaal-metaal). Bovendien is de verbinding met het bot cruciaal: vergelijking van acrylcement met poreuze coatings voor osseo-integratie.
Precisieproductie, microstructuur en oppervlakte-engineering
In het geval van metalen implantaten zijn de eigenschappen het resultaat van de gehele verwerkingsketen, van smelten en raffineren via plastische vervorming en warmtebehandeling tot machinale bewerking, lassen, coaten en steriliseren. Microstructuur (korrelgrootte, fasen, textuur) en door het proces veroorzaakte defecten beïnvloeden de vermoeiingssterkte en corrosiebestendigheid. De introductie van poreuze coatings en structuren (bijv. gesinterde gaasjes, plasmasprays) is een voorbeeld van een interdisciplinaire taak: de hechting, stijfheid, topografie en vermoeiingsintegriteit van het gehele onderdeel moeten in evenwicht zijn.
Bij polymeren zijn verwerkingsparameters (temperatuur, tijd en restspanningen) even belangrijk als de keuze van antioxidantstabilisatoren en zuiverheidscontrole, aangezien deze factoren bepalend zijn voor de latere biostabiliteit. In de praktijk zijn er gevallen geweest van spanningsscheuren in polyurethanen die worden gebruikt in pacemakerleidingen, met name op het raakvlak tussen restspanningen, de biologische omgeving en oxidatie door de gastheer.
Oppervlakte-engineering is een reeks hulpmiddelen voor het wijzigen van eigenschappen, variërend van fysisch-chemische coatings tot het aanbrengen van dunne films en geënte polymeerlagen, evenals micro-/nanotopografie. Correlaties tussen oppervlakteparameters en biologische respons zijn het onderwerp van speciale praktische hoofdstukken.
Voor langdurig geïmplanteerde apparaten kunnen kleine procesbeslissingen (bijv. type sterilisatie, opslag- en verouderingsomstandigheden) jaren later belangrijke oorzaken van klinische verschillen worden; het documenteren van de verwerkingsgeschiedenis en kwaliteitscontrole zijn integrale onderdelen van het ontwerp van biomaterialen.
Ethiek, regelgeving en normen
Producten worden op de markt gebracht onder strenge evaluatiesystemen, waaronder de FDA en ISO. De kosten voor het aantonen van veiligheid en werkzaamheid zijn aanzienlijk, maar het beschermt patiënten en vormt het kwaliteitsbeleid. Tegelijkertijd rijzen er ethische vragen: hoe kan een evenwicht worden gevonden tussen de belangen van patiënten en economische druk, hoe kunnen studies met minimaal risico worden ontworpen, wanneer en hoe moeten verouderde oplossingen worden teruggetrokken? Deze kwesties, samen met de rol van consensusnormen en technologische ontwikkeling, worden besproken in het hoofdstuk over nieuwe producten en normen. Klinische vooruitgang vereist gelijktijdige vooruitgang op het gebied van beoordelingsmethodologie, normen en ethiek; anders kan innovatie illusoir of risicovol blijken.
Vooruitzichten
Aan de horizon verschijnen biologisch functionele (op prikkels reagerende) materialen en geavanceerde biosensor– en kunstorgaan-systemen (implanteerbaar en extracorporaal) die de biomateriaalinterface tot het centrum van de fysiologische informatica maken. Hun succes zal afhangen van subtiele controle van oppervlakte-interacties, langdurige stabiliteit en bescherming tegen degradatie. Het hoofdstuk van de monografie dat gewijd is aan kunstorganen en biosensoren laat zien hoe nauw materialen, elektronica en biologie moeten samenwerken. De toekomst van biomaterialen ligt in hybride systemen, die een nog nauwkeurigere controle van de microstructuur en het oppervlak vereisen.
Biomaterialen in de geneeskunde en tandheelkunde – samenvatting
Biomaterialen zijn actieve componenten van therapieën die mede de biologische micro-omgeving creëren. Het succes wordt in gelijke mate bepaald door de keuze van de materiaalklasse, de oppervlaktebehandeling, de microstructuur en de verwerkingsgeschiedenis, evenals door inzicht in de reactie van de gastheer en de afbraakmechanismen in de loop van de tijd. Metalen, polymeren en keramiek hebben verschillende voordelen en risico’s; natuurlijke polymeren en bioactieve systemen breiden het palet uit met regeneratieve functies. Vanuit klinisch perspectief vormt elk project een multi-objectief optimalisatieprobleem voor een specifieke indicatie en patiëntenpopulatie, dat in de monografie wordt gesystematiseerd, van definities en eigenschappen, via contactbiologie en testen, tot de praktische aspecten van implantatie en explantatieanalyse. Ten slotte zijn precisieproductie en kwaliteitscontrole niet de laatste fase, maar een integraal onderdeel van de biomaterialenwetenschap, aangezien zij het langetermijngedrag van het materiaal in het lichaam bepalen.
De overkoepelende competentie in het ontwerpen van biomaterialen is het vermogen om materiaalkunde te combineren met biologie en productengineering – van chemie en microstructuur, via oppervlakte, tot productie en sterilisatie. Dit resulteert in één enkele, goed gedocumenteerde klinische oplossing, geverifieerd in het in vitro-in vivo-klinische traject.
Bibliografie
Ratner, B.D., Hoffman, A.S., Schoen, F.J., Lemons, J.E. (eds.). Biomaterials Science: An Introduction to Materials in Medicine. Academic Press, San Diego–Londen–Boston–New York–Sydney–Tokio–Toronto, 1996.





